Металлы являются одним из основных строительных блоков нашего мира. Они используются в различных отраслях промышленности и играют важную роль в технологических и научных процессах. Однако, металлы подвержены взаимодействию с различными веществами, включая концентрированные кислоты. Такое взаимодействие может привести к различным химическим реакциям и образованию новых соединений.
Одной из особенностей взаимодействия металла с концентрированными кислотами является их агрессивность. Концентрированные кислоты обладают высокой концентрацией активных ионов, что способствует разрушению структуры металла и приводит к его коррозии. В результате такого взаимодействия могут образоваться газы, растворы или осадки, в зависимости от химической природы металла и кислоты.
Возможные реакции между металлами и концентрированными кислотами включают образование солей, расщепление кислоты на воду и газы, а также реакции окисления и восстановления. Например, реакция между металлом и концентрированной соляной кислотой может привести к образованию хлоридов металла и выделению газа хлора. Подобные реакции могут быть использованы в различных процессах, включая производство химических соединений или очистку металлических поверхностей от коррозии.
Взаимодействие металла с концентрированными кислотами представляет собой сложный химический процесс, требующий учета множества факторов, включая химическую природу металла и кислоты, их концентрацию и температуру. Правильное понимание и контроль этих факторов позволяют использовать взаимодействие металла с концентрированными кислотами в различных отраслях промышленности и науки, а также предотвращать возможные негативные последствия, связанные с коррозией и разрушением металла.
Физические свойства металлов и кислот
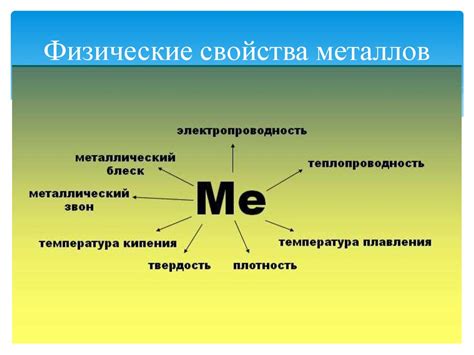
Металлы – это химические элементы, обладающие определенными физическими свойствами. Они характеризуются высокой теплопроводностью и электропроводностью, а также обладают блеском, довольно высокой плотностью и пластичностью.
У металлов есть различные особенности поведения при взаимодействии с концентрированными кислотами. Например, некоторые из них (например, золото и платина) химически инертны и не реагируют с кислотами. Другие металлы (например, железо и алюминий) могут реагировать с кислотами, образуя соответствующие соли и выделяя газы.
Кислоты – это химические соединения, которые могут растворяться в воде с образованием положительных и отрицательных ионов. Они обладают кислотной реакцией, т.е. могут отдавать протоны. Кислоты могут быть органическими (например, уксусная кислота) или неорганическими (например, серная кислота).
Реакция металлов с концентрированными кислотами может протекать с разной интенсивностью. Например, алюминий реагирует с соляной или серной кислотой, образуя газ водород и соответствующие соли. Некоторые металлы, такие как цинк или магний, могут реагировать с разными видами кислот, проявляя свою активность.
Влияние концентрации кислоты на химическую реакцию

Металлические материалы взаимодействуют с концентрированными кислотами, образуя различные химические соединения. Однако степень реакции и характер получаемого продукта зависят от концентрации кислоты.
При повышенной концентрации кислоты реакция с металлами протекает более интенсивно. Кислота максимально активна и образуется большее количество продукта реакции. Это происходит из-за увеличения количества активных ионов в растворе, что облегчает и ускоряет процесс взаимодействия с металлом.
Однако при неконтролируемой высокой концентрации кислоты может происходить разрушение металла с образованием агрессивных газов и температуры. Здесь необходимо учитывать не только концентрацию кислоты, но и специфические свойства металла и его способность выдерживать химические реакции.
Наоборот, при низкой концентрации кислоты реакция между металлом и кислотой происходит медленно и менее интенсивно. Металлическая поверхность меньше подвергается окислительному воздействию, что может замедлить реакцию. Однако это может быть не всегда нежелательным, так как низкая концентрация кислоты может не справиться с очисткой поверхности металла или формированием необходимого химического соединения.
Итак, концентрация кислоты является одним из главных факторов, влияющих на химическую реакцию с металлом. Она может значительно повлиять на скорость и степень реакции, а также на вид и свойства получаемого продукта. Для получения желаемого результата необходимо учитывать концентрацию кислоты и особенности взаимодействия с выбранным металлом.
Различные виды реакций между металлом и концентрированными кислотами

Взаимодействие металла с концентрированными кислотами может привести к различным реакциям, которые зависят от свойств и химической активности как металла, так и кислоты. Эти реакции могут быть классифицированы на несколько основных типов.
Первый тип реакции представляет собой образование соли металла и выделение водорода. Когда металл вступает в контакт с концентрированной кислотой, происходит окислительно-восстановительное взаимодействие, в результате которого образуется соль металла и выделяется водород. Например, при взаимодействии цинка с концентрированной серной кислотой образуется сульфат цинка и выделяется водородный газ.
Второй тип реакции связан с образованием нерастворимых солей. В некоторых случаях, при взаимодействии металла с концентрированной кислотой, образуется нерастворимая соль, которая оседает на поверхности металла и защищает его от дальнейшего взаимодействия с кислотой. Например, при реакции железа с концентрированной азотной кислотой образуется нерастворимый нитрат железа, который образует защитную пленку на поверхности металла.
Третий тип реакции характеризуется образованием комплексных соединений. Некоторые металлы могут образовывать соединения с кислотой, в которых металл играет роль лиганда. Эти соединения называются комплексами. Например, медь может образовывать комплексы с серной кислотой, в результате чего образуется сульфат меди (II).
И наконец, четвертый тип реакции представляет собой окислительную реакцию между металлом и кислородом из воздуха при наличии концентрированной кислоты. В этом случае, металл окисляется кислородом, а кислота восстанавливается. Например, при окислении алюминия концентрированной серной кислотой образуется алюминийсульфат и выделяется диоксид серы.
Особенности реакции с разными металлами

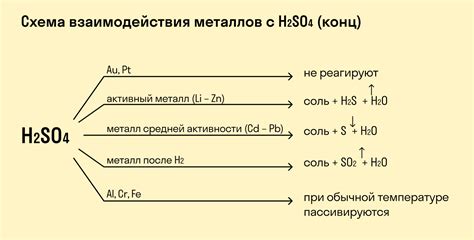
Реакция металлов с концентрированными кислотами зависит от их позиции в ряду активности металлов. Первая группа металлов – щелочные металлы (натрий, калий, литий) и алкалиноземельные металлы (магний, кальций) – являются наиболее активными и реагируют с кислотами со значительной выделением газов и тепла.
Железо, цинк, алюминий и свинец, относящиеся к группе относительно активных металлов, реагируют с некоторыми кислотами только при нагревании. При этом могут образовываться соответствующие соли и выделяться газы. Например, при взаимодействии цинка с концентрированной серной кислотой возникает выделение сернистого газа SO2.
Медь, серебро и золото относятся к малоактивным металлам. Они, как правило, не реагируют с концентрированными кислотами. Но некоторые металлы могут реагировать с некоторыми кислотами при высоких температурах или в особых условиях. Например, золото может растворяться в растворах цианида или арсенида.
Таким образом, особенности реакции металлов с концентрированными кислотами обусловлены их активностью и образованием соответствующих солей. Важно помнить, что реакции металлов с концентрированными кислотами часто сопровождаются выделением газа, который может быть опасен, поэтому необходимо соблюдать меры предосторожности при выполнении данных реакций.
Возможные применения реакции металла с концентрированными кислотами
Реакция металла с концентрированными кислотами имеет широкий спектр применений и находит применение в различных областях науки и промышленности. Одним из возможных применений является получение водорода, который является важным реагентом в химической промышленности и используется для производства аммиака, метанола и других продуктов. Также можно получить водородное топливо, которое является экологически чистым и перспективным источником энергии.
Другим важным применением реакции металла с концентрированными кислотами является процесс очистки металлических поверхностей от окиси и нежелательных примесей. При взаимодействии металла с кислотой возникает реакция, в результате которой ионный слой окиси разрушается, позволяя улучшить адгезию покрытий, как например, покрытий защитными лаками, красками или гальваническими покрытиями.
Также реакция металла с концентрированными кислотами может быть использована для аналитических целей. При взаимодействии металлов с кислотами происходит выделение газов, что позволяет определить наличие конкретных металлов в образце. Это широко применяется в химическом анализе для определения качественного и количественного содержания металлов в различных образцах и смесях веществ.
В целом, реакция металла с концентрированными кислотами является важным инструментом в химической промышленности, аналитике и поверхностных технологиях, позволяя получать водород, очищать металлы от нежелательных примесей и производить анализ содержания металлов в различных образцах.
Вопрос-ответ

Какие металлы реагируют с концентрированными кислотами?
С реакцией с концентрированными кислотами могут взаимодействовать различные металлы, такие как цинк, железо, алюминий, медь и т. д. Однако, не все металлы реагируют одинаково с разными кислотами, так как реакция может зависеть от конкретных условий и свойств металла.
Какие особенности имеют реакции металла с концентрированными кислотами?
При взаимодействии металла с концентрированными кислотами возможны различные реакции, включая выделение водорода, образование солей и выделение тепла. Реакция зависит от свойств кислоты, свойств металла, концентрации и температуры реагентов, а также других факторов. Некоторые металлы могут вступать в реакцию только с определенными кислотами, в то время как другие металлы могут реагировать со многими кислотами.
Что происходит при взаимодействии металла с концентрированными кислотами?
При взаимодействии металла с концентрированной кислотой происходит обмен ионами между металлом и кислотой, что приводит к образованию соответствующих солей. В большинстве случаев, при реакции с концентрированными кислотами, выделяется водород, который можно обнаружить по характерному "шипящему" звуку.
Какие реакции могут происходить при взаимодействии цинка с разными концентрированными кислотами?
Цинк может вступать в реакцию с разными концентрированными кислотами, образуя соответствующие соли и выделяя водород. Например, при реакции цинка с серной кислотой образуется сульфат цинка (ZnSO4) и выделяется водород. А при реакции цинка с хлороводородной кислотой образуется хлорид цинка (ZnCl2) и также выделяется водород.
