Металлы обладают особыми свойствами, которые позволяют им взаимодействовать с кислотами. Кислоты влияют на металлы, изменяя их химические свойства и структуру. Это позволяет провести ряд исследований и получить важные данные о взаимодействии металла с различными типами кислот.
Одной из основных характеристик этого взаимодействия является реакция металла с кислотой. Реакция может происходить с выделением газа (эффервесценция), с образованием соли и воды. Результаты таких реакций могут быть использованы в различных областях, таких как химия, металлургия и научные исследования.
Важно отметить, что взаимодействие металла с кислотой зависит от их свойств и химических структур. Некоторые металлы могут быть реактивными и быстро реагировать с кислотами, в то время как другие могут быть менее реактивными и требовать длительного времени для проявления реакции. При этом, взаимодействие может приводить к различным эффектам, включая образование осадка или изменение цвета.
Виды реакций металлов с кислотами

1. Водородное смещение
Водородное смещение — это реакция, при которой металл вытесняет водород из кислоты. Например, реакция цинка с соляной кислотой:
Zn (цинк) + 2HCl (соляная кислота) → ZnCl2 (хлорид цинка) + H2 (водород)
В результате реакции образуется хлорид цинка и выделяется водородный газ.
2. Формирование соли
При данной реакции металл взаимодействует с кислотой, формируя соль. Например, реакция железа с серной кислотой:
Fe (железо) + H2SO4 (серная кислота) → FeSO4 (сульфат железа) + H2 (водород)
Результатом реакции является образование сульфата железа и выделение водородного газа.
Взаимодействие металла с кислотой: изучение процесса

Взаимодействие металла с кислотой является одной из основных тем в изучении химии. Этот процесс является важным для понимания многих физических и химических свойств металлов и кислот.
Изучение взаимодействия металла с кислотой позволяет понять, какие реакции происходят на молекулярном и атомарном уровнях. Оно позволяет установить, какие ионы и соединения образуются в результате такого взаимодействия, а также выяснить условия и факторы, влияющие на скорость и характер реакции.
Часто изучение этого процесса проводится с использованием различных методов анализа и экспериментальных приборов. Например, можно провести опыт, в котором определится сила кислоты и ее влияние на реакцию с металлом. Также можно использовать спектральные методы анализа для изучения образовавшихся соединений и ионов.
Результаты изучения взаимодействия металла с кислотой имеют важное практическое значение. Они позволяют оптимизировать промышленные процессы, связанные с обработкой и очисткой металлов, а также разрабатывать новые материалы и сплавы с определенными свойствами. Кроме того, эти результаты применяются в медицине для создания лекарственных препаратов и диагностических средств.
Влияние металла на кислотную реакцию

Металлы играют важную роль в кислотных реакциях, влияя на их скорость и характер. Это связано с особенностями химических свойств металлов и их способностью реагировать с кислотами.
При взаимодействии металла с кислотой происходит выделение водорода и образование солей металлов. Металлы обладают высокой электроотрицательностью, поэтому они способны отдавать электроны в реакции с кислотой. В результате этой реакции металл окисляется, образуя положительные ионы, а кислота восстанавливается.
Реакция металла с кислотой вызывает образование соли и выделение водорода. Соли представляют собой соединения металлов и кислоты, их свойства определяются химическими свойствами обоих компонентов. Водород, выделяющийся при реакции, может возгоняться или образовывать газовые пузыри в жидкости.
Важно отметить, что способность металла реагировать с кислотой зависит от его активности. Некоторые металлы, такие как магний или цинк, активно реагируют с кислотами, образуя соли и выделяя водород. Другие металлы, такие как золото или платина, менее активны и могут не реагировать с кислотами в обычных условиях.
Исследование влияния металла на кислотную реакцию позволяет понять особенности химических свойств металлов и их реакций с другими веществами. Это знание имеет важное значение для различных промышленных процессов и научных исследований в области химии и материаловедения.
Физические изменения металла после контакта с кислотой
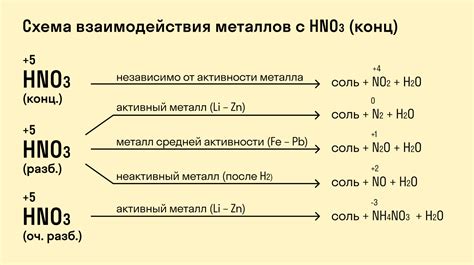
Контакт металла с кислотой вызывает серьезные физические изменения в его структуре и внешнем виде. Одним из наиболее ярких проявлений этого взаимодействия является коррозия. В результате реакции с кислотой на поверхности металла образуются окислы и гидроксиды, которые способны проникать в глубину металла и влиять на его прочность и стабильность.
В процессе взаимодействия с кислотой металл может испытывать различные эффекты: образование пузырьков, выделение газа, образование пятен, изменение цвета и текстуры поверхности. Например, при контакте железа с соляной кислотой образуется хлорид железа, который может приводить к образованию коричневых пятен на поверхности металла.
Кроме того, взаимодействие металла с кислотой может привести к его потемнению или появлению налета. Это связано с образованием оксидов или солей металла, которые могут изменять оптические свойства поверхности. Например, при действии соляной кислоты на медь может происходить образование зеленого налета, известного как патина.
Интенсивность физических изменений металла после контакта с кислотой зависит от различных факторов, таких как концентрация кислоты, продолжительность контакта и особенности металлического материала. Поэтому важно проводить эксперименты и изучать влияние различных факторов на характер взаимодействия металла с кислотой.
Химические свойства образовавшихся соединений
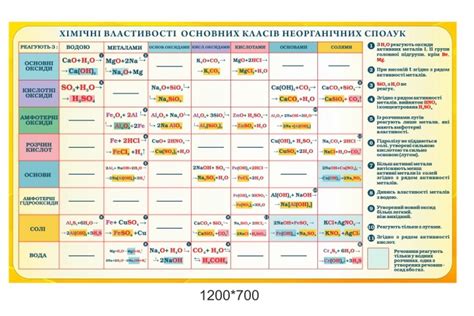
В результате взаимодействия металла с кислотой образуются различные соединения, которые обладают своими уникальными химическими свойствами.
Одним из таких соединений может быть соль, образованная ионами металла и анионами кислоты. Соли могут быть как растворимыми, так и нерастворимыми в воде. Растворимые соли образуют прозрачные растворы, а нерастворимые соли выпадают в осадок.
Помимо солей, при взаимодействии металла с кислотой могут образовываться и другие соединения, такие как газы или воды. Например, некоторые металлы, такие как цинк или алюминий, реагируют с кислородом из воды, образуя оксид металла и выделяя водородный газ.
Химические свойства образовавшихся соединений зависят от свойств металла и кислоты, используемых в реакции. Например, металлы различной активности могут реагировать с кислотами по-разному. Также различные кислоты могут образовывать разные типы соединений с металлами.
Изучение химических свойств образовавшихся соединений может помочь понять и прогнозировать результаты взаимодействия металла с кислотой, а также применять эти знания для различных химических и технологических процессов.
Влияние кислоты на структуру и свойства металла:

Взаимодействие металла с кислотой негативно отражается на его структуре и свойствах. Кислота обладает агрессивными свойствами и способна разрушать металлическую поверхность, приводя к ее коррозии и деформации.
Когда металл погружается в кислоту, происходит химическая реакция между активными частицами кислоты и металлической поверхностью. Результатом этой реакции является образование солей и газов, которые могут изменить структуру металла и его механические свойства.
Кислота может растворять металл, образуя коррозию. Растворение металла, особенно его поверхностных слоев, приводит к изменению геометрической формы и размеров металлической детали. Это может сказаться на ее функциональности и безопасности.
Важно отметить, что различные металлы реагируют по-разному на кислоты. Некоторым металлам удается образовать защитную пленку, которая препятствует дальнейшей коррозии, в то время как другие металлы могут быть более подвержены разрушению.
- Распространенные металлы, такие как железо или алюминий, подвержены коррозии в кислотных средах.
- Некоторые специальные металлы, например, нержавеющая сталь, благодаря наличию хрома в своем составе, обладают более высокой устойчивостью к кислотному воздействию.
Изучение влияния кислоты на металл имеет большое практическое значение, так как позволяет разработать специальные покрытия и составы для защиты металла от коррозии и сохранения его механических свойств.
Возможные последствия взаимодействия металла с кислотой

1. Коррозия и разрушение поверхности металла. Взаимодействие металла с кислотой может привести к образованию коррозионных реакций, которые вызывают разрушение металлической поверхности. Коррозия может привести к образованию пузырьков, трещин и отслаивания поверхностных слоев металла.
2. Выделение вредных газов или паров. В реакции металла с кислотой может образоваться вредный газ или пар, который негативно влияет на окружающую среду и здоровье человека. Например, взаимодействие цинка с соляной кислотой приводит к образованию хлорида цинка и выделению хлороводородного газа.
3. Изменение физических свойств металла. Взаимодействие металла с кислотой может привести к изменению его физических свойств. Например, металл может стать более хрупким или менять цвет из-за образования оксидных или солевых соединений.
4. Потеря металлом своих свойств и структуры. Взаимодействие металла с кислотой может привести к потере металлом его свойств и структуры. Например, алюминий при взаимодействии с азотной кислотой может образовать нитрид алюминия, что может привести к потере его химической активности и способности вступать в реакции.
5. Возможность возникновения взрыва. В некоторых случаях взаимодействие металла с кислотой может привести к образованию взрывоопасных смесей. Например, взаимодействие меди с азотной кислотой может привести к образованию взрывчатого соединения - нитрата меди.
Методы защиты металла от воздействия кислоты

Кислоты могут негативно влиять на металлы, вызывая их ржавление и разрушение. Чтобы предотвратить это, применяют различные методы защиты металла от воздействия кислоты.
1. Покрытия металла: Один из самых распространенных способов защиты металла - это нанесение на его поверхность покрытий, которые создают защитный слой. Например, покрытия из цинка (гальваническое покрытие) или эпоксидные краски. Эти покрытия предотвращают проникновение кислоты на поверхность металла, защищая его от коррозии.
2. Избегание контакта с кислотой: Другой способ защиты металла - предотвращение его контакта с кислотой. Например, можно использовать не-металлические материалы вместо металлических, если они не подвергаются коррозии от кислоты. Также можно разместить металлические конструкции на безопасном расстоянии от источника кислоты.
3. Установка анодов: Этот метод используется в гальванической защите. Защищаемый металл становится катодом, а другой металл, анодом. При попадании кислоты на металл, анод теряет свойство быть анодом и не подвергается разрушению. Таким образом, металл, который нужно защитить, остается неповрежденным.
4. Использование коррозионностойких сплавов: В некоторых случаях можно использовать специальные сплавы, которые обладают повышенной устойчивостью к коррозии от кислот. Эти сплавы состоят из основного металла и добавки, которая способствует образованию защитной пленки на поверхности металла.
Практическое применение взаимодействия металла с кислотой
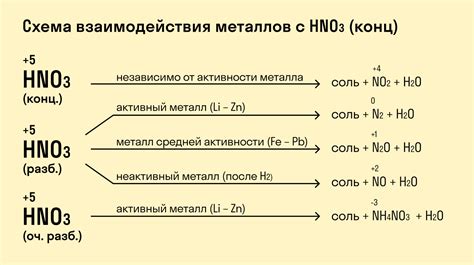
Взаимодействие металла с кислотой имеет широкое практическое применение в различных областях, таких как промышленность, наука и медицина.
Одним из основных применений этого процесса является получение водорода. Путем обработки металла кислотой, особенно соляной, можно получить водород, который затем может быть использован в таких сферах, как производство аммиака, синтез органических соединений или водородной энергетике. Возможность получения водорода из взаимодействия металла с кислотой является довольно дешевым и эффективным способом его производства.
Взаимодействие металла с кислотой также имеет применение в гальванических элементах. Когда металл погружается в раствор кислоты, происходит окислительно-восстановительная реакция, в результате которой возникает электрический ток. Это основа работы гальванических элементов, которые являются источником энергии для множества устройств, включая аккумуляторы, электролизеры и другие.
Удаление оксида металла с поверхности изделий также является одним из практических применений взаимодействия металла с кислотой. Кислота способна растворять оксидные пленки, что позволяет очищать металлические поверхности от нежелательных отложений. Это особенно важно в металлургической и машиностроительной отраслях, где необходимо обеспечить чистоту и гладкость поверхностей для дальнейшей обработки и соединения деталей.
Таким образом, взаимодействие металла с кислотой находит широкое применение в различных сферах, от производства водорода до очистки поверхностей от оксидов. Это позволяет эффективно использовать металл и его свойства в разных областях человеческой деятельности.
Вопрос-ответ

Как происходит взаимодействие металлов с кислотой?
Взаимодействие металлов с кислотой происходит путем реакции металла с ионами водорода в кислоте. Металл выделяет электроны и образует положительные ионы, а ионы водорода в кислоте получают эти электроны и образуют молекулярный водород.
Какие металлы реагируют с кислотами?
Реакция металлов с кислотами зависит от активности металла и типа кислоты. Некоторые металлы, такие как натрий и калий, реагируют с кислотами очень быстро, выделяя водород. Другие металлы, такие как ртуть и золото, вообще не реагируют с кислотами.
Какие газы образуются при взаимодействии металлов с кислотой?
При взаимодействии металлов с кислотой образуется газ водород (H2), который выделяется в виде пузырьков. Это происходит из-за того, что металл отдает электроны, а ионы водорода в кислоте получают эти электроны и образуют молекулярный водород.
Какова роль кислоты в реакции с металлом?
Кислота играет роль активатора реакции. Она образует ионы водорода, которые получают электроны от металла. Эти электроны помогают металлу окислиться и образовать положительные ионы.
Какие свойства металла влияют на его реакцию с кислотой?
Активность металла является главным фактором, влияющим на его реакцию с кислотой. Более активные металлы, такие как натрий и калий, реагируют с кислотами быстрее и интенсивнее. Также важными свойствами металла являются его структура, поверхность и наличие оксидной пленки на поверхности.
