Цинк - один из самых распространенных элементов в природе, который широко используется в различных отраслях науки и промышленности благодаря своим особым химическим свойствам. Одним из наиболее интересных и важных аспектов, связанных с цинком, является его взаимодействие с кислотами.
Кислоты - это вещества, которые способны отдавать водородные ионы (протоны) в раствор. В то время как цинк, являясь металлом, не может напрямую реагировать с кислотами, он может вступать в реакцию с некоторыми связанными с ними группами, образуя различные соединения.
Одним из наиболее известных примеров взаимодействия цинка с кислотами является его реакция с соляной кислотой. В результате этой реакции образуется хлорид цинка, который имеет широкое применение в различных областях, включая гальванику, производство лекарств, производство пластмассы и другие.
Цинк также может реагировать с другими кислотами, такими как серная кислота и азотная кислота. В экспериментах было показано, что эти реакции могут быть использованы для получения различных соединений цинка, которые имеют важное значение в промышленности и научных исследованиях.
Взаимодействие цинка с кислотами является одной из основных тем изучения в химии. Оно позволяет ученым понять особенности реакций между металлами и кислотами, а также разрабатывать новые способы синтеза и получения соединений с использованием цинка. Кроме того, понимание этого взаимодействия помогает оптимизировать процессы производства и повышать эффективность использования цинка в различных областях применения.
Химическое взаимодействие цинка с кислотами

Цинк является одним из наиболее активных металлов и реагирует с различными кислотами, образуя соли и выделяя водород. Одной из наиболее распространенных реакций цинка с кислотами является его взаимодействие с соляной кислотой (HCl). При этом образуется хлорид цинка (ZnCl2) и выделяется водород (H2). Эта реакция может быть использована для получения хлорида цинка, который широко применяется в различных отраслях промышленности.
Кроме соляной кислоты, цинк также реагирует с азотной кислотой (HNO3), образуя нитрат цинка (Zn(NO3)2) и выделяя водород. Эта реакция может быть использована для получения нитрата цинка, который применяется в производстве удобрений, пигментов, взрывчатых веществ и других продуктов химической промышленности.
Взаимодействие цинка с уксусной кислотой (CH3COOH) приводит к образованию ацетата цинка (Zn(CH3COO)2) и выделению водорода. Ацетат цинка используется в фотографии, в производстве лаков, покрытий и других химических продуктов.
Химическое взаимодействие цинка с кислотами может быть описано следующей реакцией: Zn + 2HCl → ZnCl2 + H2. Эта реакция является типичным примером реакции замещения одного металла другим. Она основана на том, что цинк является более активным металлом, чем водород, и может вытеснить его из кислотного раствора.
Основы химического взаимодействия

Химическое взаимодействие - это процесс взаимодействия веществ, при котором происходят изменения их состава и структуры. Одним из примеров химического взаимодействия является взаимодействие цинка с кислотами.
Цинк относится к активным металлам и обладает способностью реагировать с различными кислотами. Кислоты, в свою очередь, представляют собой соединения, способные выделять протоны (H+) при реакции с другими веществами.
Взаимодействие цинка с кислотами основано на образовании солей цинка и соответствующих кислот. При этом происходит обмен ионов, в результате которого цинк замещает металлы или водород в структуре кислоты.
Химическое взаимодействие цинка с кислотами широко используется в различных областях. Например, в медицине цинк используется как компонент витаминов и препаратов для лечения различных заболеваний. Кроме того, цинковые соединения активно применяются в промышленности, в том числе в производстве батареек, лакокрасочных материалов и электронных компонентов.
- Цинковая кислота (H2ZnO3) является одним из примеров вещества, получаемого при химическом взаимодействии цинка с кислотами.
- Взаимодействие цинка с серной кислотой (H2SO4) приводит к образованию сульфата цинка (ZnSO4) и выделению газа - водорода.
Таким образом, химическое взаимодействие цинка с кислотами является важным процессом, который находит применение как в научных исследованиях, так и в повседневной жизни человека.
Применение цинка в реакциях с кислотами
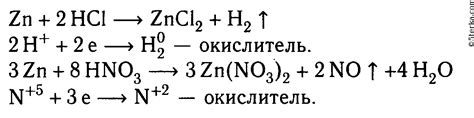
Цинк, являясь активным металлом, образует реакции с различными кислотами, что делает его полезным во многих областях жизни и промышленности.
Цинк имеет способность активно взаимодействовать с сильными кислотами, такими как соляная кислота (HCl), серная кислота (H2SO4) и азотная кислота (HNO3). В результате реакции соляной кислоты, образуется хлорид цинка (ZnCl2), особо важный промышленный продукт, который используется в качестве катализатора и в производстве других химических соединений.
Цинк также взаимодействует с серной кислотой, образуя сульфат цинка (ZnSO4). Это соединение широко используется в агрокультуре как удобрение и для производства керамических и стеклянных изделий.
Реакция цинка с азотной кислотой приводит к образованию нитрата цинка (Zn(NO3)2). Нитрат цинка используется в фотографии, в производстве огнепрочных материалов и в электротехнике.
Вопрос-ответ

Какие кислоты реагируют с цинком?
Цинк может реагировать с различными кислотами, в том числе с соляной, серной и уксусной кислотами.
Какое значение имеет химическое взаимодействие цинка с кислотами?
Химическое взаимодействие цинка с кислотами имеет большое значение в химической промышленности и лабораторных исследованиях. Оно применяется для получения соединений цинка, водорода и других продуктов реакции.
