Взаимодействие кислот и металлов является одной из основных реакций в химии. Кислоты обладают способностью выделять положительно заряженные ионы (катионы) в растворе, а металлы, в свою очередь, способны отдавать эти ионы. В результате такого взаимодействия образуются соли, которые являются основными химическими соединениями металлов с кислотами.
Соли, образующиеся при взаимодействии кислот и металлов, имеют разнообразное применение. Они широко используются в промышленности, медицине, сельском хозяйстве и других отраслях. Соли могут быть как растворимыми в воде, так и нерастворимыми. Растворимость солей зависит от их химического состава и структуры, а также условий окружающей среды.
Взаимодействие кислот с металлами имеет ряд особенностей. Некоторые металлы, такие как цинк, магний и алюминий, способны реагировать с кислотами с выделением водорода. Другие металлы, например, железо или медь, реагируют с кислотами с образованием соответствующих солей и выделением газов.
Реакция кислот с металлами

Кислоты – это химические соединения, которые могут реагировать с различными веществами. Одним из веществ, с которыми кислоты взаимодействуют, являются металлы. Реакция кислот с металлами приводит к образованию солей.
Во время реакции между кислотой и металлом происходит обмен ионами. Кислота отдает ионы водорода (H+), а металл отдает свои положительные ионы. Образованные ионы вступают в реакцию и образуют соль. Реакция кислот с металлами может быть представлена в виде химического уравнения.
Соли, образующиеся в результате реакции кислот с металлами, имеют особое название – металлосоли. Они обладают характерными свойствами и широко применяются в различных отраслях промышленности и научных исследованиях.
Реакция кислот с металлами может протекать с выделением газа – это наблюдается, например, при реакции кислоты с цинком или алюминием. Выделение газа является одним из признаков такой химической реакции.
Также, реакция кислот с металлами может протекать с выделением тепла. Это наблюдается, например, при реакции кислоты с железом. При этом реакции тепло выделяется в виде теплоты и света.
Реакция кислот с металлами широко изучается в химии и имеет практическое значение. Изучение этой реакции позволяет не только понять принципы взаимодействия кислот и металлов, но и применять эти знания в различных областях науки и производства.
Взаимодействие кислот и металлов

Взаимодействие кислот и металлов является одним из основных процессов в химии. Оно происходит при соприкосновении металла с кислотой, что приводит к образованию солей и выделению водорода.
Кислоты могут быть различного вида – органические и неорганические. Большинство неорганических кислот содержат водород, который обладает свойством выступать в реакциях со многими металлами. Органические кислоты, в свою очередь, обычно содержат кислород и водород, и они также могут способствовать взаимодействию с металлами.
Взаимодействие кислот и металлов происходит в результате окислительно-восстановительных реакций. Когда кислота вступает в реакцию с металлом, происходит передача электронов, что приводит к окислению металла и одновременному восстановлению кислоты.
Результатом реакции взаимодействия кислот и металлов являются соли. Это химические соединения, образуемые в результате обменной реакции между атомами металла и группами кислоты. Соли обладают разнообразными свойствами и широко используются в различных сферах нашей жизни.
При взаимодействии кислот и металлов также выделяется водород. Образование водорода может быть заметно по появлению пузырьков газа или по характеристическому шипящему звуку. Это явление часто используется для определения активности металла – чем активнее металл, тем больше водорода будет выделяться при взаимодействии.
Формирование солей при взаимодействии кислот и металлов
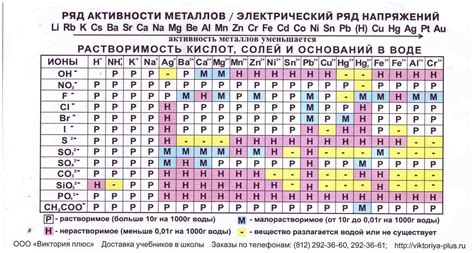
Соли — это химические соединения, образующиеся при реакции взаимодействия металлов с кислотами. Одной из основных характеристик солей является их кристаллическая структура, которая обеспечивает устойчивость вещества и его растворимость.
Взаимодействие кислот и металлов происходит в результате перехода электрона от металла к кислоте. Как правило, это происходит на поверхности металла, где происходит окислительно-восстановительная реакция. В результате этого процесса образуется ионная соль.
Реакция взаимодействия кислот и металлов может протекать различными путями, в зависимости от свойств металла и кислоты. Например, реакция с образованием растворимой соли может быть экзотермической, при этом выделяется тепло. Также возможно образование нерастворимых солей, которые образуют осадок в виде мелких кристаллов.
Чтобы ускорить реакцию образования солей, можно использовать катализаторы или повысить температуру. В результате взаимодействия кислот и металлов образуется ряд различных солей с различными свойствами. Некоторые из них могут иметь широкое применение в промышленности и научных исследованиях.
Формирование солей при взаимодействии кислот и металлов является важным процессом в химии. Оно не только позволяет получать новые вещества, но и имеет большое значение для понимания основных законов химических реакций. Поэтому изучение этого процесса является неотъемлемой частью образования в области химии.
Химические и физические свойства полученных солей
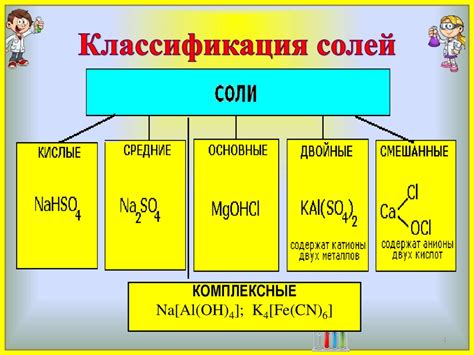
Соли, полученные в результате взаимодействия кислот и металлов, обладают рядом химических и физических свойств, которые определяют их уникальные характеристики.
Химические свойства:
- Соли обладают электрохимической активностью и могут взаимодействовать с другими химическими веществами, образуя новые соединения. Это позволяет использовать их в различных химических реакциях и синтезе других соединений.
- Соли могут образовывать кристаллическую структуру, что определяет их форму и регулярность внутреннего строения. Благодаря этому свойству, соли широко применяются в качестве катализаторов и в процессах кристаллизации различных веществ.
- Соли обладают способностью образовывать ионы при диссоциации в растворах. Это свойство позволяет использовать соли как электролиты в электрохимических процессах и в медицине для восстановления электролитического баланса организма.
Физические свойства:
- Соли обладают кристаллической структурой, что делает их твердыми и хрупкими веществами с высокой температурой плавления. Это позволяет использовать их в качестве подложек и носителей для различных химических реакций.
- Соли имеют разные цвета, которые связаны с присутствием различных ионов в их составе. Например, соли меди могут иметь зеленый или синий цвет, а соли железа - красный или желтый.
- Соли обладают определенным степенями растворимости в воде, что может влиять на их использование в различных областях. Некоторые соли легко растворяются, а другие - практически не растворяются, что делает их ценными веществами в промышленности и научных исследованиях.
Практическое применение солей, образующихся из кислот и металлов
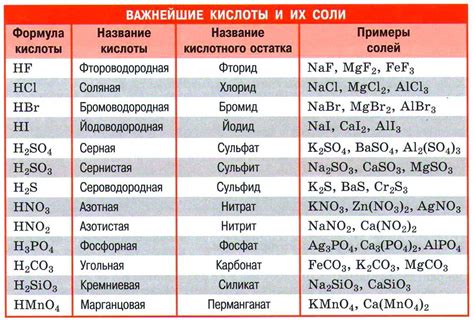
Образование солей при реакции кислоты и металла имеет множество практических применений в разных сферах нашей жизни.
В медицине соли кислот и металлов используются для производства лекарственных препаратов. Например, магния соль может применяться для восстановления нормального уровня магния в организме, что помогает укрепить зубы и кости. Калия соли могут использоваться для улучшения функции сердца и нормализации работы нервной системы.
В пищевой промышленности соли, образующиеся при реакции кислот и металлов, используются как добавки для придания пищевым продуктам специфического вкуса и аромата. Например, натрия соли применяются для приготовления хлеба, мороженого и различных соусов. Кальция соли добавляются в пищевые продукты для укрепления зубов и костей.
В промышленности соли кислот и металлов используются в процессе производства различных материалов. Например, алюминия соль применяется для получения алюминия, который используется в автомобильной и строительной промышленности. Железа соль любое знаменита в качестве катализатора в процессе производства пластика и резины.
В искусстве соли, образующиеся в результате соединения кислот и металлов, также имеют свое исключение. Например, меди соли используются для создания желтых, оранжевых и красных красителей. Ртути соль применяется для производства термометров.
Вопрос-ответ

Какие вещества реагируют с кислотами?
С кислотами реагируют различные вещества, в том числе металлы, оксиды, гидроксиды и соли.
Что происходит при реакции металла с кислотой?
При реакции металла с кислотой происходит образование соли и выделение водорода.
Какие кислоты образуют соли?
Все кислоты образуют соли. Например, соляная кислота образует хлориды металлов, серная кислота - сульфаты, азотная кислота - нитраты и т.д.
Можно ли получить соль при реакции кислоты с неметаллом?
Да, при реакции кислоты с неметаллом также образуется соль. Например, при реакции серной кислоты с сероводородом образуется сероводородная соль.
Каким образом происходит реакция образования соли между кислотой и металлом?
Реакция образования соли между кислотой и металлом происходит следующим образом: металл диссоциирует под действием кислоты, образуя положительные ионы металла, а кислота диссоциирует, образуя положительные ионы водорода. Затем положительные ионы металла и положительные ионы водорода образуют соль, а отрицательные ионы кислоты соединяются вместе, образуя воду.
