Кислоты и металлы являются двумя основными классами химических веществ, которые проявляют различные свойства и взаимодействуют между собой. Однако, существуют также металлы, которые могут проявлять амфотерные свойства и реагировать как с кислотами, так и с щелочами. Такое взаимодействие имеет свои особенности и может быть использовано в различных областях науки и промышленности.
Амфотерные металлы представляют собой специфический класс химических элементов, которые способны образовывать ионы с различной зарядностью в зависимости от окружающей среды. Они обладают особой реакционной способностью, которая позволяет им взаимодействовать как с протонами, так и с гидроксид-ионами. Эти металлы включают в себя такие элементы, как алюминий, цинк, свинец, железо и др.
Взаимодействие кислот с амфотерными металлами происходит в результате образования сложных структур, которые состоят из ионов металла и анионов кислоты. Однако, данная реакция может быть как обратимой, так и необратимой в зависимости от реагентов и условий проведения. Важной особенностью этого взаимодействия является возможность образования инорганических соединений с данными металлами, которые обладают важными физическими и химическими свойствами.
Кислоты и их взаимодействие
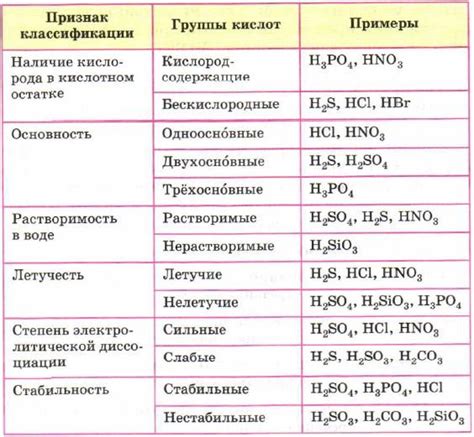
Кислоты — это химические вещества, которые обладают свойством отдавать протоны (водородные ионы) и образовывать положительные ионы при диссоциации в воде. Кислоты могут быть однократно или многократно замещенными органическими или неорганическими группами, что влияет на их силу и химические свойства. Взаимодействие кислот с другими веществами может привести к образованию солей и новых химических соединений.
Взаимодействие кислот с амфотерными металлами является одним из важных аспектов химии. Амфотерные металлы могут проявлять свойства кислоты или щелочи в зависимости от условий реакции. Такое поведение обусловлено наличием свободных электронов и возможностью образования координационных связей.
Взаимодействие кислот с амфотерными металлами имеет широкое применение в различных отраслях науки и промышленности. Например, такие реакции используются в процессе производства лекарственных препаратов, катализаторов, электролитов для аккумуляторов и других химических соединений. Это позволяет получать новые вещества с определенными свойствами и обеспечивать эффективность процессов, в которых они используются.
Амфотерные металлы: определение и примеры

Амфотерные металлы - это класс химических элементов, которые могут реагировать как с кислотами, так и с основаниями. Они обладают способностью изменять свою валентность и формировать различные ионы в растворах.
Примерами амфотерных металлов являются алюминий (Al), цинк (Zn), железо (Fe), свинец (Pb), олово (Sn), кадмий (Cd) и другие. Все эти металлы имеют способность взаимодействовать с кислотами и основаниями в соответствии со своей валентностью и электрохимическим свойствам.
Например, алюминий (Al) может реагировать с кислотами, образуя соли алюминия, такие как алюминиевый карбонат, алюминиевая сульфат или алюминиевая нитрат. В то же время алюминий может быть растворим в щелочных растворах, образуя гидроксид алюминия.
Особенностью амфотерных металлов является их способность образовывать комплексные соединения с различными лигандами, такими как аммиак, гидроксиды или фториды. Это делает их весьма востребованными в различных областях, включая производство лекарственных препаратов, катализаторов, пигментов и других химических веществ.
Основные свойства кислот и амфотерных металлов
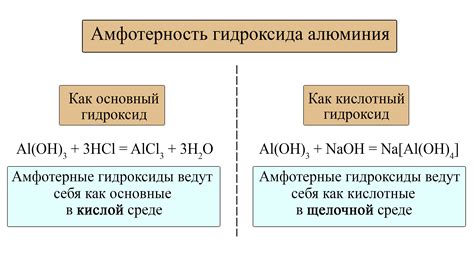
Кислоты - это химические соединения, которые обладают способностью выделять положительные ионы водорода (H+) в растворе. Кислоты могут быть органическими или неорганическими. Органические кислоты обычно содержат карбоксильные группы (-COOH), а неорганические кислоты могут содержать анионы, такие как сероводород (HS-) или азотная кислота (HNO3).
Амфотерные металлы - это металлы, которые могут проявлять свойства как кислоты, так и основания. То есть, они способны как отдавать, так и принимать ионы водорода в реакции. Примерами амфотерных металлов являются алюминий (Al), цинк (Zn) и железо (Fe).
Кислоты обладают рядом характерных свойств:
- Кислоты имеют кислый вкус и способны вызывать жжение на коже.
- Они обладают способностью растворять металлы и реагировать с основаниями, образуя соль и воду.
- Кислоты могут изменять цветы индикаторных веществ, изменяя кислотно-щелочной баланс в растворе.
- Они могут иметь различную силу и концентрацию, что определяет их реакционную активность.
Амфотерные металлы способны проявлять свойства и как кислоты, и как основания, благодаря следующим свойствам:
- Амфотерные металлы могут быть растворены как в кислотном, так и в щелочном растворе.
- Они способны образовывать соли с кислотами и основаниями.
- Амфотерные металлы могут образовывать комплексные соединения с различными лигандами.
- Эти металлы могут действовать как катализаторы в различных химических реакциях.
Основные свойства кислот и амфотерных металлов определяют их способность взаимодействия друг с другом и с другими веществами, что находит применение в различных областях химии, в том числе в химической промышленности, медицине и исследованиях.
Реакция кислот с амфотерными металлами

Амфотерные металлы – это металлы, которые способны взаимодействовать как с кислотами, так и с основаниями. Реакция кислот с амфотерными металлами имеет свои особенности и широкое применение в различных областях.
Взаимодействие кислот с амфотерными металлами основано на образовании солей и воды. При контакте кислоты с амфотерным металлом происходит образование соответствующего солевого соединения и выделение воды. Это свойство металлов позволяет им реагировать как с кислотами, так и с основаниями.
Применение реакции кислот с амфотерными металлами очень разнообразно. Одним из наиболее известных применений является процесс нейтрализации. Кислота растворяется в воде и образует протон, который взаимодействует с амфотерным металлом, образуя соль.
Кроме того, реакция кислот с амфотерными металлами применяется в процессе восстановления окислителей и получения различных соединений. Многие из этих соединений имеют важное значение в промышленности и научных исследованиях.
Стоит отметить, что силу реакции кислоты с амфотерным металлом можно оценить по реакционной способности кислоты и его амфотерного окислительного потенциала. Чем больше реакционная способность кислоты и амфотерный окислительный потенциал металла, тем интенсивнее будет идти реакция.
Применение в практике и науке
Взаимодействие кислот с амфотерными металлами имеет широкое применение как в практике, так и в науке. С одной стороны, оно используется в различных производствах для получения необходимых продуктов и материалов. Например, реакция кислоты с амфотерными металлами может привести к образованию соединений с определенными свойствами, такими как прочность, электропроводность или магнитные свойства. Это позволяет создавать новые материалы с улучшенными характеристиками, которые могут быть применены в различных отраслях промышленности.
С другой стороны, изучение взаимодействия кислот с амфотерными металлами имеет большое значение в химической науке. Это позволяет расширить наши знания о взаимодействии различных веществ и помогает в поиске новых реакций и соединений. Исследования в этой области могут привести к открытию новых методов синтеза, оптимизации процессов и развитию новых технологий. Кроме того, изучение взаимодействия кислот с амфотерными металлами помогает лучше понять и предсказывать свойства и поведение других химических систем.
Применение взаимодействия кислот с амфотерными металлами также находит свое применение в аналитической химии. Оно может быть использовано для определения концентрации кислоты или металла в растворе. Например, с помощью соответствующих реакций можно провести титрование, позволяющее определить точную концентрацию кислоты. Это важный метод анализа, который находит применение в различных областях, таких как фармацевтика, пищевая промышленность, экология и т.д.
Таким образом, взаимодействие кислот с амфотерными металлами играет важную роль и имеет широкий спектр применения как в практике, так и в науке. Оно позволяет получать новые материалы с улучшенными свойствами, расширить наши знания о химических реакциях и развить новые методы анализа. Это открывает новые перспективы для применения в различных отраслях и помогает совершенствовать наши сознания о мире химии.
Амфотерные металлы в промышленности
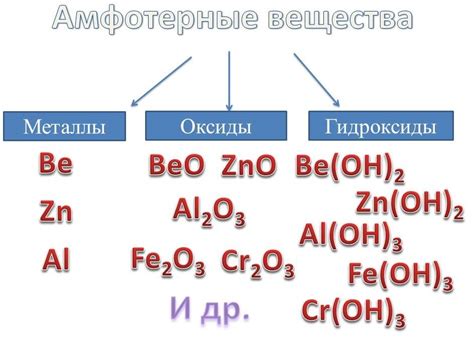
Амфотерные металлы, такие как алюминий, цинк и олово, играют важную роль в промышленности благодаря своей универсальности и свойству взаимодействовать как с кислотами, так и с основаниями.
Алюминий, являясь одним из самых распространенных амфотерных металлов, широко используется в различных сферах промышленности. Он применяется для производства автомобилей, самолетов и поездов, так как обладает легкостью и прочностью. Алюминиевые сплавы также находят применение в строительстве, судостроении и производстве упаковочных материалов.
Цинк играет важную роль в гальванической и электротехнической промышленности. Он используется для покрытия металлических поверхностей, чтобы защитить их от коррозии. Также цинк применяется в производстве батареек, аккумуляторов, электроники и солнечных панелей.
Олово, благодаря своей высокой плавкости и устойчивости к коррозии, находит применение в производстве различных товаров, включая пищевую упаковку, консервные банки, санитарно-техническое оборудование и элементы электрических цепей.
Амфотерные металлы являются важными составляющими промышленности благодаря своим свойствам и широкому спектру применения. Они используются в производстве различных продуктов и материалов, обеспечивая прочность, защиту от коррозии и электропроводность.
Использование кислот и амфотерных металлов в химических исследованиях
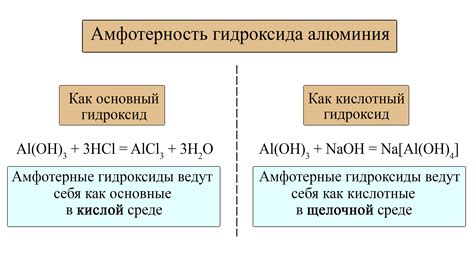
Кислоты и амфотерные металлы играют важную роль в химических исследованиях, так как обладают разнообразными свойствами и применяются в различных областях науки и технологии.
Кислоты являются ключевыми компонентами в химической аналитике. Они используются для определения концентрации веществ в растворе, выявления наличия определенных элементов и соединений. Кроме того, кислоты используются в процессе обработки образцов и исследования их химического состава.
Амфотерные металлы - это металлы, способные проявлять свойства как кислот, так и щелочей. Эти металлы широко применяются в качестве катализаторов в химических реакциях. Они обладают уникальными свойствами, такими как способность взаимодействовать с различными соединениями и увеличивать скорость химических реакций.
В химических исследованиях кислоты и амфотерные металлы используются для синтеза новых соединений, получения материалов с определенными свойствами, а также для изучения различных химических процессов. Например, амфотерные металлы могут использоваться в качестве электродов в электрохимических исследованиях, а кислоты - для проведения титрования и определения pH растворов.
Таким образом, использование кислот и амфотерных металлов в химических исследованиях позволяет расширить наши знания о свойствах веществ, проводить анализ химических реакций и создавать новые материалы с определенными свойствами. Это является важным шагом в развитии науки и технологий, а также применения химии в различных отраслях промышленности.
Вопрос-ответ

Какие металлы считаются амфотерными?
Амфотерными металлами считаются алюминий, цинк, свинец, медь.
Какие особенности взаимодействия кислот с амфотерными металлами?
Особенностью является то, что амфотерные металлы могут реагировать как с кислотами, так и с щелочами.
