В мире существует бесконечное множество веществ, каждое из которых состоит из атомов. Атомы двух разных элементов могут взаимодействовать, образуя новые соединения. Особенно интересно взаимодействие атомов металлов с атомами неметаллов.
Металлы и неметаллы обладают разными свойствами и структурой атома. Металлы, как правило, обладают положительно заряженными ионами, а неметаллы - отрицательно заряженными ионами. Взаимодействие атомов металлов с атомами неметаллов основано на том, что атомы металлов отдают свои электроны атомам неметаллов, образуя ионные соединения.
В процессе взаимодействия между атомами металлов и атомами неметаллов происходит передача электронов. Атомы металлов отдают свои электроны атомам неметаллов, чтобы достичь стабильной конфигурации электронных оболочек. В результате этого образуются ионные соединения, в которых металлы образуют положительные ионы, а неметаллы образуют отрицательные ионы. Ионные соединения обладают особыми свойствами, например, высокой температурой плавления и кристаллической структурой.
Реакция металлов с неметаллами: основное взаимодействие

Реакция металлов с неметаллами представляет собой процесс, при котором металлы и неметаллы образуют соединения, называемые соединениями между ними. Это взаимодействие определяется электрохимическими свойствами металлов и неметаллов.
Основное взаимодействие металлов с неметаллами заключается в передаче электронов от металла к неметаллу. Металлы обладают свободными электронами на своей внешней оболочке, которые они легко могут отдать. Неметаллы, в свою очередь, имеют недостаток электронов на своей внешней оболочке и готовы их принять.
В процессе реакции металлы окисляются, передавая электроны на внешнюю оболочку неметалла, который в свою очередь восстанавливается. Таким образом, образуются ионные соединения между металлом и неметаллом.
Примером реакции металла с неметаллом является образование хлорида натрия (NaCl) при взаимодействии натрия (Na) с хлором (Cl). В ходе реакции натрий отдает один электрон хлору, который принимает его, образуя ион натрия (Na+) и ион хлорида (Cl-).
Химический процесс образования соединений

Химическое взаимодействие между атомами металлов и неметаллами приводит к образованию соединений. Этот процесс основывается на передаче или совместном использовании электронов между атомами.
При взаимодействии атомов металлов с неметаллами происходит образование ионов. Металлы, как правило, отдают электроны и образуют положительно заряженные ионы – катионы. Неметаллы, напротив, принимают электроны и образуют отрицательно заряженные ионы – анионы.
Образование соединений между металлами и неметаллами происходит на основе принципа электронной конфигурации. Металлы, отдавая электроны, достигают стабильной конфигурации с октетом электронов во внешней оболочке. Неметаллы, принимая электроны, также стараются достичь октета во внешней оболочке.
Химический процесс образования соединений между атомами металлов и неметаллами может быть представлен с помощью химических формул. В формулах соединений указываются символы элементов и их соотношение. Например, оксид железа Fe2O3 представляет собой соединение между железом (Fe) и кислородом (O) в отношении 2 к 3.
Образование соединений между атомами металлов и неметаллами является основой для понимания многих химических реакций и процессов, влияющих на свойства и применение материалов. Это важное явление, которое тесно связано с различными областями химии и материаловедения.
Передача электронов и ионный обмен
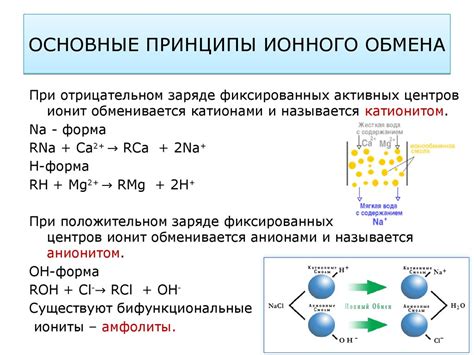
Взаимодействие атомов металлов с неметаллами может происходить через передачу электронов или ионный обмен. При передаче электронов, атом металла отдает один или несколько электронов атому неметалла, образуя положительный и отрицательный ионы соответственно. Это происходит из-за различия в электроотрицательностях металла и неметалла.
Передача электронов может приводить к образованию ионов, простейшим примером является образование ионов натрия и хлора при взаимодействии атомов натрия и хлора: натрий отдает один электрон хлору, в результате чего получается положительный ион натрия Na+ и отрицательный ион хлора Cl-. Это позволяет обоим атомам достичь электронной конфигурации инертного газа.
Ионный обмен — это процесс, в котором атомы металла и неметалла обменяются ионами. Например, взаимодействие атомов меди и серы приводит к образованию ионов меди(II) и ионов серы(II). В этом случае ионы меди(II) образуют положительные ионы Cu2+, а ионы серы(II) образуют отрицательные ионы S2-. Этот процесс обеспечивает установление равновесия между ионами металла и неметалла.
Роль атомов металлов и неметаллов в реакции

Атомы металлов играют важнейшую роль в реакциях с неметаллами, так как они являются источником электронов. Металлы могут отдавать электроны из своей внешней электронной оболочки, образуя катионы. Такие катионы потом взаимодействуют с атомами неметаллов, которые стремятся принять эти электроны.
Атомы неметаллов в реакции с металлами играют роль акцепторов электронов. Они стремятся получить дополнительные электроны для заполнения своей внешней электронной оболочки и образования отрицательного заряда. Это дает возможность атомам металлов отдать свои электроны и образовать положительный заряд в виде катиона.
Реакции между атомами металлов и неметаллами могут протекать различными способами в зависимости от их свойств и энергетических характеристик. В некоторых случаях происходит простой обмен электронами, в других - образование ионных связей или сопряжение атомов в ковалентные связи.
При взаимодействии металлов и неметаллов образуются различные химические соединения, такие как соли, оксиды, гидроксиды, аммиак и другие. Эти соединения имеют различные физические и химические свойства и находят широкое применение в различных отраслях промышленности и научных исследованиях.
Формирование связей и образование кристаллической структуры

Взаимодействие атомов металлов с неметаллами ведет к образованию химических связей, которые определяют кристаллическую структуру материала.
Одним из основных типов связей, образующихся между атомами металлов и неметаллов, является ионная связь. При этом металлы отдают электроны и образуют положительно заряженные ионы (катионы), а неметаллы принимают эти электроны и образуют отрицательно заряженные ионы (анионы). В результате образуются кристаллические соединения, состоящие из положительно и отрицательно заряженных ионов, притягивающихся друг к другу силой электростатического взаимодействия.
Кристаллическая структура таких соединений может быть описана с помощью решетки, в которой каждый ион занимает определенное положение и имеет своих соседей. Расположение ионов в решетке определяется их размерами, зарядом и координационным окружением - количество и тип атомов, окружающих каждый ион.
Помимо ионной связи, металлы и неметаллы могут образовывать и другие типы связей, например, ковалентные или металлические связи. Ковалентная связь возникает при обмене электронами между атомами, а металлическая связь - при образовании электронного газа, состоящего из свободно движущихся электронов и положительных ионов металла.
Таким образом, взаимодействие атомов металлов с неметаллами приводит к образованию различных типов химических связей и формированию кристаллической структуры материала. Знание этих процессов позволяет понять свойства и поведение различных соединений и применять их в разных областях, включая металлургию, электронику и материаловедение.
Влияние валентности элементов на тип соединения

Валентность элементов влияет на тип соединения, которое образуется между атомами металлов и неметаллов. Валентность определяется числом электронов, которые атом может отдать или принять при образовании химической связи.
Если валентность металла и неметалла совпадает или различается не более чем на 1, образуется ионно-атомное или ионно-молекулярное соединение. В этом типе соединения металл отдает один или несколько электронов неметаллу, образуя положительный ион металла и отрицательный ион неметалла.
Если валентность металла и неметалла различается более чем на 1, образуется соединение с ковалентной связью. В этом случае атомы образуют совместные электронные пары, которые связывают их в молекулы. Тип соединения с ковалентной связью может быть различным в зависимости от валентностей элементов и их электроотрицательностей.
Если валентность металла и неметалла слишком большая, образуется металлическое соединение, в котором атомы металла образуют кристаллическую решетку, а электроны свободно передвигаются внутри нее. Металлические соединения обладают характерными свойствами металлов, такими как высокая электропроводность и теплопроводность.
Поведение металлов и неметаллов в агрессивной среде
При взаимодействии металлов с неметаллами в агрессивной среде происходят различные химические реакции, которые могут привести к разрушению или коррозии материала. Например, металлы, такие как железо, алюминий, медь и титан, могут реагировать с кислородом воздуха и влагой, образуя окислы металлов, которые являются основной причиной коррозии.
Однако, проявляются также и другие виды взаимодействия. Например, некоторые металлы могут реагировать с кислотами, образуя соли металлов и выделяяся водород. Железо, например, может реагировать с соляной кислотой с образованием хлорида железа и выделением водорода газа.
Адвидение металлов и металлов в агрессивной среде может привести к потере механической прочности, разрушению и выработке поверхностного слоя материала. Некоторые материалы имеют специальные покрытия, которые защищают от агрессивных сред, однако, с течением времени эти покрытия могут быть повреждены и возникнуть возможность контакта металла с агрессивной средой, что ведет к его повреждению.
В целом, поведение металлов и неметаллов в агрессивной среде зависит от их химических и физических свойств, окружающих условий и присутствующих химических реакций. Понимание этих процессов позволяет разрабатывать специальные материалы и покрытия, которые обладают повышенной стойкостью к агрессивным средам и могут использоваться в различных отраслях промышленности.
Коррозия и инертность элементов

Коррозия – это процесс разрушения и изнашивания материала вследствие его взаимодействия с окружающей средой. При контакте металлов с неметаллами могут происходить различные реакции, приводящие к коррозии. Например, при взаимодействии металла с кислородом из воздуха образуется оксид металла, который может проникать в материал и вызывать его разрушение.
Некоторые металлы обладают высокой инертностью и не подвержены коррозии. Например, золото, серебро и платина являются химически инертными металлами и не реагируют с большинством неметаллов. Их электрохимический потенциал является ниже, чем электрохимический потенциал кислорода, поэтому они не окисляются воздухом.
Однако некоторые металлы, такие как железо и алюминий, подвержены коррозии. Они могут реагировать с влагой, кислотами или щелочами из окружающей среды, образуя соединения, которые разрушают поверхность материала. Для защиты таких металлов от коррозии часто используют покрытия, например, цинковое покрытие или краску.
Инертность элементов играет важную роль в промышленности и электронной технике. Инертные металлы используются для создания электродов, электрических контактов и других частей, где требуется высокая устойчивость к окружающей среде. Благодаря своей инертности они не подвержены коррозии и сохраняют свои свойства в течение длительного времени.
Вопрос-ответ

Как происходит взаимодействие атомов металлов с неметаллами?
Взаимодействие атомов металлов с неметаллами происходит путем обмена или передачи электронов между атомами. При этом металл отдает электроны неметаллу, что приводит к образованию положительного ионного металлического ядра и отрицательного иона неметалла.
Какие неметаллы могут взаимодействовать с атомами металлов?
С атомами металлов могут взаимодействовать различные неметаллы, такие как кислород, хлор, сера, фтор и др. Каждый неметалл имеет свою электроотрицательность и способность принимать электроны от металла.
Каковы последствия взаимодействия атомов металлов с неметаллами?
Взаимодействие атомов металлов с неметаллами может привести к образованию ионных связей, ковалентных связей или металлических связей. Образование этих связей позволяет атомам металлов и неметаллов стабилизироваться и образовывать новые вещества с различными свойствами.
Какие свойства веществ могут изменяться в результате взаимодействия атомов металлов с неметаллами?
В результате взаимодействия атомов металлов с неметаллами могут изменяться такие свойства веществ, как температура плавления и кипения, твердость, проводимость электричества и тепла, химическая активность и др. Все это определяется спецификой образующихся связей и влияет на свойства конечного вещества.
Какие примеры взаимодействия атомов металлов с неметаллами можно привести?
Примерами взаимодействия атомов металлов с неметаллами являются образование солей, оксидов, кислот, оснований и многих других веществ. Например, реакция атомов натрия с атомами хлора приводит к образованию хлорида натрия, а взаимодействие атомов кислорода с атомами железа приводит к образованию оксида железа.
