Метод электролиза – это один из важнейших способов получения металлов, особенно из их солей. Он основан на использовании электрического тока, который переносит электроны и ионы металла из одной электродной ячейки в другую. Этот метод широко применяется в промышленности, так как позволяет получить чистые металлы необходимой степени очистки.
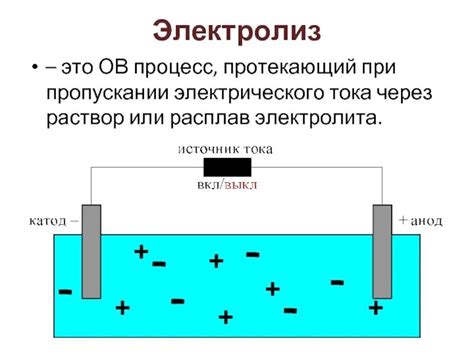
Процесс электролиза осуществляется в специальных электролизерных ячейках, в которых находятся электроды и электролит – раствор солей металла. Во время электролиза, катод – отрицательный электрод притягивает положительно заряженные ионы металла, а анод – положительный электрод привлекает отрицательно заряженные ионы. Под воздействием электролита и электрического тока, ионы металла переносятся из раствора на электроды, где оседают в виде чистого металла.
Метод электролиза широко используется для получения таких металлов, как медь, цинк, никель, алюминий и другие. Каждому металлу соответствует своя технология электролиза, определяющая не только температуру и время проведения процесса, но и особенности электродных элементов. С помощью метода электролиза можно получить высококачественные металлы, которые используются в различных областях, включая электротехнику, авиацию и сельское хозяйство.
Важно отметить, что метод электролиза характеризуется высокой энергозатратностью, поэтому в многих случаях разрабатываются и применяются более эффективные и экологически безопасные способы получения металлов. Но несмотря на это, электролиз по-прежнему остается одним из основных методов, обеспечивающих высокую степень очистки и получение требуемого качества металла.
Принцип метода электролиза

Метод электролиза — это процесс разложения веществ на элементы при помощи электрического тока. Он основан на электролитической диссоциации — разделении вещества на ионы под воздействием тока.
Принцип работы метода электролиза заключается в следующем: вещество, которое содержит ионы металла, располагается в специальной емкости, называемой электролитической ячейкой. В ячейке находятся два электрода: катод и анод. Катод подключается к отрицательному полюсу источника тока, а анод — к положительному.
Под воздействием электрического тока ионы металла перемещаются к аноду или катоду в зависимости от своего заряда. При достижении электрода ион получает или отдает электроны, что приводит к образованию атомов металла или ионов. Эти атомы или ионы далее соединяются и образуют металлы или металлические соединения.
Метод электролиза позволяет получать металлы из их солей, таких как оксиды, хлориды или сульфаты. Например, при электролизе раствора хлорида меди на катоде осаждаются атомы меди, а на аноде происходит реакция диссоциации воды. За счет электролиза могут быть получены различные металлы, такие как цинк, никель, алюминий и другие.
Выбор электролита для электролиза
Электролиз является эффективным способом получения металлов из их соединений, однако важно правильно выбрать электролит – вещество, участвующее в электролизе. Выбор электролита зависит от вида металла, который требуется получить. Электролит должен быть растворимым в воде и содержать ионы металла, который намеренно получают.
Один из способов выбора электролита – использование соли металла. Например, для получения меди из ее солей можно использовать электролитом раствор сернокислой меди (CuSO4). При электролизе этого раствора, на катоде осаждается медь, а на аноде образуется кислород.
Для получения других металлов, таких как никель или цинк, можно также использовать соли этих металлов. Например, для получения никеля можно использовать электролитом раствор никельсульфата (NiSO4), а для цинка – раствор сульфата цинка (ZnSO4).
Однако есть и другие методы выбора электролита для электролиза, такие как использование оснований или кислот. В зависимости от целей и условий эксперимента выбирается оптимальный электролит для получения требуемого металла.
Роли электродов в электролизе

Электролиз - это процесс разложения химических соединений с использованием электрического тока. Одним из ключевых элементов этого процесса являются электроды. Каждый электрод выполняет свою роль и необходим для успешного проведения электролиза.
Положительный электрод, называемый также анодом, является местом, где происходят окислительные процессы. На него подается положительный электрический заряд, что позволяет окисление ионов или молекул раствора. Результатом этого процесса может быть образование газа, осаждение вещества на аноде или образование новых соединений.
Отрицательный электрод, или катод, является местом, где происходят восстановительные процессы. На катод подается отрицательный электрический заряд, что позволяет восстановление ионов или молекул раствора. В результате этого процесса на катоде осуществляется осаждение металла или образование новых соединений.
Выбор материала для электродов зависит от среды, в которой проводится электролиз. Например, при электролизе растворов солей используются инертные электроды, такие как платина или графит. Это связано с тем, что электроды должны быть стабильными в химическом отношении и не участвовать в реакциях осаждения или окисления.
Таким образом, электроды играют важную роль в электролизе, определяя направление и характер происходящих химических процессов. Они обеспечивают разделение положительных и отрицательных зарядов, что позволяет эффективно получать металлы из их соединений.
Влияние параметров электролиза на процесс получения металлов
Метод электролиза является одним из наиболее эффективных способов получения металлов из их солей. Этот процесс основан на использовании электрического тока, который приводит к химическим реакциям и осаждению металлов на электродах. Однако эффективность этого метода зависит от нескольких параметров, которые необходимо учитывать при проведении электролиза.
Первым важным параметром является выбор материала электродов. Они должны быть проводниками электричества и устойчивыми в химически агрессивной среде. Также важным фактором является их размер и форма, которые определяют площадь контакта с раствором и, следовательно, скорость процесса.
Вторым параметром, влияющим на процесс электролиза, является напряжение, подаваемое на электроды. Оно должно быть достаточно высоким, чтобы вызвать разложение соли на ионы и осаждение металла. Однако избыточное напряжение может привести к побочным реакциям, повышению температуры и неравномерному осаждению металла.
Третьим фактором влияния на процесс электролиза является концентрация соли в растворе. Она должна быть достаточно высокой, чтобы обеспечить достаточное количество металлических ионов для осаждения. Однако слишком высокая концентрация может вызвать образование отложений на электродах и затруднить процесс.
Также необходимо учитывать температуру раствора. Она должна быть оптимальной для проведения реакции электролиза и осаждения металла. Слишком низкая температура может замедлить процесс, а слишком высокая - вызвать побочные реакции и повышенные потери энергии.
Кроме того, длительность проведения электролиза также играет важную роль. Слишком краткое время может не обеспечить полное осаждение металла, а слишком длительное время - привести к сторонним реакциям и затратам электрической энергии.
Таким образом, все параметры электролиза - материал электродов, напряжение, концентрация соли, температура и длительность процесса - оказывают влияние на эффективность получения металлов. Оптимальные условия подбираются экспериментально и зависят от конкретного металла и его соединения, что позволяет достичь наилучших результатов и получить металл высокой чистоты.
Примеры применения метода электролиза для получения металлов из солей
1. Получение алюминия из алюминиевых солей:
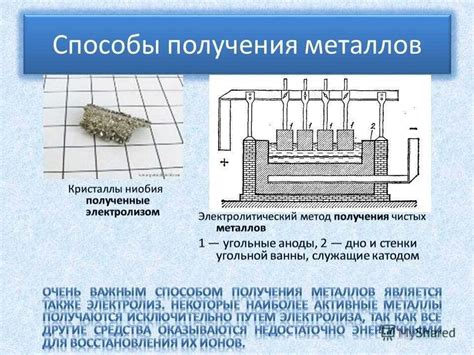
Один из наиболее распространенных примеров применения метода электролиза для получения металлов из солей - это получение алюминия из алюминиевых солей, например, алюминиевого оксида. При электролизе в расплавленной соли происходит разложение на ионы, положительно заряженные ионы алюминия переносятся к отрицательно заряженному электроду, где они получают электроны и восстанавливаются в металлическую форму.
2. Получение меди из медных солей:
Электролиз также применяется для получения меди из ее солей, таких как хлорид меди. При этом процессе положительно заряженные ионы меди переносятся к отрицательно заряженному электроду, где они получают электроны и осаждаются на поверхности, образуя металлическую медь. Этот метод является одним из основных способов получения меди в промышленном масштабе.
3. Получение никеля из никелевых солей:
Никель также можно получить из его солей методом электролиза. Например, при электролизе хлорида никеля образуются ионы никеля, которые мигрируют к отрицательному электроду и получают электроны, происходящая при этом реакция осаждает никель в металлической форме на электроде. Этот метод электролиза используется в промышленности для получения никеля.
4. Получение цинка из цинковых солей:
Цинк можно получить из его солей, например, хлорида цинка, с помощью метода электролиза. Ионы цинка, образующиеся при растворении соли, двигаются к отрицательно заряженному электроду, где происходит осаждение цинка в металлической форме. Этот метод используется в промышленности для получения цинка.
5. Получение свинца из свинцовых солей:
Метод электролиза также применяют для получения свинца из его солей, например, хлорида свинца. Ионы свинца при электролизе переносятся к отрицательно заряженному электроду, где они вступают в реакцию, формируя металлический свинец. Этот метод является одним из способов получения свинца в промышленных масштабах.
Таким образом, метод электролиза широко применяется для получения различных металлов из их солей. Этот метод позволяет эффективно извлекать металлы из растворов солей, что дает возможность использовать его в промышленности для получения металлических продуктов.
Преимущества и недостатки метода электролиза
Метод электролиза – это процесс, позволяющий получать металлы из их соединений путем применения электрического тока. Этот метод обладает как преимуществами, так и недостатками, которые следует учитывать при его использовании.
Преимущества:
- Возможность получать металлы высокой очистки. При электролизе соли металла с помощью электрического тока происходит разложение соединения на ионы, и металл осаждается на катоде. Такой способ получения позволяет получить металл с высокой степенью очистки от примесей.
- Экономическая эффективность. Метод электролиза является относительно дешевым, так как для его проведения требуется достаточно недорогое оборудование и ресурсы.
- Широкое применение. Электролиз используется в различных отраслях промышленности, включая металлургию, химию и энергетику.
Недостатки:
- Высокая энергозатратность. Для проведения электролиза требуется большое количество энергии, что влияет на его экономическую эффективность.
- Необходимость обеспечения режима проведения электролиза. Для успешного проведения электролиза необходимо обеспечить стабильный электрический ток и определенные условия, которые зависят от типа металла и его состояния.
- Возможность загрязнения окружающей среды. При проведении метода электролиза может возникать риск загрязнения окружающей среды, связанный с использованием определенных химических реагентов и отходов, образующихся в процессе.
Таким образом, метод электролиза имеет свои преимущества, такие как возможность получения металлов высокой очистки и экономическая эффективность, а также недостатки, включающие высокую энергозатратность, необходимость обеспечения режима проведения и риск загрязнения окружающей среды.
Перспективы развития метода электролиза

Метод электролиза является широко распространенным способом получения различных металлов из их соединений. Он имеет большой потенциал для дальнейшего развития и применения в различных отраслях промышленности.
Во-первых, метод электролиза позволяет получать металлы с высокой степенью чистоты. Это особенно важно для металлов, используемых в производстве электроники и медицинских приспособлений, где даже незначительные примеси могут снизить функциональность и эффективность изделий.
Во-вторых, метод электролиза можно эффективно применять для переработки отходов и вторичного использования металлов. Таким образом, он помогает уменьшить экологическую нагрузку промышленных предприятий и сократить потребление природных ресурсов.
Помимо этого, метод электролиза может быть улучшен и оптимизирован с использованием новых технологий и материалов. Например, внедрение нанотехнологий позволит повысить эффективность электролиза и снизить энергозатраты на процесс. Также, использование новых электролитов и электродных материалов может способствовать улучшению качества получаемых металлов.
В целом, метод электролиза имеет большой потенциал для развития и улучшения. Его применение в различных сферах промышленности позволяет получать металлы с высокой степенью чистоты, эффективно перерабатывать отходы и вторично использовать металлы. Развитие и оптимизация метода электролиза с использованием новых технологий и материалов открывает новые перспективы для применения этого метода в будущем.
Вопрос-ответ

Как работает метод электролиза для получения металлов из солей?
Метод электролиза основан на применении электрической энергии для разложения соединений металлов на их ионы и последующего осаждения металла из электролита на электроды. Электролиз осуществляется в электролитической ячейке, в которой находятся анод и катод. Когда электрический ток проходит через электролитическую ячейку, ионы металла перемещаются к электродам и на поверхности катода осаждается металл. Таким образом, метод электролиза позволяет получить металлы из их солей.
Какие металлы можно получить с помощью метода электролиза?
С помощью метода электролиза можно получить широкий спектр металлов. Некоторые из них включают натрий, калий, магний, алюминий, цинк, железо, никель, медь, свинец, серебро и золото. Однако металлы, которые очень трудно или невозможно получить по другим способам, могут также быть получены с помощью метода электролиза.
В чем преимущества метода электролиза в получении металлов из солей?
Метод электролиза имеет несколько преимуществ в получении металлов из солей. Во-первых, он позволяет получить чистые металлы высокой степени очистки. Во-вторых, этот метод позволяет получать металлы из их солей с высокой эффективностью и высоким выходом продукта. В-третьих, электролиз может быть проведен в больших масштабах, что делает этот метод применимым для промышленных процессов получения металлов. Наконец, электролиз позволяет получать металлы с высоким уровнем чистоты, что важно для различных применений металлов в промышленности и научных исследованиях.
