Металлы - это основные элементы химической системы, имеющие высокую электропроводность и благоприятное соотношение между протонами и электронами в своей атомной структуре. Одним из интересных свойств металлов является их способность реагировать с кислородом, образуя оксиды. Оксиды металлов, в свою очередь, являются основными соединениями, которые широко используются в различных областях нашей жизни.
Оксиды металлов представляют собой химические соединения, состоящие из атомов металла и кислорода. Они обладают различными физическими и химическими свойствами, зависящими от их состава и структуры. Некоторые оксиды металлов являются токсичными и могут вызывать различные заболевания, в то время как другие оксиды используются в производстве лекарств, косметики, красок, стекла и других материалов.
Основные оксиды металлов - это оксиды, которые образуются при реакции металлов с кислородом и взаимодействии сильных оснований. Эти оксиды обладают щелочными свойствами и способны растворяться в воде, образуя щелочные растворы. Они обычно обладают благородным металлическим блеском, высокой теплопроводностью и электропроводностью.
Примерами основных оксидов металлов являются: оксид калия (K₂O), оксид натрия (Na₂O), оксид кальция (CaO), оксид магния (MgO) и другие.
Основные оксиды металлов имеют множество применений в различных отраслях промышленности. Они используются для производства щелочных растворов, обработки металлов, производства стекла и керамики, а также в медицине и сельском хозяйстве. Благодаря своим уникальным свойствам основные оксиды металлов играют важную роль в нашей повседневной жизни и имеют большое значение для развития современной технологии и прогресса науки.
Металлы: образцы основных оксидов

В химии основными оксидами называют соединения металлов с кислородом. Эти соединения играют важную роль в различных процессах и применяются в разных сферах деятельности.
Образцы основных оксидов представляют собой химические соединения, состоящие из металла и кислорода. Оксиды металлов хорошо изучены и широко применяются в промышленности, науке и технологии.
Оксиды металлов могут быть кислотными или основными. Основные оксиды образуют сильные щелочные растворы воды и проявляют щелочные свойства. Они могут высвобождать ионы гидроксида, что делает их важными компонентами в различных процессах, включая производство стекла, керамики и цемента.
Некоторые примеры основных оксидов металлов включают оксид натрия (Na2O), оксид калия (K2O), оксид кальция (CaO) и оксид магния (MgO). Эти соединения имеют широкое применение в различных отраслях промышленности.
Например, оксид натрия используется в производстве стекла и мыла, оксид калия - в сельском хозяйстве и химической промышленности, оксид кальция - в строительстве и производстве цемента, а оксид магния - в косметической и фармацевтической промышленности.
Оксиды металлов: что это такое?

Оксиды металлов – это химические соединения, которые образуются при взаимодействии металла с кислородом. Оксиды металлов широко распространены в природе и играют важную роль в различных процессах.
Оксиды металлов обладают различными свойствами и применяются в разных отраслях промышленности. Одни из них являются основами и используются в производстве щелочных растворов или для нейтрализации кислот. Другие оксиды металлов, например, оксиды железа, применяются в производстве стали и других металлических сплавов.
Оксиды металлов имеют различные физические и химические свойства. Они могут быть кислотными, щелочными или нейтральными в зависимости от процента кислорода в соединении. Также они могут быть твердыми или жидкими, иметь особый запах или цвет.
Одним из наиболее известных оксидов металлов является оксид алюминия, широко используемый в производстве керамики, стекла и алмазов. Еще одним примером является оксид кальция, который используется в строительстве и в производстве цемента.
Важно отметить, что оксиды металлов могут иметь как полезные, так и вредные свойства. Некоторые оксиды металлов являются токсичными и могут вызывать отравление, поэтому необходимо соблюдать меры предосторожности при работе с ними.
Примеры основных оксидов металлов
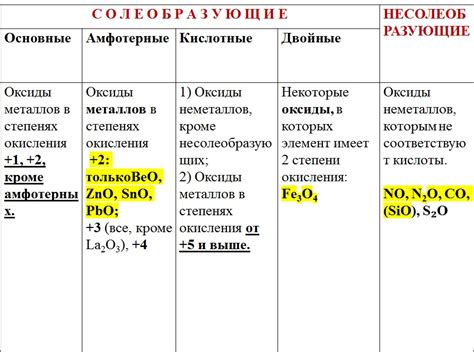
Оксиды металлов являются химическими соединениями, состоящими из металлического элемента и кислорода. Они образуются при взаимодействии металла с кислородом в присутствии воздуха или воды. Возможные окисления металла определяют тип оксида - кислотный, щелочной или нейтральный.
Один из примеров основных оксидов - оксид кальция (CaO). Он образуется при сгорании кальция или его соединений в присутствии кислорода. Оксид кальция является щелочным оксидом и хорошо растворяется в воде, образуя щелочную реакцию. Он используется в различных областях, включая производство цемента, стекла и керамики.
Другим примером основного оксида является оксид магния (MgO). Он образуется при сжигании магния или его соединений. Оксид магния также является щелочным оксидом и источником магний и кислорода. Он используется в производстве огнеупорных материалов, смазочных веществ и фармацевтических препаратов.
Оксид алюминия (Al2O3) - еще один пример основного оксида. Он образуется при обработке алюминия или его соединений. Оксид алюминия является нейтральным оксидом и обладает высокой теплостойкостью и химической инертностью. Он используется в производстве керамики, абразивов, катализаторов и электролитических конденсаторов.
В таблице ниже приведены примеры основных оксидов нескольких металлов:
| Металл | Оксид |
|---|---|
| Кальций | CaO |
| Магний | MgO |
| Алюминий | Al2O3 |
Важно отметить, что оксиды металлов имеют различные свойства и широко используются в различных отраслях промышленности, науке и технологиях. Они играют важную роль в обеспечении функциональности и применении металлических материалов.
Физические свойства основных оксидов

Оксиды являются основными химическими соединениями металлов с кислородом. Они обладают разнообразными физическими свойствами в зависимости от характера металла и его оксида.
Температурные свойства: многие основные оксиды обладают высокой температурной стабильностью. Например, оксиды щелочных металлов, такие как оксид натрия и оксид калия, выдерживают очень высокие температуры без разложения.
Электропроводность: большинство основных оксидов обладает низкой электропроводностью. Это связано с наличием ионной связи в их структуре. Однако, некоторые основные оксиды, например, оксид меди, обладают полупроводниковыми свойствами.
Физическое состояние: основные оксиды могут существовать в разных физических состояниях. Некоторые оксиды, например, оксид алюминия, представлены в виде твёрдых кристаллических соединений, тогда как другие, например, оксид серы, являются газами.
Растворимость: растворимость основных оксидов зависит от их химической природы и условий. Некоторые оксиды, например, оксид натрия, хорошо растворяются в воде, образуя щелочные растворы, в то время как другие оксиды, например, оксид алюминия, практически нерастворимы.
Кислотность: основные оксиды, как следует из их названия, обладают щелочным характером. Они могут реагировать с кислотами, образуя соли и воду. Например, оксид кальция реагирует с соляной кислотой, образуя хлорид кальция и воду.
Роль основных оксидов в химии и промышленности

Основные оксиды - это химические соединения, образующиеся при реакции металлов с кислородом. Их роль в химии и промышленности очень важна и разнообразна.
Во-первых, основные оксиды используются в производстве металлов. Многие металлы извлекают из руды путем ее обжига с кислородом, при этом образуются основные оксиды. Затем оксиды подвергаются специальным химическим процессам, чтобы получить чистый металл. Эта технология широко применяется в металлургической промышленности.
Во-вторых, основные оксиды являются важными ингредиентами в производстве различных химических соединений. Например, многие основные оксиды - это основные составляющие цемента, который широко используется в строительстве. Они также применяются в производстве стекла, керамики, эмали и других материалов.
Одна из важных ролей основных оксидов в химии - их свойство быть растворимыми в воде и образовывать основные растворы. Это свойство обусловлено наличием гидроксильных групп в структуре оксидов. Благодаря этому основные оксиды используются в различных химических процессах, например, в нейтрализации кислотных растворов или в производстве удобрений.
Кроме того, основные оксиды играют важную роль в экологии. Они могут быть использованы для удаления загрязнителей из воздуха и воды. Например, основные оксиды железа используются для удаления фосфора из сточных вод, что позволяет снижать загрязнение водных ресурсов.
В целом, основные оксиды играют важную роль в химии и промышленности, обладая разнообразными свойствами и широким спектром применений. Изучение и использование этих соединений позволяет нам лучше понять химические процессы и развивать новые технологии в различных отраслях промышленности.
Вопрос-ответ

Какие основные оксиды образуют металлы?
Металлы могут образовывать различные основные оксиды, в зависимости от их химической природы. Некоторые примеры включают оксиды кальция (CaO), натрия (Na2O), железа (Fe2O3) и меди (Cu2O).
Какова роль основных оксидов?
Основные оксиды играют важную роль в химических реакциях и различных процессах. Они часто используются в производстве стекла, цемента и других строительных материалов. Они также могут использоваться в качестве катализаторов и веществ для улучшения качества почвы или воды.
Как можно получить основные оксиды металлов?
Основные оксиды металлов можно получить путем нагревания соответствующей металлической пыли или солей в присутствии кислорода. Этот процесс, известный как окисление, вызывает выделение оксида металла в виде газа или твердого вещества.
