Амфотерными металлами называются вещества, которые могут реагировать как с кислотами, так и с основаниями. Данный класс веществ представлен рядом химических элементов, таких как алюминий, цинк, свинец, медь и другие. Особенностью амфотерных металлов является наличие активных электронных оболочек, что позволяет им вести себя по-разному в различных средах.
Амфотерные металлы широко используются в промышленности и находят применение в различных сферах. Например, алюминий является одним из самых распространенных амфотерных металлов и применяется в производстве авиационной и автомобильной промышленности, в строительстве, в производстве упаковочных материалов и т.д. Его свойство амфотерности позволяет использовать алюминий в качестве антикоррозийного материала, а также в процессе образования огнеупорных материалов.
Цинк, также относящийся к амфотерным металлам, широко используется в гальваническом производстве для покрытия поверхности других металлов, а также в производстве аккумуляторов, литий-ионных батарей и в других электротехнических устройствах. В связи с амфотерными свойствами, цинк может быть использован в процессе нейтрализации кислот и щелочей, а также в процессе очистки воды.
Применение амфотерных металлов на ЕГЭ может быть связано с заданиями по химии. Например, задачи по определению реакционной способности металлов или рассмотрению их свойств в различных средах. Изучение амфотерных металлов позволяет учащимся расширить свои знания в области химии и лучше понять принципы взаимодействия соединений веществ в различных условиях.
Определение и классификация амфотерных металлов
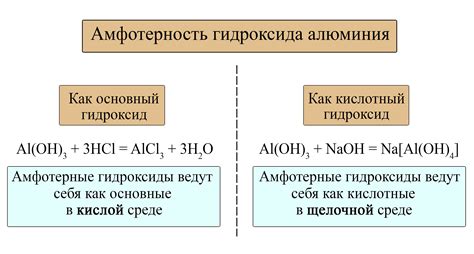
Амфотерными металлами называются вещества, способные проявлять свойства как металлов, так и неметаллов. Они могут образовывать как ионные соединения с кислородом и неметаллами, так и соединения с щелочными металлами.
Классификация амфотерных металлов осуществляется на основе их химических свойств и способности к реакциям с различными компонентами. Металлы этого класса обладают особенностью растворяться и проявляют активность при контакте с кислотами и щелочами.
Амфотерные металлы включают такие химические элементы, как алюминий (Al), цинк (Zn), германий (Ge), свинец (Pb), железо (Fe), кобальт (Co), гидроксиды которых обладают амфотерными свойствами.
Применение амфотерных металлов включает различные сферы. Например, алюминий применяется в производстве автомобилей, а также в производстве электрических проводов и кабелей. Железо, в свою очередь, является основным компонентом стали и используется в строительстве, производстве автомобилей и многих других отраслях промышленности.
Таким образом, амфотерные металлы представляют собой важную группу веществ, обладающих свойствами металлов и неметаллов, и имеют широкое применение в различных сферах человеческой деятельности.
Химические свойства амфотерных металлов
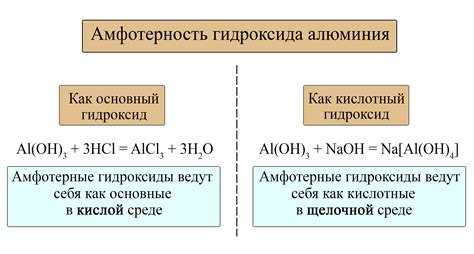
Амфотерные металлы - это металлы, которые обладают способностью образовывать соли и оксиды как с кислотными, так и с щелочными свойствами. Они могут реагировать как с кислотами, так и с основаниями, в зависимости от условий реакции.
Взаимодействуя с кислотами, амфотерные металлы образуют соли, при этом выступая в роли оснований. Они принимают от кислоты протон и образуются положительно заряженные ионы металла. Примером такой реакции может служить растворение алюминия в соляной кислоте:
2Al + 6HCl → 2AlCl3 + 3H2
В то же время, реагируя с щелочными растворами, амфотерные металлы образуют гидроксиды, проявляя кислотные свойства. В результате реакции они принимают от основания OH-ионы и образуются соответствующие гидроксиды металлов. Например, алюминий при реакции с натриевым гидроксидом образует алюминиевый гидроксид:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2
Амфотерные металлы обладают большой химической активностью и находят широкое применение в различных отраслях промышленности. Например, алюминий используется для производства авиационных и автомобильных деталей, а также в производстве электродов для сварки. Цинк широко используется в гальванической промышленности, а также для производства огнеупорных материалов.
В заключение, следует отметить, что амфотерные металлы являются универсальными веществами в химических реакциях, способными проявлять как кислотные, так и щелочные свойства, что позволяет им играть важную роль в различных процессах и применениях.
Примеры амфотерных металлов и их применение

Амфотерными металлами являются элементы, способные реагировать и с кислотами, и с основаниями. Они представляют собой особую группу металлов, которые проявляют двойственные свойства, позволяющие им участвовать в различных химических реакциях.
Один из примеров амфотерных металлов – алюминий. Он обладает способностью растворяться как в кислотах (например, в соляной кислоте), так и в щелочах (например, в растворе натрия гидроксида). Благодаря этим свойствам, алюминий находит широкое применение в различных отраслях промышленности: от производства строительных материалов до изготовления авиационной и космической техники.
Другим примером амфотерного металла является цинк. Он нейтрализует как кислоты, так и основания и может растворяться в них. Цинк используется в производстве гальванических покрытий, а также в производстве аккумуляторов и пигментов для красок.
Также в список амфотерных металлов входит свинец. Он растворяется как в кислотах, так и в основаниях. Благодаря своим физическим и химическим свойствам, свинец нашел применение в производстве аккумуляторов, косметических и керамических продуктов, а также в элементах электроники.
Особенности реакций амфотерных металлов

Амфотерные металлы – это класс веществ, которые могут проявлять как свойства оснований, так и свойства кислот в химических реакциях. Такие металлы являются универсальными активными элементами, способными взаимодействовать с различными классами соединений и реагентами.
В реакциях с кислотами амфотерные металлы проявляют свойства оснований, то есть они способны принимать протоны от кислотных реагентов. Например, амфотерный металл алюминий может реагировать с соляной кислотой, образуя соли алюминия и выделяя молекулы воды.
С другой стороны, в реакциях с основаниями амфотерные металлы проявляют свойства кислот, то есть способны отдавать протоны. Например, амфотерный металл цинк может реагировать с гидроксидом натрия, образуя соль цинка и выделяя молекулы воды.
Особенностью реакций амфотерных металлов является их способность образовывать соединения разной степени окисления. Например, амфотерные металлы, такие как железо и медь, могут образовывать как ионы с положительным зарядом (Fe2+, Cu2+), так и ионы с отрицательным зарядом (Fe3-, Cu-).
Применение амфотерных металлов включает широкий спектр областей, таких как производство лекарственных препаратов, катализаторов, электродов для аккумуляторов, а также изготовление сплавов и многие другие. Это связано с их уникальными химическими свойствами и способностью к взаимодействию с различными веществами.
Амфотерность металлов в контексте ЕГЭ

Амфотерность металлов – это способность некоторых металлов взаимодействовать и образовывать соединения как с кислотами, так и с щелочами. Такое поведение связано с особенностями структуры атомов данных металлов и их электронной конфигурации.
На ЕГЭ можно встретить задания, где требуется понять, как реагируют амфотерные металлы с разными веществами. Важно осознать, что амфотерность металлов позволяет им образовывать растворимые соли и ионы в кислой, щелочной и нейтральной средах.
Одним из примеров амфотерного металла является алюминий. Он способен растворяться как в сильных щелочах, так и в соляной кислоте, образуя соответствующие соли. Например, реакция алюминия с соляной кислотой приводит к образованию алюминия хлорида:
2Al + 6HCl → 2AlCl3 + 3H2
- Алюминий + соляная кислота → алюминий хлорид + водород
Применение амфотерных металлов в различных отраслях промышленности очень важно. Например, алюминий используется в производстве авиационных и космических конструкций из-за своей легкости и коррозионной стойкости.
Также, знание амфотерности металлов может быть полезно при изучении химии, так как многие химические реакции и процессы связаны с взаимодействием металлов с разными веществами.
Вопрос-ответ

Какие металлы называются амфотерными?
Амфотерными металлами называют металлы, которые могут образовывать ионы ионов как в качестве анода, так и в качестве катода.
Какие особенности присущи амфотерным металлам?
Одной из особенностей амфотерных металлов является их способность проявлять как кислотные, так и основные свойства в различных реакциях. Это связано с возможностью образования ионов с разными зарядами.
Каково применение амфотерных металлов на ЕГЭ?
На ЕГЭ амфотерные металлы применяются в заданиях, связанных с кислотно-основными свойствами веществ. Такие задания могут требовать определения окислителя или восстановителя в реакции или сравнения кислотности разных веществ.
