Соляная кислота (HCl) является одной из наиболее распространенных и важных химических соединений, которая широко применяется в промышленности и научных исследованиях. Одним из наиболее интересующих аспектов ее использования является влияние соляной кислоты на окисление металла.
Окисление металла – это процесс, при котором металлическая поверхность взаимодействует с окружающей средой, что приводит к образованию оксидов. Влияние соляной кислоты на этот процесс зависит от различных факторов, таких как концентрация кислоты, температура, тип металла и длительность взаимодействия.
Соляная кислота проявляет сильное влияние на окисление металла благодаря своим высоким окислительным свойствам. Взаимодействие соляной кислоты с поверхностью металла приводит к образованию хлорида металла и выделению водорода. Это обусловлено тем, что соляная кислота является сильным окислителем и способна извлекать электроны из металла.
Соляная кислота и ее влияние на окисление металлов

Соляная кислота – это очень активное и агрессивное химическое вещество, которое может взаимодействовать с различными металлами. Взаимодействие соляной кислоты с металлами приводит к процессу окисления, который может иметь важные технологические и научные применения.
Взаимодействие соляной кислоты с металлами происходит по принципу образования солей, но это процесс сопровождается выделением водорода. Соляная кислота эффективно окисляет многие металлы, такие как железо, алюминий, цинк и др. Одна из главных особенностей этого процесса – образование оксидов металлов, которые могут иметь различные свойства и применения.
Важно отметить, что окисление металла под воздействием соляной кислоты может приводить к образованию пленки на его поверхности. Эта пленка может выполнять защитную функцию, предотвращая дальнейшее окисление металла. Это свойство соляной кислоты широко используется в промышленности для получения защитных покрытий на металлических изделиях.
Соляная кислота также может использоваться для удаления окисных пленок и загрязнений с поверхности металлов. Она проникает в поры и трещины, растворяя окисные отложения и очищая поверхность металла. Этот процесс, известный как пассивация, может использоваться для восстановления металлических изделий и улучшения их внешнего вида и характеристик.
Таким образом, соляная кислота является мощным инструментом в области окисления металлов. Взаимодействие с этим химическим веществом может приводить как к окислению, так и к восстановлению металлов, что открывает широкий спектр возможностей для применения в различных сферах.
Химические свойства соляной кислоты

Соляная кислота (HCl) - одна из наиболее распространенных и широко используемых неорганических кислот. Она обладает рядом выдающихся химических свойств, которые определяют ее широкий спектр применения.
Во-первых, соляная кислота является сильной кислотой, образуя в водном растворе большое количество ионов водорода (H+). Это свойство делает ее идеальной для использования в химической лаборатории, так как она может использоваться для регулирования кислотности реакций и проведения различных химических экспериментов.
Во-вторых, соляная кислота является хорошим окислителем. Она способна окислять многие вещества, в том числе металлы, генерируя при этом большое количество тепла и газообразных продуктов. Данное свойство соляной кислоты используется в химической промышленности, например, для очистки металлов от окисных пленок перед их обработкой и для получения водорода путем реакции с металлами.
Кроме того, соляная кислота обладает растворяющими свойствами, способностью растворять многие вещества, в том числе металлы и их оксиды. Это свойство позволяет использовать соляную кислоту для очистки металлических поверхностей от ржавчины и других загрязнений, а также для получения растворов металлических солевых соединений.
В качестве реакционной среды соляную кислоту можно использовать для проведения некоторых органических реакций, таких как эфирализация и ацилирование. Также она применяется в производстве удобрений, пластиков, красителей и других химических веществ.
Реакция с водой и его значение

Соляная кислота (хлороводородная кислота, HCl) - это сильная минеральная кислота, которая широко используется в промышленности и лаборатории. При контакте с водой соляная кислота образует реакцию, которая может быть опасной и иметь разные последствия.
Когда соляная кислота смешивается с водой, происходит экзотермическая реакция, сопровождающаяся выделением тепла и образованием ионов водорода (H+) и хлорида (Cl-). Эта реакция может быть очень быстрой и взрывоопасной, особенно при больших концентрациях кислоты.
Реакция соляной кислоты с водой имеет большое значение в промышленности и научных исследованиях. Солькотолкательные (pH-стабилизаторы) добавки, основанные на этой реакции, могут использоваться для регулирования pH уровня в водных системах и процессах.
Соляная кислота также используется для очистки и обработки металлов. При контакте соляной кислоты с металлом может происходить окисление, что может привести к образованию газа водорода и выделению тепла. Этот процесс может использоваться для очистки поверхностей металла от окиси, ржавчины или загрязнений.
Однако реакция соляной кислоты с металлами и водой также может быть опасной и требует предосторожности. При неправильной обработке или неправильном смешивании соляной кислоты с водой может произойти непредсказуемая и сильно экзотермическая реакция, что может привести к опасным последствиям для здоровья и окружающей среды.
Кислотность соляной кислоты и ее влияние на металлические соединения

Соляная кислота (хлороводородная кислота) является одним из основных химических соединений, способных окислять металлы. Ее кислотность определяется концентрацией протонов, образующихся при диссоциации молекул кислоты в растворе.
Концентрация протонов соляной кислоты прямо пропорциональна ее кислотности. Чем выше концентрация протонов, тем сильнее окисляющие свойства кислоты и больше вероятность окисления металлов. Степень окисления металлов зависит от их электрохимической активности и концентрации соляной кислоты.
Под воздействием соляной кислоты металлы вступают в реакцию с протонами и образуют соли и водородный газ. Окисление металлов может привести к их коррозии или образованию пористого слоя оксидов на поверхности, что снижает их механическую прочность и электропроводность.
Важно отметить, что сила воздействия соляной кислоты на металлы может быть изменена путем регулирования концентрации или добавления ингибиторов, которые могут предотвратить окисление металлических поверхностей. Кроме того, различные металлы могут обладать разной степенью сопротивления окислению под действием соляной кислоты.
Уровень реактивности металла и его взаимодействие с соляной кислотой

Уровень реактивности металлов является важным фактором при взаимодействии с соляной кислотой. Различные металлы проявляют разные степени реакции на контакт с этой кислотой, что обусловлено их внутренней структурой и химическими свойствами.
Некоторые металлы, такие как натрий и калий, проявляют сильную реакцию с соляной кислотой. При контакте с кислотой они образуются обильное количество пузырьков газа, что свидетельствует о выделении водорода. Это связано с высоким содержанием активных электронов в их электронных оболочках, что облегчает окисление их водородом из кислоты.
Другие металлы, такие как алюминий и магний, реагируют с соляной кислотой, но менее активно. В процессе взаимодействия с кислотой они образуют хлориды металлов и выделяют меньшее количество водорода по сравнению с натрием и калием.
Некоторые металлы, такие как серебро и платина, практически не реагируют с соляной кислотой. Это связано с их низкими уровнями реактивности и инертностью кислоте, что позволяет им сохранять свою структуру и свойства в присутствии кислоты без значительных изменений.
Окисление активных и пассивных металлов
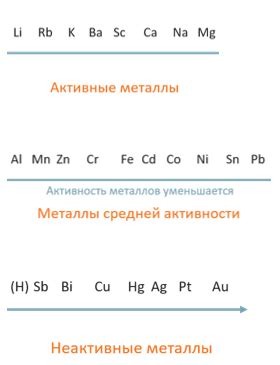
Окисление активных металлов
Активные металлы, такие как натрий, калий, цинк и алюминий, имеют невысокую устойчивость к окислению. При взаимодействии с соляной кислотой, активные металлы реагируют с ее кислотными компонентами, выделяя водород и образуя соли соответствующих металлов. Например, реакция натрия с соляной кислотой приводит к образованию хлорида натрия и выделению газообразного водорода.
Окисление пассивных металлов
Пассивные металлы, такие как нержавеющая сталь, титан и алюминий с оксидным покрытием, обладают высокой устойчивостью к окислению. Соляная кислота не способна эффективно окислять пассивные металлы при обычных условиях, так как их поверхность защищена оксидным слоем. Однако, при высоких концентрациях соляной кислоты или при наличии других окислительных веществ, пассивные металлы могут быть подвержены окислению.
Реакции окисления металлов
Окисление металлов в присутствии соляной кислоты происходит по следующему механизму - ионная реакция, в которой металл отдает электроны и переходит в положительный ион, а кислород получает электроны и становится отрицательным ионом. В результате образуются соли металлов и водород. Окисление активных металлов, таких как железо и цинк, происходит очень быстро и образуется большое количество водорода. Окисление пассивных металлов, таких как нержавеющая сталь, происходит гораздо медленнее и образуется меньше водорода.
Защита от окисления
Для защиты металлов от окисления соляной кислотой можно применять различные методы. Например, использование пассивных металлов с защитным оксидным покрытием может предотвращать контакт с кислотой. Также металлы могут быть защищены покрытием из других материалов, таких как пластик или керамика. Кроме того, регулярное нанесение защитных покрытий или использование антикоррозионных добавок может помочь уменьшить воздействие соляной кислоты на металлы и предотвратить их окисление.
Вопрос-ответ

Как соляная кислота влияет на окисление металла?
Соляная кислота играет роль окислителя при взаимодействии с металлом. Она вступает в реакцию с металлом и передает электроны, что приводит к окислению металла.
Какие металлы реагируют с соляной кислотой?
Соляная кислота может реагировать с большинством металлов, таких как железо, медь, алюминий, цинк и др. Однако, реакция может протекать по-разному в зависимости от концентрации кислоты и свойств металла.
Какие факторы могут повлиять на скорость окисления металла соляной кислотой?
Скорость окисления металла соляной кислотой может зависеть от нескольких факторов. Концентрация кислоты, температура реакции, площадь поверхности металла и продолжительность взаимодействия могут оказывать влияние на скорость окисления.
Какие продукты образуются при окислении металла соляной кислотой?
При окислении металла соляной кислотой образуются соответствующие соли и водород. Например, если реагирует цинк с соляной кислотой, то образуются цинк хлорид и молекулярный водород.
