Металлы баллов 1 группы периодической системы – литий, натрий, калий, рубидий, цезий и франций – известны своими сильными восстановительными свойствами. Эти металлы обладают возможностью передавать электроны, что позволяет им участвовать во многих химических реакциях.
Литий является самым легким металлом балла 1. Он обладает высокой активностью и реагирует с водой, кислородом и другими веществами. Литий используется в батареях, стеклах и лекарствах.
Калий также обладает сильными восстановительными свойствами. Он реагирует с водой, образуя взрывоопасный газ. Калий используется в производстве удобрений, стекла и прочих продуктов промышленности.
Барий – тяжелый металл, который может восстанавливать соединения с другими элементами. Барий используется в производстве рентгеновских ламп, стекла и красителей.
Алюминий, хотя и не является металлом балла 1, также обладает сильными восстановительными свойствами. Он используется в производстве алюминиевых сплавов, конструкций и пищевых упаковок.
В заключение, металлы баллов 1 литий, калий, барий и алюминий обладают сильными восстановительными свойствами, которые широко используются в различных отраслях промышленности и науки.
Свойства металла баллов 1 группы: лития, калия, бария и алюминия
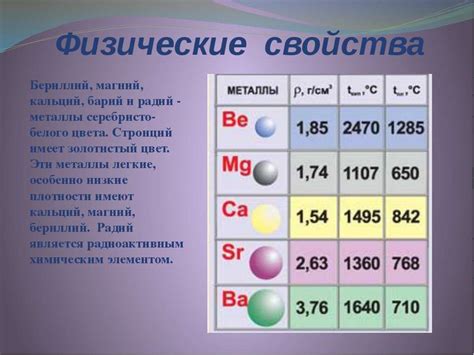
Литий (Li) является легким и очень реактивным металлом. Он обладает высокой электроотрицательностью и может быстро вступать в реакцию с водой или кислородом. Литий имеет низкую плотность и тает при невысокой температуре. Этот металл используется в производстве аккумуляторов, а также в некоторых медицинских препаратах.
Калий (K) также является реактивным металлом, но он менее активен, чем литий. Калий имеет мягкую текстуру и низкую плотность. Он имеет низкую точку плавления и может реагировать с водой, выделяя водород и образуя щелочное растворение. Калий широко используется в сельском хозяйстве в качестве удобрения, а также в производстве стекла и мыла.
Барий (Ba) является мягким и серебристым металлом. Он химически активен и может реагировать с кислородом, образуя оксид бария. Барий используется в производстве ламп низкого давления, а также в медицинской диагностике для создания контрастных веществ. Изотоп бария-137 используется в радиотерапии для лечения рака.
Алюминий (Al) является легким и коррозионно-стойким металлом. Он хорошо проводит электричество и тепло, что делает его идеальным материалом для использования в электрических проводах и теплообменниках. Алюминий также широко используется в строительстве, производстве упаковки и транспорте. Он может быть легко переработан и повторно использован, что делает его экологически более устойчивым, чем некоторые другие материалы.
Литий: сильное восстановительное действие
Литий - это химический элемент из группы щелочных металлов, который известен своими сильными восстановительными свойствами. Он является одним из наиболее активных металлов в периодической системе.
Сильное восстановительное действие лития связано с его способностью вступать в реакции с другими веществами и снижать окислительное состояние. Это свойство делает литий ценным элементом во многих промышленных процессах, а также в медицине и фармацевтике.
Литий используется в производстве литиевых батарей, которые отличаются высокой энергоемкостью и длительным сроком службы. Они широко применяются в электронике, автомобильной промышленности и других отраслях. Благодаря своим восстановительным свойствам, литиевые батареи обеспечивают эффективное хранение и передачу энергии.
В медицине литий используется в качестве лекарственного препарата для лечения биполярного аффективного расстройства. Это психическое заболевание характеризуется периодическими сменами настроения, от эйфории до депрессии. Литий помогает стабилизировать настроение и уменьшить частоту и тяжесть эпизодов заболевания.
Также литий может использоваться в производстве сплавов и керамики, добавляться в стекло для повышения его прочности и стойкости к воздействию окружающей среды. Этот металл обладает высоким температурным сопротивлением и химической инертностью, что делает его ценным материалом для различных технических и промышленных приложений.
Калий: преобразование в соединения с антиоксидантными свойствами
Калий – один из основных металлов, обладающий сильными восстановительными свойствами. Он способен превратиться в различные соединения, которые обладают антиоксидантными свойствами.
Антиоксиданты – это вещества, которые защищают клетки от воздействия свободных радикалов, предотвращая окислительные процессы и возникновение множества заболеваний. Калий, входя в состав соединений с антиоксидантными свойствами, способен защищать клетки организма и поддерживать их нормальное функционирование.
Преимущества калия и его соединений с антиоксидантными свойствами проявляются в поддержании здоровой работы сердечно-сосудистой системы, нормализации кровяного давления и улучшении работы нервной системы. Кроме того, калий помогает предотвращать развитие различных заболеваний, связанных с воспалением и окислительным стрессом.
Содержание калия в пищевых продуктах чрезвычайно важно для правильного функционирования организма. Однако, при недостатке этого металла, применение соединений калия с антиоксидантными свойствами может быть эффективной альтернативой. Важно помнить, что употребление калия и его соединений следует согласовывать с врачом, чтобы избежать возможных побочных эффектов.
Барий: активное участие в реакциях окисления-восстановления

Барий - это химический элемент, принадлежащий к группе щелочноземельных металлов. Он обладает сильными восстановительными свойствами и активно участвует в реакциях окисления-восстановления.
Барий способен образовывать ионы Ba2+, которые взаимодействуют с оксидами и пероксидами, восстанавливая их. В результате таких реакций образуются соответствующие оксиды или пероксиды бария. Эта особенность бария позволяет использовать его в процессах очистки воды и в производстве железа, где барий применяется в качестве восстановителя для удаления примесей оксида железа.
Кроме того, барий обладает способностью образовывать сплавы с другими металлами, такими как алюминий и калий. Эти сплавы также проявляют высокую активность в реакциях окисления-восстановления, что делает их полезными в различных промышленных процессах, включая производство стали и алюминиевых сплавов.
Таким образом, активное участие бария в реакциях окисления-восстановления делает его важным элементом для различных отраслей промышленности и науки.
Алюминий: высокая степень стойкости к окислительному воздействию

Алюминий, химический элемент с атомным номером 13, является одним из самых распространенных элементов в земной коре. В чистом виде алюминий обладает серебристым блеском и легкостью, что делает его идеальным материалом для многих промышленных и конструкционных задач.
Одной из наиболее удивительных характеристик алюминия является его высокая степень стойкости к окислительному воздействию. В отличие от многих других металлов, алюминий имеет внешнюю оксидационную пленку, так называемый оксид алюминия, которая предотвращает дальнейшее окисление металла.
Эта пленка образуется натуральным образом воздействием кислорода из воздуха и оберегает алюминий от коррозии и повреждений. Более того, если оксидационная пленка повреждается или разрушается, она сразу же восстанавливается под влиянием кислорода, что позволяет алюминию оставаться стойким к окислительным процессам.
Высокая стойкость к окислительному воздействию делает алюминий незаменимым материалом для производства различных конструкций и изделий, которым требуется сохранить свою форму и функциональные свойства в условиях высокой влажности, изменяющейся температуры или агрессивной среды.
Общие черты и сравнение свойств металлов баллов 1 группы

Металлы баллов 1 группы включают в себя литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Эти металлы обладают несколькими общими чертами, однако есть и отличия в их свойствах.
Во-первых, металлы баллов 1 группы имеют низкую плотность и низкую температуру плавления. Литий, например, является самым легким металлом с плотностью всего 0,53 г/см³. Калий ицезий также имеют низкую плотность и низкую температуру плавления.
Во-вторых, металлы баллов 1 группы обладают высокой реактивностью. Они мгновенно реагируют с водой, образуя щелочные растворы и выделяясь водородом. Их реактивность увеличивается по мере движения по группе от лития к францию.
В-третьих, металлы баллов 1 группы образуют ионы с положительным зарядом (+1). Они легко отдают электрон и образуют стабильные ионы, что делает их хорошими редукторами.
Однако, есть и отличия в свойствах металлов баллов 1 группы. Например, литий является самым легким и наиболее реактивным из них. Калий ищезий имеют более высокую температуру плавления и крахмаль, в отличие от других металлов этой группы, обладает совсем низкой реактивностью.
Таким образом, металлы баллов 1 группы обладают некоторыми общими чертами, такими как низкая плотность, низкая температура плавления и высокая реактивность. Однако, каждый из них имеет свои уникальные свойства, которые отличают их друг от друга. Это делает их важными и полезными элементами для различных промышленных и научных приложений.
Вопрос-ответ

Какие свойства у металла балла 1 лития?
Металл балла 1 лития обладает множеством восстановительных свойств, таких как способность восстанавливать кислородные соединения, восстанавливать многие неорганические и органические соединения, а также служить катализатором при реакциях гидрирования и дегидрирования.
Чем отличаются свойства металлов баллов 1 лития, калия, бария и алюминия?
Металлы баллов 1 лития, калия, бария и алюминия имеют различные восстановительные свойства. Например, литий обладает более сильными восстановительными свойствами, чем калий, барий или алюминий. Кроме того, каждый из этих металлов может взаимодействовать с различными соединениями и катализировать различные реакции восстановления.
Какие применения могут быть у металлов баллов 1 лития, калия, бария и алюминия с учетом их восстановительных свойств?
Металлы баллов 1 лития, калия, бария и алюминия находят широкое применение благодаря своим восстановительным свойствам. Например, литий используется в аккумуляторах, калий - в удобрениях, барий - в производстве светофильтров и радиоактивных источников, а алюминий - в производстве различных изделий, включая упаковку и строительные материалы.
