Водородные связи – это сильные не-коавалентные связи, которые могут образовываться между атомами водорода и другими атомами или молекулами. Одним из примеров таких связей является водородная связь между молекулами водорода и молекулами метана при участии атомов металлов.
Метан (CH4) – это простейший углеводород, состоящий из одного атома углерода и четырех атомов водорода. В молекуле метана атом углерода образует четыре одиночные ковалентные связи с атомами водорода. Такие молекулы, которые содержат водород и обладают потенциалом для образования водородных связей, называются акцепторами водородной связи.
Атомы металлов, такие как литий (Li), натрий (Na), калий (K) и др., обладают особенными химическими свойствами, которые позволяют им быть донорами водородной связи. Это означает, что атомы металлов могут донировать свои электроны для образования общих электронных облаков с акцепторами водородной связи, в данном случае, с молекулами метана.
Таким образом, между атомом металла, молекулой водорода и молекулой метана может образоваться водородная связь. Это может привести к образованию стабильных комплексов, которые имеют значительные энергетические преимущества и разнообразные химические свойства. Понимание и изучение механизмов образования и взаимодействия водородных связей между молекулами водорода и метана с участием атомов металлов может привести к разработке новых катализаторов и процессов, которые могут быть использованы в различных областях, включая химическую, энергетическую и фармацевтическую промышленность.
Механизм возникновения водородной связи

Водородная связь возникает между молекулами водорода и молекулами метана, при этом в процессе образования водородной связи участвуют атомы металлов. Механизм возникновения водородной связи основан на взаимодействии электронных облаков молекул водорода и метана с электродонорными и электроакцепторными свойствами атомов металлов.
При наличии электродонорных атомов металлов происходит донорно-акцепторное взаимодействие, при котором электронное облако молекулы водорода действует как донор и образует донорно-акцепторную пару с электронной оболочкой атома металла. В результате этого взаимодействия образуется слабая водородная связь между молекулой водорода и молекулой метана.
Электроакцепторные атомы металлов, в свою очередь, проявляют акцепторные свойства по отношению к электронной оболочке молекулы водорода, что позволяет образовывать акцепторно-донорные пары. Такое взаимодействие приводит к образованию вторичных водородных связей между молекулами водорода и метана.
Механизм возникновения водородной связи с участием атомов металлов характерен для различных процессов в природе и имеет большое значение в различных областях науки и техники, таких как химия, физика и биология.
Молекулы водорода и метана
Молекулы водорода и метана - это два различных химических соединения, состоящие из различных элементов и обладающие различными свойствами.
Молекула водорода (H2) состоит из двух атомов водорода. Это самый простой и наиболее распространенный вещества во Вселенной. Водород является легким, горючим и взрывоопасным газом. За счет своей низкой энергии связи между атомами, молекула водорода хорошо сжимается и может образовывать водородные связи с другими молекулами.
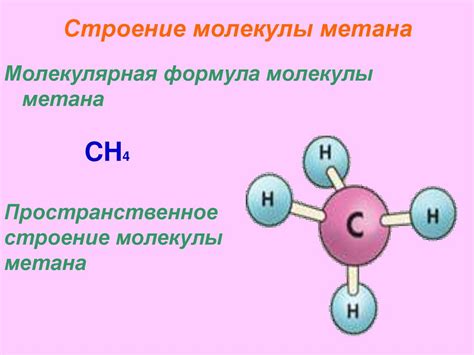
Молекула метана (CH4) состоит из одного атома углерода и четырех атомов водорода. Метан является безцветным и беззапаховым газом, широко распространенным в природе. Он используется в качестве топлива и сырья для синтеза различных химических соединений. Молекука метана имеет форму тетраэдра, где атом углерода находится в центре, а атомы водорода расположены вокруг него. Благодаря своей структуре и атомной конфигурации, молекула метана не образует водородные связи с другими молекулами.
Тем не менее, с участием атомов металлов, такие как натрий или медь, молекулы водорода и метана могут образовывать водородные связи. Это связи, которые образуются между электронно-податливыми атомами водорода и электроотрицательными атомами металлов. Это позволяет молекулам водорода и метана взаимодействовать между собой и образовывать сложные структуры.
Таким образом, водородные связи между молекулами водорода и метана с участием атомов металлов представляют собой важный фактор в различных химических реакциях и могут играть важную роль в образовании сложных соединений и материалов.
Роль атомов металлов

Атомы металлов играют важную роль в образовании водородной связи между молекулами водорода и молекулами метана. Металлы способны притягивать и удерживать молекулы водорода и метана, что способствует формированию водородной связи.
При наличии атомов металлов, молекулы водорода и метана могут образовывать стабильную структуру, где водородная связь служит "мостом" между атомами металлов и молекулами метана. В результате образуется металлоорганический комплекс, который имеет широкий спектр применения в различных областях науки и технологии.
Атомы металлов также влияют на химическую активность метана и водорода. Взаимодействие атомов металлов с молекулами метана и водорода может приводить к изменению структуры и энергии молекул. Это позволяет использовать металлоорганические комплексы в качестве катализаторов, ускоряющих химические реакции, в том числе превращение метана в другие полезные продукты.
В целом, атомы металлов являются важными компонентами для образования водородной связи между молекулами водорода и метана. Их присутствие способствует стабильности и активности металлоорганических комплексов, что открывает многообещающие перспективы для применения в различных областях науки и технологии.
Вопрос-ответ

Как происходит образование водородной связи между молекулами водорода и метана?
Образование водородной связи между молекулами водорода и метана происходит благодаря взаимодействию атомов водорода, содержащихся в молекуле метана, с атомами металлов. В результате образуется дополнительная связь, которая сильно укрепляет взаимодействие молекул и может приводить к изменению их структуры и свойств.
Какие атомы металлов участвуют в образовании водородной связи с метаном?
В образовании водородной связи с метаном могут участвовать различные атомы металлов, такие как литий, натрий, калий, медь, цинк и т.д. Каждый металл имеет свои характеристики и способность образовывать водородные связи может отличаться в зависимости от его электрохимических свойств.
Какое значение имеет образование водородной связи между молекулами водорода и метана?
Образование водородной связи между молекулами водорода и метана имеет большое значение с точки зрения химических реакций и взаимодействий между веществами. Она может повышать реакционную способность молекул, влиять на их физические и химические свойства, а также обеспечивать более эффективную передачу энергии и информации.
Какие практические применения может иметь образование водородной связи между молекулами водорода и метана с участием атомов металлов?
Образование водородной связи между молекулами водорода и метана с участием атомов металлов может иметь широкий спектр практических применений. Например, такие взаимодействия могут быть использованы в каталитических процессах, при производстве химических соединений, в электрохимии, в синтезе новых материалов и в других областях науки и промышленности.
