Водород – это наиболее обычный и известный элемент в периодической таблице Менделеева. Его атомный номер 1 указывает на его простую структуру - атом содержит только один протон и один электрон. Несмотря на свою простоту, водород является уникальным элементом с широким спектром физических и химических свойств.
Одним из интересных аспектов водорода является его классификация в периодической таблице. На первый взгляд может показаться, что водород должен быть металлом, так как расположен слева от периодической таблицы. Однако, в действительности водород не является ни металлом, ни полуметаллом, ни неметаллом. Химический символ H в периодической таблице указывает на его неметаллическую природу.
Вместо того чтобы быть металлом, водород обладает особой ролью в химии. Он может образовывать соединения с многими другими элементами, как металлическими, так и неметаллическими, и нести информацию о своей электроотрицательности. Водород также может образовывать два изотопа - электронейтральный протий и нейтронейтральный дейтерий, которые имеют свои уникальные свойства и применения.
Водород: особенности структуры атома
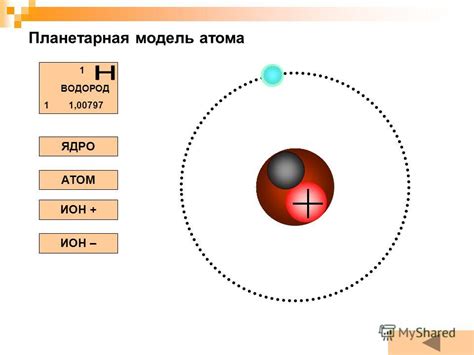
Водород – самый простой элемент в периодической системе химических элементов. Структура его атома состоит из одного протона в ядре и одного электрона движущегося вокруг него на определённых энергетических уровнях.
Обратите внимание, что электрон в атоме водорода находится на самом низком энергетическом уровне, так называемом основном состоянии. Именно поэтому водород является самым активным химическим элементом и обладает огромной химической реактивностью.
Кроме того, структура атома водорода обуславливает его особенности в связи с другими элементами. Водород, благодаря малой массе электрона и хорошей подвижности в природе, образует различные химические связи и взаимодействие с другими элементами, такими как кислород, углерод, азот и многими другими.
Интересной особенностью атома водорода является его изотопический состав. Атомы водорода могут иметь различное количество нейтронов в ядре, что влияет на их стабильность и свойства. Так, наиболее известными изотопами водорода являются протий, дейтерий и тритий, обладающие разными массами и свойствами.
В целом, структура атома водорода является уникальной и определяет его отличительные химические свойства. Водород играет важную роль во многих химических реакциях и процессах, а его изотопы находят применение в различных областях науки и промышленности.
Водородный атом: состав и строение
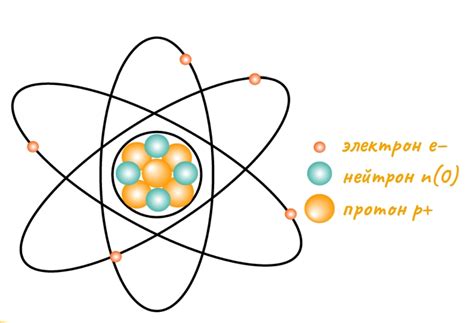
Водородный атом является наименьшим и простейшим атомом во всей таблице Менделеева. Он состоит из всего одного протона в ядре и одного электрона, движущегося по орбите вокруг ядра.
Протон, являясь элементарной частицей положительного электрического заряда, находится в центре атома, образуя его ядро. Единственный электрон, который находится на определенном расстоянии от ядра, движется с определенной скоростью по орбите.
Такое строение атома водорода является уникальным и обусловлено специфическими свойствами водорода. В связи с этим, водород широко используется в различных научных и технических областях, включая энергетику, химию и космическую промышленность.
Помимо основного водородного атома, существует также дейтерийный и тритиевый атомы, которые отличаются наличием двух или трех нейтронов в ядре, соответственно. Это делает эти атомы немного тяжелее и более устойчивыми.
Таким образом, водородный атом представляет собой особую систему, где протон и электрон взаимодействуют друг с другом, образуя устойчивую структуру. Это строение атома водорода играет важную роль в понимании основных законов и принципов атомной и молекулярной физики.
Водород: химические свойства и области применения

Водород – это самый легкий химический элемент, он обладает уникальными свойствами и широко применяется в различных областях. Он является неметаллом, но при высоком давлении и низкой температуре обладает металлическими свойствами.
Одним из главных химических свойств водорода является его высокая воспламеняемость. При контакте с источником огня он взрывается, что делает его важным компонентом ракетного топлива и средств пожаротушения.
Водород также обладает высокой электропроводностью и используется в процессе электролиза для получения различных веществ. Он является сырьем для производства аммиака, который широко применяется в производстве удобрений.
Водород используется в качестве водородных перекисей в медицине для дезинфекции и обработки ран. Также его применяют в промышленности при производстве стекла, металлов и пластмасс, а также в процессе сварки.
Более экологически чистые источники энергии, такие как водородные топливные элементы, становятся всё более популярными. Они применяются в автомобильной промышленности и энергетике, что позволяет снизить выбросы вредных веществ и уменьшить зависимость от ископаемых топлив.
В заключение, водород обладает уникальными химическими свойствами и широко применяется в различных областях. Он является важным компонентом ракетного топлива, сырьем для производства удобрений, используется в медицине, в промышленности и в качестве альтернативного источника энергии.
Водород: физические свойства и реактивность

Водород - наименьший и самый легкий химический элемент, характеризующийся уникальными физическими свойствами и высокой реактивностью. Он обладает уникальной способностью существовать в трех основных состояниях: газообразном, жидком и твердом.
Газообразный водород - безцветный, без запаха и безвкусный газ, которым можно заполнять шары и применять в различных процессах. Он обладает самой низкой плотностью среди всех газов и впитывается различными материалами, что делает его чрезвычайно легким и трудно удерживаемым. Газообразный водород также обладает высокой теплопроводностью и может быть использован в качестве энергетического исходного материала.
Жидкий водород - при очень низких температурах (-253,15°С) водород превращается в прозрачную и безцветную жидкость. Жидкий водород обладает очень низкой плотностью и может использоваться в качестве ракетного и реактивного топлива благодаря своим высоким энергетическим характеристикам.
Твердый водород - при очень низких температурах он может превращаться в твердое вещество со структурой, близкой к металлической. Твердый водород обладает невероятно высокой электропроводностью и сверхпроводимостью при очень низких температурах, что делает его потенциально интересным материалом для создания эффективных проводников и магнитов.
Водород является крайне реактивным элементом и может легко реагировать с большинством других элементов. Он может гореть в контакте с кислородом, образуя воду. Водород также может реагировать с различными химическими соединениями, образуя новые вещества. Эта высокая реактивность делает водород важным компонентом в многих химических и промышленных процессах, а также позволяет использовать его в качестве энергетического исходникита.
Водород: возможность превращения в металл

Водород – наиболее распространенный элемент во Вселенной. Его особенности и свойства поднимают много вопросов и вызывают интерес у ученых. Одним из таких вопросов является возможность превращения водорода в металл.
На данный момент существует несколько теорий, которые предполагают возможность металлизации водорода при достаточно высоком давлении. Согласно одной из таких теорий, при давлении более 4 миллиона бар водород должен стать металлическим.
Если эта теория окажется верной, то это откроет новые возможности для науки и технологий. Металлический водород будет обладать уникальными свойствами, которые смогут быть использованы в разных сферах, таких как энергетика, электроэлектроника и материаловедение.
Ученые проводят многочисленные эксперименты и моделирования, чтобы выяснить, как именно водород может стать металлом и каковы будут его свойства в этом состоянии. Несмотря на то, что на данный момент нет однозначного ответа на этот вопрос, исследования в этой области продолжаются. Это свидетельствует о том, что превращение водорода в металл – это одна из важных и интересных задач, которая активно изучается учеными со всего мира.
Вопрос-ответ

Водород – это металл?
Нет, водород не является металлом. Он является химическим элементом из группы неметаллов.
Почему водород не считается металлом?
Водород не считается металлом из-за его физических и химических свойств. У него нет характерных металлических свойств, таких как блеск, теплопроводность и пластичность.
Какие еще есть неметаллы, помимо водорода?
К неметаллам относятся такие химические элементы, как кислород, азот, фтор, хлор, сера и др. Они обладают свойствами, противоположными металлам.
