Вода является универсальным растворителем и существенным компонентом нашей жизнедеятельности. Она играет важную роль в множестве химических реакций, в том числе и в реакциях с оксидами щелочных металлов. Реакция воды с оксидами щелочных металлов весьма характерна и может протекать с образованием солей, кислот или щелочей.
Оксиды щелочных металлов являются бинарными соединениями состоящими из кислорода и металла. Примерами таких оксидов являются оксид натрия (Na2O), оксид калия (K2O) и оксид лития (Li2O). При контакте с водой, эти оксиды могут проявлять разную активность и вызывать различные химические реакции.
Реакция воды с оксидами щелочных металлов часто сопровождается образованием щелочного раствора. Например, оксид натрия реагирует с водой и образует щелочной раствор сильной щелочности – гидроксид натрия (NaOH). Такая реакция представляет собой образование гидроксида металла и сопровождается выделением большого количества тепла.
Взаимодействие воды с оксидами щелочных металлов: основные примеры и процесс образования

Взаимодействие воды с оксидами щелочных металлов является одной из основных реакций в химии. Оксиды щелочных металлов - это неорганические соединения, получаемые при сгорании металлов или их окислении. Когда они попадают в воду, происходит химическая реакция, сопровождающаяся выделением тепла и образованием основной соли.
Процесс взаимодействия воды с оксидами щелочных металлов начинается с растворения оксида в воде. При этом оксид превращается в гидроксид - основу. Примером такой реакции может служить реакция гидроксида натрия с водой:
- Натрий оксид (Na2O) + вода (H2O) → гидроксид натрия (NaOH)
Оксид натрия растворяется в воде, образуя гидроксид натрия, который в свою очередь является сильной щелочью. Подобные реакции происходят и с оксидами других щелочных металлов, например, лития, калия или цезия.
В результате взаимодействия воды с оксидами щелочных металлов образуется основной раствор. Этот раствор is непрозрачен, имеет выраженный щелочной вкус и влажность. Образование основного раствора является необратимым процессом, и его свойства существенно отличаются от свойств обычной воды. Основные растворы используются в различных отраслях химической промышленности, медицине и быту.
Взаимодействие воды с оксидами щелочных металлов - важный химический процесс, который находит применение в различных областях жизни человека. Понимание этого процесса позволяет лучше осознать свойства и характеристики основных растворов, а также использовать их в нужных целях.
Оксид натрия и его реакция с водой
Оксид натрия – это химическое соединение, образующееся в результате соединения натрия с кислородом. Он представляет собой белый кристаллический порошок, который обладает щелочными свойствами.
При контакте с водой оксид натрия происходит его реакция. В результате такой реакции образуются гидроксид натрия и выделяется большое количество тепла. Гидроксид натрия, или щелочь, является щелочным раствором и обладает щелочными свойствами.
Реакция оксида натрия и воды происходит со следующим уравнением:
- Na2O + H2O → 2NaOH
Оксид натрия может быть использован в различных областях: в производстве стекла, моющих средствах, мыле, щелочных батареях и др. Вода является необходимым компонентом для реакции оксида натрия, поэтому важно соблюдать безопасность при работе с этим веществом.
Взаимодействие оксида калия и воды

Оксид калия, также известный как калий пероксид, является химическим соединением из группы щелочных оксидов. При взаимодействии оксида калия с водой образуется гидроксид калия и выделяется кислород. Реакция происходит по следующему уравнению:
2 K2O + 2 H2O → 4 KOH + O2
В результате этой реакции образуется гидроксид калия, который является сильным щелочным раствором. При этом значительное количество кислорода выделяется в виде газа. Гидроксид калия имеет множество применений в различных областях, таких как химическая промышленность, медицина и сельское хозяйство.
Реакция взаимодействия оксида калия и воды является экзотермической, то есть выделяется значительное количество тепла. Кроме того, при этой реакции возможна ионизация оксида калия, в результате чего образуется гидроксид-ион и кислород-ион. Взаимодействие оксида калия и воды является одной из причин возникновения щелочного смещения в экологическом балансе водных систем.
Таким образом, взаимодействие оксида калия и воды приводит к образованию гидроксида калия и выделению кислорода. Эта реакция имеет широкое применение в промышленности и других областях и может оказывать влияние на экологический баланс водных систем.
Образование гидроксида рубидия при смешении воды и оксида рубидия

Гидроксид рубидия является щелочным соединением, образующимся при смешении воды и оксида рубидия. Оксид рубидия (Rb2O) представляет собой бинарное соединение, в котором кислород связан с атомами рубидия.
При контакте оксида рубидия с водой происходит реакция гидратации, в результате которой образуется гидроксид рубидия (RbOH) и высвобождается большое количество тепла. Эта реакция является экзотермической, то есть сопровождается выделением тепла.
Гидроксид рубидия обладает щелочными свойствами, поскольку ион OH- (гидроксид-ион) обладает отрицательным зарядом и способен давать гидроксидное ионное растворение в воде. Это значит, что гидроксид рубидия может образовывать раствор с щелочной средой, которая обладает рядом характеристик, таких как высокий уровень pH и способность нейтрализовать кислотные соединения.
Образование гидроксида рубидия при смешении воды и оксида рубидия является примером химической реакции между кислотой (водой) и основанием (оксидом рубидия). Эта реакция является одним из способов получения гидроксидов щелочных металлов в лабораторных условиях и имеет широкое применение в химической промышленности и научных исследованиях.
Оксид цезия и его реакция с водой

Оксид цезия (Cs2O) - химическое соединение щелочного металла цезия с кислородом. Он является белым кристаллическим веществом с высокой температурой плавления.
Реакция оксида цезия с водой происходит с образованием гидроксида цезия и выделением водорода. Данная реакция является экзотермической, то есть сопровождается выделением тепла.
Молекулярное уравнение реакции можно записать следующим образом:
- Cs2O + H2O → 2CsOH + H2
При взаимодействии оксида цезия с водой образуется гидроксид цезия (CsOH), который является сильной щелочной солью. Гидроксид цезия является гигроскопичным веществом, то есть способным быстро впитывать влагу из окружающей среды.
Реакция оксида цезия с водой происходит с выделением водорода. Водород является легким воспламеняющимся газом, поэтому при проведении данной реакции необходимо быть осторожным и соблюдать безопасность.
Взаимодействие оксида франция и воды

Оксид франция – это химическое соединение, представляющее собой оксид металла франция Fe2O3. Взаимодействие этого оксида с водой происходит с образованием особенного вещества – гидроксида франция Fe(OH)3.
Оксид франция не растворяется в воде, поэтому первоначально образуется осадок, состоящий из частиц оксида франция. При этом реакция протекает в две стадии:
- Окислительный процесс: водород из воды окисляется до гидроксида франция, а металл франция Fe3+ восстанавливается до иона франция Fe2+. В результате это приводит к образованию водорода H2 и гидроксида франция Fe(OH)3.
- Гидролиз: гидроксид франция реагирует с водой, что приводит к образованию ионов гидроксила OH- и ионов франция Fe3+. Таким образом, образуется гидроксид франция Fe(OH)3.
Взаимодействие оксида франция и воды проходит с выделением тепла и сопровождается реакцией, сопровождающейся изменением цвета раствора – он становится желтого цвета.
Гидроксид франция является слабым основанием, обладает амфотерными свойствами. Поэтому он может реагировать с кислотами, образуя соответствующие соли франция, а также сильнощелочные растворы, образуя комплексные соли франция, например, алуминат франция.
Образование гидроксида цезия при соединении воды и оксида цезия
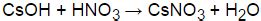
Гидроксид цезия – это бинарное соединение, образующееся при реакции воды с оксидом цезия. Оксид цезия (Cs2O) – это неорганическое вещество, содержащее атомы цезия и кислорода. При контакте с водой, оксид цезия реагирует, образуя гидроксид цезия (CsOH) и выделяя тепло.
Реакция между оксидом цезия и водой является экзотермической, то есть выделяет тепло. При соприкосновении оксида цезия с водой происходит химическая реакция, в результате которой образуется гидроксид цезия. Гидроксид цезия представляет собой кристаллическое вещество, растворимое в воде. Он выглядит как белый порошок или кристаллы сильного щелочного запаха.
Гидроксид цезия часто используется в лабораторных исследованиях, а также в промышленности. Он является важным компонентом в процессе получения других соединений цезия, таких как соли и органические соединения. Гидроксид цезия также применяется в качестве катализатора в различных химических реакциях.
Реакция воды с оксидами щелочных металлов, включая оксид цезия, является одной из основных реакций химии щелочных металлов. Образование гидроксида цезия в результате этой реакции подчеркивает важность гидроксидов щелочных металлов в различных областях науки и промышленности.
Оксид лития и его химическая реакция с водой

Оксид лития – химическое соединение, образующееся при окислении металлического лития воздухом. Он представляет собой белый кристаллический порошок с формулой Li2O.
Взаимодействие оксида лития с водой является более слабым по сравнению с некоторыми другими щелочными металлами, такими как натрий и калий. Но при контакте с водой оксид лития все же проявляет химическую активность.
При взаимодействии оксида лития и воды образуется слабое щелочное растворение.
Реакция оксида лития с водой:
- Легкий нагрев: при нагревании оксид лития с водой начинается реакция.
- Реакцией образуется щелочное растворение с образованием щелочной воды (LiOH) и выделением водорода (H2).
- Реакция протекает экзотермически, то есть сопровождается выделением тепла.
Образующийся при взаимодействии оксида лития с водой литиевый гидроксид (LiOH) является слабым щелочным раствором. Он имеет широкое применение в различных промышленных и научных областях, включая производство литиевых батарей и фармацевтической промышленности.
Гидроксид поглущает оксид калия при взаимодействии с водой

Оксид калия (K2O) – это химическое соединение, представляющее собой сильный щелочной оксид. При реакции с водой образуется гидроксид калия (KOH), который является щелочным гидроксидом.
В ходе взаимодействия оксида калия с водой происходит поглощение оксидом воды из атмосферы. Калий в оксиде находится во валентной форме +1, а в гидроксиде калия - в форме +1 и -1. За счет этого происходит реакция реагентов, и образуется гидроксид калия в результате гидратации гранул оксида калия.
Гидроксид калия (KOH) представляет собой гигроскопичное вещество, то есть способное притягивать и удерживать влагу из окружающей среды. При взаимодействии с оксидом калия образуется гидроксид, который обладает жидкой или плотной структурой в зависимости от условий эксперимента.
Вопрос-ответ

Как реагирует вода с оксидами щелочных металлов?
Вода реагирует с оксидами щелочных металлов, образуя основания. Реакция происходит с выделением тепла.
Какие примеры реакций воды с оксидами щелочных металлов можно привести?
Примерами реакций воды с оксидами щелочных металлов являются реакция натрия (Na) с водой (H2O), образующая гидроксид натрия (NaOH), и реакция калия (K) с водой, образующая гидроксид калия (KOH).
Почему при реакции воды с оксидами щелочных металлов выделяется тепло?
Выделение тепла при реакции воды с оксидами щелочных металлов связано с тем, что эта реакция является экзотермической, то есть происходит с выделением тепла. Энергия, выделяющаяся в результате реакции, связана с образованием новых химических связей в гидроксидах щелочных металлов.
Какие еще вещества могут образовываться в результате реакции воды с оксидами щелочных металлов?
В результате реакции воды с оксидами щелочных металлов могут образовываться не только гидроксиды, но и гидроксидные соли. Например, при реакции кальция (CaO) с водой образуется гидроксид кальция (Ca(OH)2), а при реакции магния (MgO) с водой образуется гидроксид магния (Mg(OH)2).
