Электронные формулы внешнего уровня металла являются важным инструментом для понимания строения и свойств различных металлических материалов. Внешний уровень металла относится к самому внешнему энергетическому уровню, на котором находятся электроны в металле. Ученые и инженеры используют эти формулы для изучения химических свойств, обработки и применения металлов в различных отраслях промышленности.
В электронных формулах внешнего уровня металла используется обозначение электронных оболочек, называемых энергетическими уровнями. Число электронов, находящихся на внешнем уровне, определяет химические свойства металла. Также они определяют способность металла образовывать химические связи с другими материалами.
Внешний уровень металла может быть представлен в виде формулы, как правило, с использованием символов, обозначающих энергетические уровни и количество электронов на каждом уровне. Например, внешний уровень железа может быть представлен формулой "3s^23p^64s^23d^6", где цифры и буквы указывают на количество электронов на каждом энергетическом уровне.
Изучение электронных формул внешнего уровня металла помогает определить основные свойства материала, например, его проводимость, пластичность и коррозионную стойкость. Это также помогает в разработке новых сплавов и материалов с улучшенными химическими и физическими свойствами.
Роль внешнего уровня металла

Внешний уровень металла играет важную роль в его свойствах и реакционной способности. Электронная структура внешнего уровня определяет, как металл взаимодействует с другими веществами и какие свойства он обладает. Внешний уровень металла обычно состоит из одной или нескольких энергетических подуровней, заполненных электронами.
Количество электронов на внешнем уровне определяет химическую активность металла. Металлы с неполной оболочкой электронов на внешнем уровне имеют большую склонность к взаимодействию с другими веществами и образованию соединений. Это объясняет их реакционную способность и способность к образованию ионов.
Свойства металлов также определяются их внешним уровнем. Например, большинство металлов отличаются высокой электропроводностью и теплопроводностью благодаря свободному движению электронов на внешнем уровне. Это позволяет им быть хорошими проводниками электричества и тепла. Также внешний уровень может определять магнитные свойства металла, его плотность и твердость.
Исследование внешнего уровня металла позволяет лучше понять его свойства и возможности применения. Это важно для разработки новых материалов и технологий, а также для изучения взаимодействия металлов с другими веществами. Понимание роли внешнего уровня металла помогает оптимизировать условия производства и улучшить качество конечных продуктов, основанных на металлах.
Как строится электронная формула
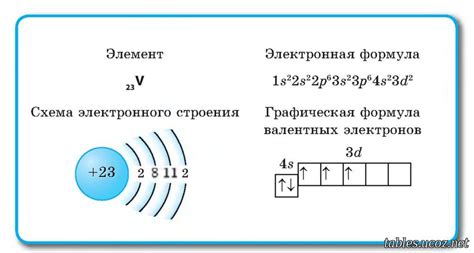
Электронная формула внешнего уровня металла – это способ отображения орбитального расположения электронов во внешней оболочке атома металла. Она позволяет визуализировать количество и заполненность электронных орбиталей металла, а также представить их в виде электронных подуровней.
Для построения электронной формулы внешнего уровня металла необходимо знать атомный номер металла и расположение его электронов на энергетической схеме. По атомному номеру можно определить количество электронов в атоме металла, а по расположению электронов можно определить их заполненность определенными энергетическими уровнями.
Основные шаги построения электронной формулы внешнего уровня металла:
- Определить атомный номер металла.
- Распределить электроны между энергетическими уровнями в порядке возрастания энергии.
- Поэлектроны в показываемымеле поднижнем подуровне заполняются полностью сначала!
- Определить количество электронов на внешнем уровне металла.
Электронная формула внешнего уровня металла позволяет получить представление о том, какие электронные орбитали металла заполнены и какие доступны для химических реакций. Это важно для понимания химических свойств и реакционной способности металла.
Взаимодействие внешнего уровня металла с другими элементами

Внешний уровень металла, также известный как валентный уровень, играет ключевую роль в его взаимодействии с другими элементами. Валентные электроны на этом уровне определяют химическую активность металла и способность образовывать связи с другими атомами.
Взаимодействие внешнего уровня металла с другими элементами может происходить посредством обмена или передачи электронов. Если металлический атом имеет меньшую электроотрицательность, он может отдавать свои электроны другим элементам, что приводит к образованию положительно заряженных ионов металла.
С другой стороны, металльные атомы также могут принимать электроны от других элементов с большей электроотрицательностью. В этом случае, металл становится отрицательно заряженным. Процесс образования ионов взаимодействием внешнего уровня металла с другими элементами называется ионизацией.
В результате взаимодействия внешнего уровня металла с другими элементами, образуются химические соединения, известные как металлические ионы. Эти ионы обладают своими характеристиками и свойствами, которые влияют на поведение и реактивность металла.
В общем, внешний уровень металла является ключевым фактором, определяющим его реактивность и взаимодействие с другими элементами в химических соединениях. Этот процесс имеет особое значение в контексте каталитических реакций и синтеза различных соединений, которые играют важную роль во многих областях науки и технологии.
Влияние электронного строения на свойства металла
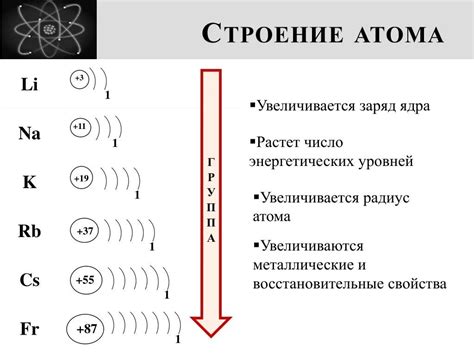
Электронное строение является одним из основных факторов, влияющих на свойства металла. Количество и распределение электронов в внешнем уровне металла определяет его химическую реактивность, электропроводность и магнитные свойства.
Количество электронов в внешнем уровне определяет, насколько легко металл может отдавать или принимать электроны. Металлы с малым количеством электронов в внешнем уровне, такие как щелочные металлы, имеют большую способность отдавать электроны и образовывать ионы положительного заряда. Это делает их хорошими проводниками электричества.
Распределение электронов в внешнем уровне также влияет на свойства металла. Металлы с электронами, расположенными ближе к ядру, обладают более высокими плотностью заряда и сильными металлическими связями. Это делает металлы твердыми, прочными и имеющими высокую температуру плавления.
Кроме того, электронное строение влияет на магнитные свойства металла. Материалы, такие как железо и никель, имеют неспаренные электроны, что приводит к возникновению магнитных свойств вещества.
Все эти факторы делают электронное строение ключевым аспектом, который необходимо учитывать при изучении свойств металла и его применении в различных областях, включая электронику, строительство и производство.
Практическое применение электронных формул внешнего уровня металла

Электронные формулы внешнего уровня металла имеют широкое практическое применение в различных областях. Одной из наиболее распространенных областей, где они используются, является металлургия.
С помощью электронных формул внешнего уровня металла возможно предсказать и объяснить различные свойства металлов, такие как их магнитные и электрические свойства, пластичность, твердость и т.д. Это позволяет инженерам и ученым разрабатывать новые сплавы, которые обладают определенными желаемыми свойствами.
Кроме того, электронные формулы внешнего уровня металла используются для определения и понимания реакций и превращений, которые происходят с металлами при воздействии различных внешних факторов, таких как температура, давление и влажность. Это важно для контроля качества металлов и разработки новых методов их обработки.
В области электроники и полупроводников также широко используются электронные формулы внешнего уровня металла. Они позволяют понять, как металлы влияют на электронный транспорт и проводимость в различных устройствах и материалах. Благодаря этому можно разрабатывать более эффективные и мощные электронные компоненты и системы.
Таким образом, практическое применение электронных формул внешнего уровня металла охватывает множество областей, включая металлургию, контроль качества, разработку новых сплавов, а также электронику и полупроводники. Разработка и использование этих формул позволяет нам лучше понять и контролировать свойства металлов и создавать новые материалы и технологии с оптимальными характеристиками.
Способы определения электронной формулы
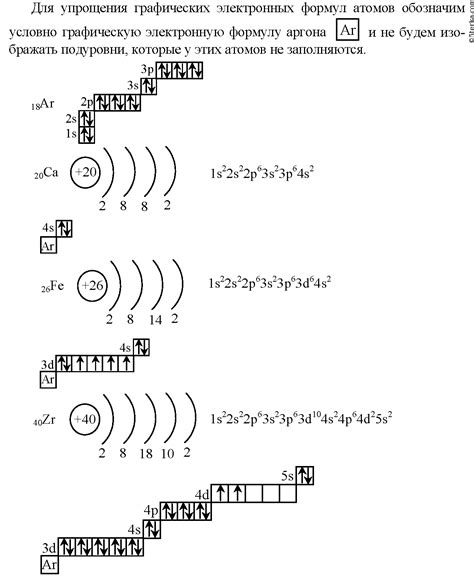
Электронная формула внешнего уровня металла определяет его активность и характер взаимодействия с другими элементами. Существуют различные способы определения электронной формулы, которые позволяют получить информацию о распределении электронов на внешней оболочке одного атома или иона металла.
Одним из способов определения электронной формулы металла является использование таблицы Менделеева. В таблице указывается количество электронов на каждом энергетическом уровне, что позволяет представить общую картину распределения электронов на внешнем уровне металла.
Кроме того, электронную формулу можно определить с помощью электронной конфигурации атома металла. Для этого необходимо знать последовательность заполнения энергетических уровней электронами и правила заполнения подуровней. Такая информация позволяет точно определить распределение электронов на внешнем уровне металла и его электронную формулу.
Также существуют способы определения электронной формулы внешнего уровня металла с использованием спектроскопических методов. Они позволяют анализировать характеристики излучения, поглощаемого или испускаемого металлом, и на основе этих данных определить электронную формулу металла.
Определение электронной формулы внешнего уровня металла имеет большое практическое значение, так как она определяет его свойства и возможность взаимодействия с другими элементами. Знание электронной формулы металла позволяет управлять его реактивностью и использовать его в различных промышленных процессах.
Ключевые особенности электронных формул внешнего уровня металла
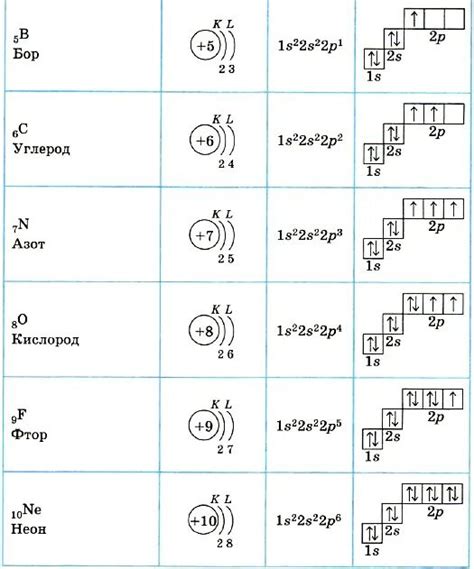
Электронные формулы внешнего уровня металла играют важную роль в определении его химических свойств и взаимодействий с другими веществами. Внешний уровень металла содержит электроны с наибольшей энергией, которые определяют его реакционную способность и химический потенциал.
Каждый металл имеет определенное количество электронов на внешнем уровне, которое часто определяет его положение в периодической системе элементов. Например, у металлов в 1-й группе периодической системы на внешнем уровне находится один электрон, а у металлов в 2-й группе - два электрона.
Электроны внешнего уровня металла обычно легко отделяются от атома, что является причиной их отличной электропроводности. Этот факт является основой для использования металлов в различных электронных и электрических устройствах. Отделяясь от атома, эти электроны создают "море" свободных электронов, которое может перемещаться по материалу и обеспечивать электрическую проводимость.
Электронные формулы внешнего уровня металла также помогают объяснить его химическую реактивность. Атомы металла могут обмениваться электронами с другими атмосферными атмосферами, образуя ионные связи или совместные связи. В результате этих реакций, металл может образовывать различные соединения и соединяться с другими элементами, что делает его весьма химически активным.
Примеры электронных формул внешнего уровня металла

1. Натрий (Na). В электронной формуле внешнего уровня металла натрия (Na) обычно указывают общую электронную формулу 2,8,1. Это означает, что внешний энергетический уровень металла натрия содержит 1 электрон, а внутренние уровни содержат соответственно 2 и 8 электронов.
2. Железо (Fe). Электронная формула внешнего уровня металла железа (Fe) обычно имеет вид 2,8,8,6. Это означает, что внешний энергетический уровень металла железа содержит 6 электронов, а внутренние уровни содержат 2, 8 и 8 электронов соответственно.
3. Медь (Cu). В электронной формуле внешнего уровня металла меди (Cu) присутствует следующая запись: 2,8,18,1. Таким образом, внешний энергетический уровень металла меди содержит 1 электрон, а внутренние уровни содержат 2, 8 и 18 электронов соответственно.
4. Алюминий (Al). Электронная формула внешнего уровня металла алюминия (Al) имеет вид 2,8,3. Поэтому на внешнем энергетическом уровне металла алюминия находится 3 электрона, а на внутренних уровнях содержится 2 и 8 электронов соответственно.
5. Серебро (Ag). В электронной формуле внешнего уровня металла серебра (Ag) указывают следующую запись: 2,8,18,18,1. Это означает, что внешний энергетический уровень металла серебра содержит 1 электрон, а внутренние уровни содержат 2, 8, 18 и 18 электронов соответственно.
6. Золото (Au). В электронной формуле внешнего уровня металла золота (Au) присутствует запись 2,8,18,32,18,1. Таким образом, внешний энергетический уровень металла золота содержит 1 электрон, а внутренние уровни содержат 2, 8, 18, 32 и 18 электронов соответственно.
Вопрос-ответ

Какая структура имеют электронные формулы внешнего уровня металла?
Электронная формула внешнего уровня металла имеет структуру, где наружному уровню металла присутствуют одна или несколько незаполненных d- и f-подуровней.
Каково значение электронных формул внешнего уровня металла?
Электронные формулы внешнего уровня металла имеют важное значение, поскольку они определяют химические и физические свойства металлов, их способность образовывать соединения с другими веществами и участвовать в различных химических реакциях.
Какие элементы могут образовывать электронные формулы внешнего уровня металла?
Электронные формулы внешнего уровня металла могут быть образованы различными элементами, включая переходные металлы, лантаниды и актиниды. Каждый из этих элементов имеет свою собственную электронную формулу внешнего уровня.
