Металлы являются основными компонентами различных материалов и представляют большой интерес при изучении их реакций с другими веществами. Одной из таких реакций является взаимодействие металлов с углеродом, в результате которого образуются иды.
Иды – это бинарные химические соединения, состоящие из металла и углерода. Они обладают различными свойствами и широко используются в промышленности и науке. Изучение процессов образования идов является важным направлением химических исследований и позволяет более глубоко понять взаимодействие металлов с окружающей средой.
При нагревании металлы могут реагировать с углеродными материалами и образовывать различные иды. Температура, давление и состав реакционной среды играют важную роль в этой реакции. Некоторые металлы, такие как железо, реагируют с углеродом при высокой температуре, образуя ид железа – железоуглеродистый сплав, который является основным компонентом стали.
Изучение реакции металлов с углеродом имеет большое практическое значение и позволяет разработать новые материалы с улучшенными свойствами. Это важное направление в развитии современной науки и технологий.
Металлы и их реакция с углеродом
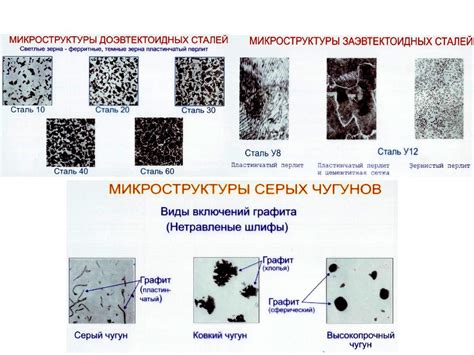
Металлы – это химические элементы, обладающие низкой электроотрицательностью и способные проводить электрический ток. Они широко используются в различных отраслях промышленности благодаря своим физическим и химическим свойствам.
Одной из интересных реакций, которую металлы проявляют, является их взаимодействие с углеродом. При нагревании металлов с углеродом образуются соединения, называемые карбидами. Эта реакция имеет большое практическое значение.
В результате реакции металлов с углеродом образуются карбиды, которые являются соединениями металла с углеродом. Карбиды могут быть структурированы как ионные соединения, ковалентные соединения или лигандные соединения. Они обладают различными свойствами и могут использоваться в производстве различных материалов.
Примером реакции металлов с углеродом является образование карбида железа (Fe3C) при нагревании чугуна с добавлением углеродного материала. Карбид железа обладает высокой твёрдостью и используется в производстве инструментов и материалов, устойчивых к износу.
Важно отметить, что реакция металлов с углеродом зависит от условий, в которых она происходит. Температура, давление, наличие катализаторов и другие факторы могут влиять на скорость и направление реакции.
В заключение, реакция металлов с углеродом является важным процессом, позволяющим получить карбиды с различными свойствами. Эта реакция используется в различных отраслях промышленности и имеет большое практическое значение.
Общее понятие об идах

Иды – это неорганические соединения, образующиеся в результате реакции металлов с углеродом при нагревании. Они являются типичными примерами бинарных соединений, состоящих из одного металла и одного или нескольких атомов углерода.
Иды широко распространены в природе и имеют большое промышленное значение. Они используются в различных отраслях, включая металлургию, химическую промышленность, электротехнику и другие.
Образование идов происходит в результате нагревания металлических идов с верхним или нижним графитовым слоем. При этом происходит реакция между металлом и углеродом, в результате которой образуется ид. Реакция может протекать при разных температурах и давлениях в зависимости от свойств металла и условий проведения процесса.
Важно отметить, что иды могут обладать различными свойствами и применяться с разными целями. Например, иды могут быть хрупкими и красивыми кристаллами, которые используются в ювелирном искусстве. Или же они могут быть прочными и применяться в производстве различных металлических сплавов и материалов с повышенной прочностью и стойкостью к коррозии.
Процесс нагревания металлов
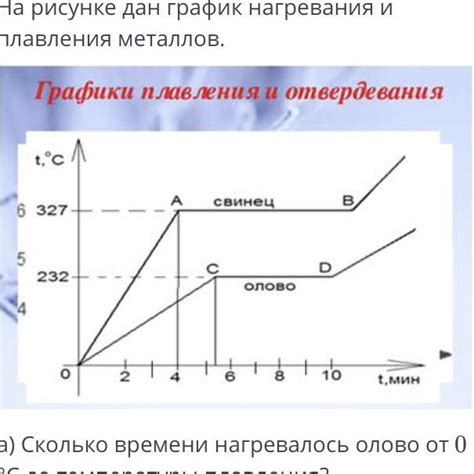
Процесс нагревания металлов является важным этапом в химических реакциях, связанных с образованием идов. Нагревание металлов происходит для активации их поверхности, что способствует реакции с углеродом.
Нагревание металлов может осуществляться различными способами, включая прямое нагревание на пламени горелки или в печи. При этом важно достичь определенной температуры, которая позволит запустить реакцию с углеродом.
Процесс нагревания металлов основывается на принципах термодинамики, а именно на изменении энергии связей веществ при нагревании. Под воздействием тепла, металлы начинают активно взаимодействовать с углеродом, что приводит к образованию идов и их последующему выводу.
Для эффективного нагревания металлов используются различные инструменты и устройства, способные создавать высокие температуры. Например, горелки с регулируемой интенсивностью пламени или печи с контролируемыми параметрами.
В ходе процесса нагревания металлов образуются различные соединения, отличающиеся структурой и свойствами. Например, при нагревании железа с углеродом образуется цементит, который обладает высокой твердостью и прочностью. Эта реакция широко используется в металлургической промышленности для получения сталей различного класса.
В заключение, процесс нагревания металлов является важным этапом в формировании идов при взаимодействии с углеродом. Он основывается на принципах термодинамики и активации поверхности металла. Результатом такой реакции являются новые соединения с измененными свойствами, которые находят широкое применение в различных отраслях промышленности.
Реакция различных металлов с углеродом
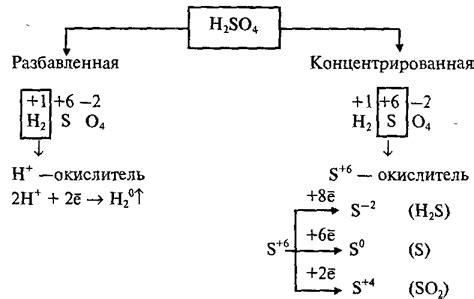
Металлы – вещества с высокой проводимостью электричества и тепла, химически они обладают активностью и способностью образовывать соединения с другими веществами. Реакция металлов с углеродом является одной из важных химических реакций, которая может происходить при нагревании.
Разные металлы проявляют различную реактивность при взаимодействии с углеродом. Например, алюминий, находящийся в верхней части периодической системы элементов, не реагирует с углеродом при обычных температурах. Однако, при высоких температурах возникает реакция алюминия с углеродом, при которой образуется карбид алюминия Аl4C3.
Более активные металлы, такие как железо, никель и кобальт, могут реагировать с углеродом уже при нагревании до 400 градусов Цельсия. При этом образуются железный карбид Fe3C, никелевый карбид Ni3C и кобальтовый карбид Co3C. Эти соединения обладают металлическими свойствами и находят применение в различных отраслях промышленности.
Однако самой известной реакцией металлов с углеродом является реакция железа с углеродом, которая происходит при высоких температурах в присутствии катализаторов. Результатом этой реакции является образование стали, которая широко используется в строительстве, автомобильной и машиностроительной промышленности, а также других отраслях производства.
Таким образом, реакция металлов с углеродом при нагревании может приводить к образованию различных карбидов, которые обладают разными свойствами и находят применение в разных областях промышленности. Эта реакция играет важную роль в современных технологиях и производстве.
Факторы, влияющие на реакцию

Реакция металлов с углеродом и образование идов при нагревании зависят от ряда важных факторов. Одним из ключевых факторов является температура, при которой происходит реакция.
На поведение металла в реакции с углеродом также влияет его химическая активность, которая определяется электрохимическим потенциалом. Металлы с более высокими активностями находятся в более высоких позициях в электрохимическом ряду и энергичнее реагируют с углеродом.
Форма и размеры образца металла также играют роль в реакции. Большая поверхность контакта образца с углеродом способствует более интенсивному протеканию реакции и образованию большего количества идов.
Химическое состояние металла, его чистота и примеси могут влиять на процесс реакции. Наличие примесей или оксидов на поверхности металла может замедлить или изменить ход реакции и влиять на выход идов.
Кроме того, на скорость и интенсивность реакции может влиять наличие катализаторов или добавок, которые могут активировать поверхность металла и ускорить процесс взаимодействия с углеродом.
Свойства образовавшихся идов

1. Реактивность: Образование идов при взаимодействии металлов с углеродом может происходить при различных температурах. Некоторые металлы, такие как железо и никель, могут образовывать иды при обычных условиях, а другие, такие как алюминий и цинк, требуют нагревания для этого процесса.
2. Строение: Иды обладают кристаллической структурой, которая может быть различной в зависимости от взаимодействующих металлов и углерода. Например, иды железа имеют кубическую решетку, в то время как иды алюминия образуют тетрагональные решетки.
3. Физические свойства: Образовавшиеся иды обычно обладают высокой плотностью и твёрдостью. Например, иды железа обычно являются твёрдыми и хрупкими материалами. Они имеют серый или черный цвет и не проводят электричество.
4. Химические свойства: Иды могут реагировать с различными веществами, образуя новые соединения. Например, ид железа может реагировать с кислородом в воздухе, образуя ржавчину. Они также могут растворяться в кислотах и образовывать соли.
5. Применение: Иды имеют широкое применение в различных отраслях промышленности. Например, ид железа используется как катализатор в химических процессах, а иды алюминия применяются в производстве литий-ионных аккумуляторов.
Применение идов в промышленности
Иды, образующиеся в результате реакции металлов с углеродом при нагревании, имеют широкое применение в различных отраслях промышленности. Они обладают рядом уникальных свойств, которые делают их незаменимыми во многих технологических процессах.
Одним из основных применений идов является их использование в производстве легированной стали. Сплавы с добавлением идов обладают повышенной прочностью и стойкостью к коррозии, что делает их идеальными для производства автомобилей, строительных конструкций и других металлических изделий, требующих высокой надежности и долговечности.
Кроме того, иды находят широкое применение в электронной промышленности. Они используются при производстве полупроводников, микрочипов и других компонентов электроники. Иды обладают высокой электропроводностью и подходят для создания микросхем малых размеров с высокой точностью и быстрой реакцией.
Применение идов также можно найти в производстве косметики и медицинских препаратов. Иды используются в процессе синтеза различных органических соединений, которые являются основой для производства косметических продуктов и лекарственных препаратов. Они обладают антибактериальными и противовоспалительными свойствами, что делает их важными компонентами в медицинской и косметической промышленности.
Наконец, иды находят применение в производстве различных аддитивов и катализаторов. Они используются в процессе синтеза различных химических соединений, таких как пластиковые полимеры и смолы. С помощью идов можно значительно повысить эффективность и скорость проведения химических реакций, что имеет положительное влияние на производительность и экономическую эффективность процесса.
Вопрос-ответ

Что такое реакция металлов с углеродом?
Реакция металла с углеродом - это химическая реакция, при которой металл взаимодействует с углеродом, приводя к образованию идов. Такие реакции могут происходить при нагревании металла с углеродным веществом, например, при обработке металла углеродистым газом или при нагревании металла в атмосфере углеродного материала.
Какие металлы реагируют с углеродом?
Ряд металлов могут реагировать с углеродом, включая железо, никель, хром, марганец, цинк и др. Эти металлы имеют достаточно высокую активность и способны образовывать иды при взаимодействии с углеродом.
Какие иды образуются при реакции металлов с углеродом?
При реакции металлов с углеродом образуются иды, которые представляют собой химические соединения металла с углеродом. Например, при реакции железа с углеродом образуется ид железа (Fe3C), известный также как цементит.
В каких условиях происходит реакция металлов с углеродом?
Реакция металлов с углеродом может происходить при нагревании металла с углеродным веществом. Также, некоторые металлы могут реагировать с углеродом при нормальных температурах и давлениях, если есть достаточная контактная поверхность между металлом и углеродом.
