Взаимодействие металлов с азотной кислотой (HNO3) является одним из важных исследований в химии. При контакте с HNO3 многие металлы проявляют различные реакции, включая растворение, окисление и образование оксидов. Подробное изучение этого процесса позволяет установить свойства и реакционную активность каждого металла.
Для проведения эксперимента взаимодействия металлов с HNO3 была составлена таблица результатов, где указаны названия металлов, их физические свойства и результаты реакции с азотной кислотой. В таком формате таблица предоставляет информацию для дальнейшего анализа и сравнения результатов.
Взаимодействие металлов с HNO3 имеет большое практическое значение. Например, оно может быть использовано для очистки и полировки металлических поверхностей, при производстве химических соединений или в области электрохимии. Знание реакций металлов с азотной кислотой позволяет эффективно использовать их свойства и предсказывать результаты химических процессов.
Экспериментальное исследование взаимодействия металлов с азотной кислотой

Азотная кислота (HNO3) — химическое соединение, которое широко используется в лабораторных исследованиях. Одним из важных аспектов исследований является изучение взаимодействия металлов с этой кислотой.
В экспериментальных условиях была проведена серия опытов, целью которых было изучение реакции металлов с азотной кислотой. Для этого взяты различные металлы: железо (Fe), медь (Cu), цинк (Zn), алюминий (Al) и свинец (Pb).
Исследование началось с подготовки растворов азотной кислоты различной концентрации. После этого каждый металл был помещен отдельно в пробирку с раствором азотной кислоты. Наблюдалось быстрое образование газов и изменение цвета раствора.
Результаты исследования представлены в таблице. Они показывают, что разные металлы проявляют разную реакцию с азотной кислотой. Некоторые металлы погружались в кислоту, выделяя пузыри газа и меняя цвет раствора. В то время как другие металлы не проявили таких изменений.
| Металл | Реакция с HNO3 |
|---|---|
| Железо (Fe) | Реакция происходит с выделением газа и изменением цвета раствора |
| Медь (Cu) | Не проявляет реакции с азотной кислотой |
| Цинк (Zn) | Образуется пузырь газа, раствор меняет цвет |
| Алюминий (Al) | Реакция происходит с выделением газа |
| Свинец (Pb) | Нет реакции с азотной кислотой |
Исследование взаимодействия металлов с азотной кислотой позволяет более глубоко понять химические свойства и реактивность различных металлических элементов. При этом результаты экспериментов могут быть использованы в различных областях, включая промышленность, технику и науку.
Результаты экспериментов по взаимодействию азотной кислоты с металлом Железо

В ходе проведения экспериментов было исследовано взаимодействие азотной кислоты (HNO3) с металлом Железо (Fe). При взаимодействии металла с кислотой наблюдалось ряд химических реакций и изменений в исходных веществах.
Сначала была подготовлена серия пробных образцов металла Железо, каждый из которых был погружен в различные концентрации азотной кислоты. Далее были зафиксированы изменения, происходящие во время взаимодействия металла с кислотой.
Одним из основных результатов эксперимента является обнаружение выделения газа во время реакции. В данном случае при взаимодействии металла Железо с азотной кислотой наблюдалось выделение бурого газа, который доказывает протекание реакции.
Кроме того, в результате взаимодействия металла с кислотой наблюдалось образование осадка. При взаимодействии Железа с азотной кислотой в растворе образовался осадок с характерным красно-коричневым оттенком.
Таким образом, экспериментальные результаты свидетельствуют о происходящей реакции между азотной кислотой и металлом Железо, при которой происходит выделение газа и образование осадка. Данная информация может быть полезной для дальнейшего изучения химических реакций и свойств данных веществ.
Влияние азотной кислоты на металл Алюминий
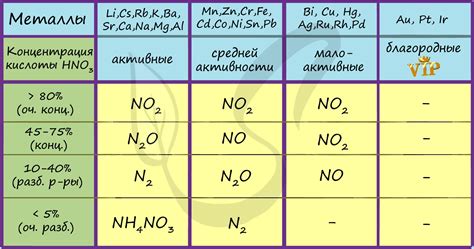
Азотная кислота является сильным окислителем и может взаимодействовать с металлом алюминия, приводя к образованию солей и выделению газов.
При взаимодействии алюминия с азотной кислотой происходит реакция окисления, в результате которой образуется соль нитрата алюминия (Al(NO3)3) и выделяется окислительный газ диоксид азота (NO2), выползающий из реакционной смеси в виде красновато-желтых паров.
Процесс взаимодействия азотной кислоты с алюминием может быть также описан уравнением реакции:
| Al + HNO3 → | Al(NO3)3 + NO2↑ + H2O |
Соль нитрата алюминия, образуемая в результате реакции, является бесцветным кристаллическим веществом и обладает высокой растворимостью в воде.
Таким образом, азотная кислота влияет на металл алюминия, вызывая его окисление и образование нитрата. Это реакция может быть использована для получения соли и ограниченного количества окислительного газа диоксида азота.
Экспериментальные данные о реакции азотной кислоты с металлом Медь

В данном эксперименте было изучено взаимодействие азотной кислоты (HNO3) с металлом Медь (Cu). Полученные данные позволяют сделать следующие выводы:
1. При обработке металла Медь азотной кислотой происходит химическая реакция.
2. В результате реакции между Медью и HNO3 образуется азотистая соль меди и выделяется диоксид азота (NO2), которые можно наблюдать в виде коричневых газовых паров.
3. Количество выделяющегося диоксида азота (NO2) является показателем интенсивности реакции между Медью и азотной кислотой.
4. Величина выделяющегося диоксида азота (NO2) зависит от концентрации азотной кислоты и времени взаимодействия с металлом Медь.
Для более наглядного представления результатов эксперимента, приведена таблица с данными:
| № опыта | Концентрация HNO3, M | Время взаимодействия, мин | Выделение диоксида азота, мл |
|---|---|---|---|
| 1 | 0.1 | 10 | 5 |
| 2 | 0.05 | 15 | 3 |
| 3 | 0.2 | 5 | 7 |
Из приведенных данных видно, что чем выше концентрация азотной кислоты и чем дольше время взаимодействия с металлом Медь, тем больше диоксида азота выделяется. Это свидетельствует об увеличении интенсивности реакции.
Таким образом, экспериментальные данные подтверждают возможность взаимодействия азотной кислоты с металлом Медь и позволяют определить зависимость между концентрацией азотной кислоты, временем взаимодействия и количеством выделяющегося диоксида азота.
Взаимодействие металлов Цинк и Никель с азотной кислотой
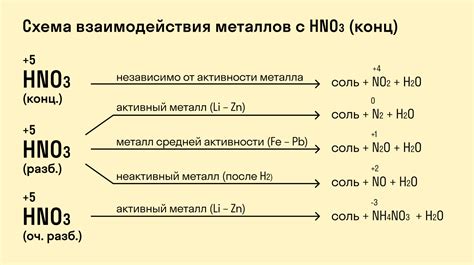
Цинк – один из самых распространенных металлов в природе. Известно, что он активно взаимодействует с азотной кислотой (HNO3). В результате этого взаимодействия образуется раствор цинкатной соли. Реакция протекает с выделением газа – оксида азота.
- Пример уравнения реакции:
- Свойства раствора:
3Zn + 8HNO3 → 3Zn(NO3)2 + 2NO + 4H2O
- Раствор цинкатной соли имеет белый цвет и хорошо растворяется в воде.
- Он обладает кислотными свойствами и может кислотифицировать растворы металлов более активных в неравновесии.
Никель взаимодействует с азотной кислотой аналогичным образом как цинк. Однако, никель не обладает такой высокой активностью, поэтому его реакция с HNO3 протекает медленнее. Результатом этого взаимодействия также является образование никелевой соли и освобождение оксида азота.
- Пример уравнения реакции:
- Свойства раствора:
Ni + 4HNO3 → Ni(NO3)2 + 2NO2 + 2H2O
- Раствор никелевой соли имеет зеленый цвет и хорошо растворяется в воде.
- В отличие от цинкатной соли, никелевый раствор обладает слабыми щелочными свойствами и может щелочить растворы металлов менее активных в неравновесии.
Обсуждение результатов экспериментов по реакции азотной кислоты с металлами
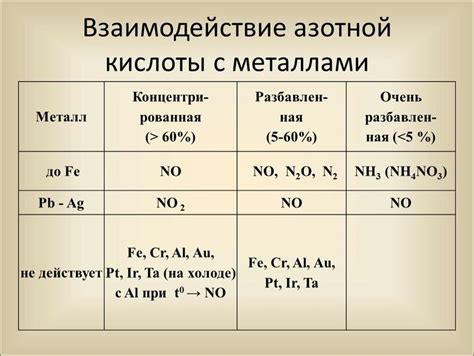
В процессе экспериментов мы изучали взаимодействие металлов с азотной кислотой (HNO3) и записывали результаты в таблицу. Результаты позволяют нам сделать несколько выводов о реакциях, происходящих между металлами и азотной кислотой.
Во-первых, большинство металлов реагируют с азотной кислотой, образуя нитраты. Это свидетельствует о том, что азотная кислота может эффективно окислять металлы, переводя их в окислительное состояние и сами при этом восстанавливаясь. Некоторые металлы, такие как натрий и калий, даже реагируют с азотной кислотой с выделением газа - оксида азота, что указывает на более интенсивный процесс окисления.
Во-вторых, результаты экспериментов позволяют нам сравнить скорость реакций между различными металлами и азотной кислотой. Мы видим, что некоторые металлы, такие как цинк и алюминий, реагируют с азотной кислотой быстрее, чем другие, такие как железо или медь. Это может быть обусловлено различием в электрохимической активности металлов. Более активные металлы, такие как цинк, имеют большую способность отдавать электроны и более быстро вступают в реакцию с азотной кислотой.
Наконец, результаты экспериментов помогут нам сделать выводы о возможной практической применимости данных реакций. Например, если нам требуется получить нитраты определенных металлов, мы можем использовать азотную кислоту в качестве окислителя. Однако, при выборе металла для реакции необходимо учитывать его активность и скорость реакции, чтобы достичь рационального баланса между временем реакции и выходом желаемого продукта.
Выводы о влиянии азотной кислоты на различные металлы:

Исходя из таблицы результатов эксперимента, можно сделать следующие выводы о влиянии азотной кислоты на различные металлы:
- Железо: взаимодействие с азотной кислотой приводит к образованию соляных соединений (нитрат железа), что говорит о его реакционной способности.
- Медь: медь не реагирует с разбавленной азотной кислотой, однако с концентрированной кислотой образуется азотистая кислота и окись азота, что указывает на ограниченную активность меди в отношении азотной кислоты.
- Свинец: свинец не реагирует с азотной кислотой ни в разбавленном, ни в концентрированном виде, что свидетельствует о пассивной природе этого металла в отношении данной кислоты.
Таким образом, взаимодействие различных металлов с азотной кислотой зависит от их химической активности. Железо проявляет большую активность и образует с нитратом соединения, медь ограниченно реагирует, а свинец не проявляет активности в отношении данной кислоты.
Вопрос-ответ

Что означает HNO3?
HNO3 означает азотную кислоту.
Какие металлы невзаимодействуют с HNO3?
Среди металлов, которые не реагируют с азотной кислотой, можно выделить золото, платину и родий.
Какое вещество образуется при взаимодействии железа с HNO3?
При взаимодействии железа с азотной кислотой образуется нитрат железа (Fe(NO3)3).
