Соли щелочных металлов – это класс химических соединений, состоящих из катионов щелочных металлов и анионов. К этой категории относятся соли лития (Li), натрия (Na), калия (K), рубидия (Rb) и цезия (Cs). За счет своей химической природы и структурных особенностей, соли щелочных металлов обладают разнообразными свойствами и широким спектром применения.
Одной из разновидностей солей щелочных металлов являются хлориды. Хлориды щелочных металлов имеют высокую растворимость в воде и обладают сильной кристаллической решеткой. Благодаря этим свойствам, хлориды щелочных металлов широко используются в химической промышленности, сельском хозяйстве, медицине и других отраслях. Например, хлорид натрия (NaCl), или поваренная соль, является одним из основных продуктов питания.
Еще одной разновидностью солей щелочных металлов являются карбонаты.Карбонаты щелочных металлов, такие как карбонат натрия (Na2CO3) и карбонат калия (K2CO3), обладают щелочным pH и являются важными компонентами в производстве стекла, мыла, моющих средств и других продуктов повседневного использования. Кроме того, карбонаты щелочных металлов широко применяются в процессах очистки воды и в производстве лекарственных препаратов.
Основные типы солей щелочных металлов
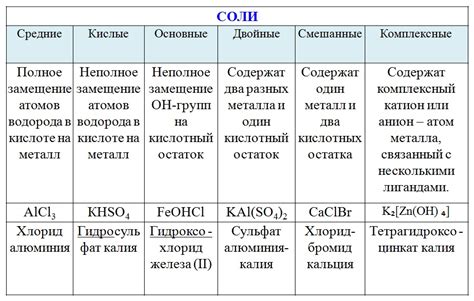
Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, образуют различные типы солей, которые обладают различными свойствами и применениями.
Сульфаты щелочных металлов являются одним из наиболее распространенных типов солей. Они образуются в результате реакции щелочного металла с сульфатной кислотой. Сульфаты обладают хорошей растворимостью в воде и находят широкое применение в производстве удобрений, стекла, щелочных батарей и других продуктов.
Хлориды щелочных металлов, полученные из реакции щелочного металла с хлоридной кислотой, также являются распространенным типом солей. Хлориды обладают высокой растворимостью в воде и используются в процессе электролиза, производстве стекла, пищевой промышленности и как добавка в средствах по уходу за кожей.
Нитраты щелочных металлов образуются в результате реакции щелочного металла с азотной кислотой. Они обладают хорошей растворимостью в воде и широко применяются в производстве взрывчатых веществ, удобрений и пищевой промышленности.
Карбонаты щелочных металлов являются основными составными частями природных миров и являются основой для производства пищевых добавок и лекарственных препаратов. Карбонаты обладают способностью нейтрализовать кислоты и являются основным компонентом антацидов.
Фосфаты щелочных металлов используются в производстве удобрений и пищевых добавок. Они образуются в результате реакции щелочного металла с фосфорной кислотой и обладают хорошей растворимостью в воде.
Ацетаты щелочных металлов являются солями уксусной кислоты и часто используются в пищевой промышленности в качестве консервантов и регуляторов кислотности. Они также широко используются в лабораторных исследованиях и производстве лекарственных препаратов.
Описание солей щелочных металлов и их разновидности
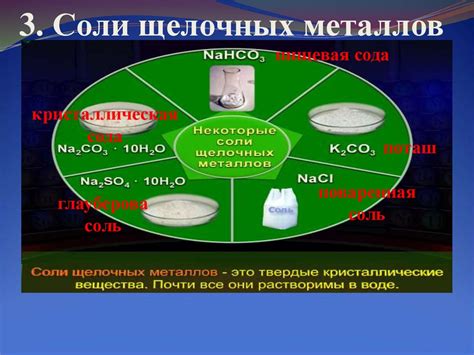
Соли щелочных металлов представляют собой химические соединения, образующиеся в результате реакции щелочных металлов (например, лития, натрия, калия) с кислотами. Они обладают различными свойствами и широко используются в различных областях.
В зависимости от ионов, которые могут образовывать, соли щелочных металлов могут быть однозарядными (например, хлориды и бромиды), двухзарядными (сульфаты и карбонаты) или многозарядными (фосфаты и нитраты). Каждый тип соли имеет свои особенности и применение.
Однозарядные соли щелочных металлов, такие как хлориды и бромиды, обладают хорошей растворимостью в воде и широко используются в медицине, пищевой промышленности и производстве удобрений. Они также являются важными электролитами.
Двухзарядные соли щелочных металлов, такие как сульфаты и карбонаты, нерастворимы в воде и могут использоваться в качестве пигментов, абразивных материалов и добавок в строительных материалах. Они также являются важными компонентами стекла и керамики.
Многозарядные соли щелочных металлов, такие как фосфаты и нитраты, обладают специфическими свойствами и применяются в производстве удобрений, стекла, керамики и других химических соединений.
В целом, соли щелочных металлов играют важную роль в промышленности, медицине, сельском хозяйстве и научных исследованиях. Их разнообразные свойства и применение делают их важными компонентами во многих отраслях человеческой деятельности.
Свойства солей щелочных металлов и их основные характеристики
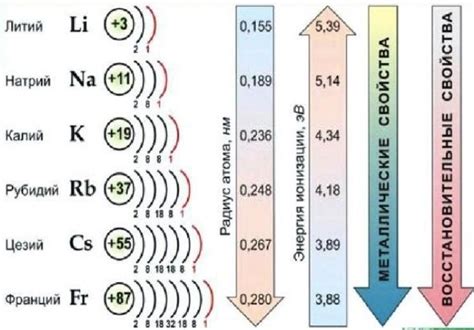
Соли щелочных металлов являются белыми кристаллическими веществами с высокой растворимостью в воде. Они имеют хорошую теплопроводность и электропроводность, что делает их полезными в различных применениях. Одной из основных характеристик солей щелочных металлов является их щелочная реакция, которая выражается в способности образовывать щелочные растворы при растворении.
Соли щелочных металлов также обладают высокими температурами плавления и кипения. Например, соль натрия имеет температуру плавления около 801 градуса Цельсия, а температура кипения составляет около 1413 градуса Цельсия. Эти значения связаны с сильными электростатическими силами взаимодействия ионов щелочных металлов в решетке кристалла.
Соли щелочных металлов также обладают высокой растворимостью в воде. Это связано с тем, что ионы металлов йодовых солей имеют высокую положительную энергию гидратации, что способствует их хорошей растворимости и стабильности в водных растворах.
Одним из основных свойств солей щелочных металлов является их способность образовывать двойные соли. Двойные соли состоят из ионов нескольких металлов и позволяют расширить диапазон их применения. Например, алюмошлюзовые соли, содержащие ионы алюминия и других металлов, используются в процессах обработки воды и производстве керамики.
Соли щелочных металлов также обладают хорошей термической стабильностью и низкой токсичностью, что делает их безопасными для использования в различных применениях. Они широко применяются в различных отраслях промышленности, включая производство стекла, мыла, удобрений и косметики.
Применение солей щелочных металлов в различных областях науки и промышленности

Медицина: Соли щелочных металлов, такие как натрий и калий, являются важными компонентами многих лекарственных препаратов. Они используются в качестве антацидов для нейтрализации избытка желудочной кислоты и снижения симптомов изжоги. Кроме того, соли этих металлов используются в инфузионной терапии для поддержания электролитного баланса в организме.
Пищевая промышленность: Соли щелочных металлов, особенно натрий, широко применяются в пищевой промышленности. Они используются как консерванты для продления срока годности продуктов, а также для улучшения вкуса и текстуры пищевых товаров. Например, натрий может использоваться для придания пикантности и поддержания структуры хлеба и кондитерских изделий.
Батарейная промышленность: Соли щелочных металлов, в особенности литий, играют важную роль в производстве аккумуляторов и батарей. Литиевые ионные батареи имеют высокую энергетическую плотность и малый вес, что делает их идеальными для использования в различных устройствах, таких как мобильные телефоны, ноутбуки и электромобили.
Стекольная промышленность: Соли щелочных металлов, в особенности калий, нашли применение в стекольной промышленности. Калийная соль используется для снижения температуры плавления стекла и улучшения его рабочих характеристик. Она также помогает снизить количество потребляемой энергии и улучшает качество производимого стекла.
Аналитическая химия: Соли щелочных металлов применяются в аналитической химии для проведения различных аналитических методик. Например, гидроксид натрия используется для проведения щелочного распада органических веществ, а цианид калия применяется для определения содержания нитратов и нитритов в образцах.
Текстильная промышленность: Соли щелочных металлов, особенно натрия и калия, используются в текстильной промышленности для обработки тканей и нитей. Натрий гидроксид используется для удаления восковых и жировых примесей с тканей, а карбонат натрия служит для регулирования PH растворов и отбеливания натуральных волокон.
Складирование энергии: Соли щелочных металлов, в особенности натрий и калий, также применяются в складировании энергии. Они используются в топотермических и химических системах хранения энергии, таких как солевые аккумуляторы и хранение тепла.
Вопрос-ответ

Какие разновидности солей щелочных металлов существуют?
Существует несколько разновидностей солей щелочных металлов, таких как хлориды, бромиды, йодиды, фториды, сульфаты, нитраты, карбонаты, гидроксиды и другие.
Какие свойства имеют соли щелочных металлов?
Соли щелочных металлов обладают несколькими характерными свойствами. Они обычно имеют высокую степень растворимости в воде, образуют кристаллическую структуру, хорошо проводят электрический ток, способны образовывать кислотные или щелочные растворы, обладают высокой термической устойчивостью и т.д.
В каких областях применяются соли щелочных металлов?
Соли щелочных металлов имеют широкое применение в различных областях. Например, хлориды и гидроксиды натрия используются в производстве щелочей, мыла и стекла. Нитраты и сульфаты калия используются в сельском хозяйстве как удобрения. Карбонаты щелочных металлов находят применение в производстве стекла, моющих средств и других товаров.
