Металлы - это важный класс элементов, которые обладают способностью вступать в химические реакции с другими веществами. Одной из наиболее распространенных реакций металлов является их взаимодействие с газами, особенно с газами воздуха. Столь разнообразные элементы, как железо, алюминий, медь и цинк проявляют различные степени активности в данной реакции, что обуславливает их применение в различных сферах нашей жизни.
Воздух, окружающий нас, состоит в основном из азота, кислорода и малых примесей газов. Такое разнообразие компонентов обуславливает различную реакционную активность металлов. Некоторые металлы, такие как золото и платина, почти не взаимодействуют с газами воздуха и могут сохранять свою блестящую поверхность на протяжении длительного времени. В то время как другие металлы, такие как натрий и калий, реагируют с кислородом и азотом, образуя соответственно оксиды и нитриды.
После реакции с кислородом и азотом, поверхность металла может измениться, что приводит к образованию пленки оксида или нитрида на его поверхности. Эта пленка может быть защитной, предотвращающей дальнейшую коррозию металла, или пористой, что может ускорить процесс разрушения. Поэтому важно понимать взаимодействие металлов с газами и подбирать материалы с учетом их поведения в конкретных условиях.
Металлические элементы

Металлические элементы – это химические элементы, обладающие свойствами металлов, такими как высокая теплопроводность, электропроводность, пластичность и блеск. В периодической системе элементов металлы находятся слева от ступеньки. Они представляют большую часть элементов таблицы Менделеева.
Металлы образуют ионы положительного заряда, которые легко взаимодействуют с отрицательно заряженными частицами, такими как атомы воздушных газов. При контакте с воздухом некоторые металлы могут окисляться, образуя оксиды или другие соединения.
Некоторые металлы, такие как железо и алюминий, обладают способностью образовывать защитную пленку оксида на своей поверхности, что предотвращает дальнейшую реакцию с воздухом. Другие металлы, такие как магний и цинк, реагируют более активно с воздухом, образуя соответственно оксиды и гидроксиды.
Некоторые металлы, такие как злато и платинум, не окисляются на воздухе и сохраняют свою блеск долгое время. Они называются драгоценными металлами и широко используются в ювелирной промышленности. Другие металлы, такие как натрий и калий, взаимодействуют так активно с воздухом, что даже могут самовоспламеняться при прикосновении к воздуху.
Металлы имеют множество применений в различных отраслях промышленности и производстве. Они используются для изготовления металлических конструкций, электрических проводов, транспортных средств, бытовых приборов и многого другого. Благодаря своим уникальным свойствам, металлы играют важную роль в современном обществе.
Окисление металлов

Окисление металлов - это процесс, при котором металлы взаимодействуют с кислородом воздуха и образуют оксиды. В результате окисления металлы могут менять свою внешность и свойства.
Окисление металлов происходит в присутствии кислорода и влаги. При этом поверхность металла покрывается слоем оксида, который защищает металл от дальнейшего окисления. Однако, в некоторых случаях оксид может быть пористым или разрушенным, что приведет к дальнейшему проникновению кислорода и продолжению окисления.
Окисление металлов может привести к изменению их свойств. Например, окисление железа приводит к образованию ржавчины, которая делает металл менее прочным и вызывает его разрушение. Окисление меди приводит к образованию зеленого налета (медной ржавчины), что может стать причиной потери электрической проводимости.
Для защиты металлов от окисления используют различные способы. Например, нанесение защитных покрытий (лака, краски, гальванических покрытий) или использование специальных антиоксидантов, которые замедляют процесс окисления.
Оксиды металлов
Многие металлы способны взаимодействовать с кислородом воздуха, образуя оксиды металлов. Оксиды металлов широко распространены и имеют различные свойства и применение.
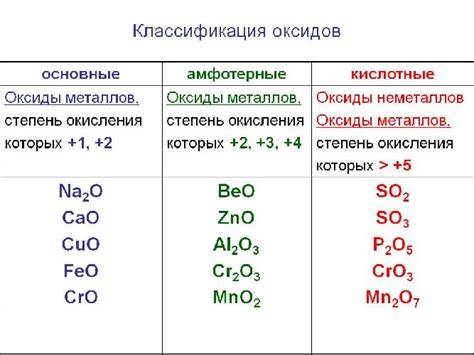
Оксиды металлов являются химическими соединениями, состоящими из атомов металла и кислорода. Они могут быть кислотными, основными и амфотерными в зависимости от своей реакции с водой. Кислотные оксиды образуют кислоты взаимодействуя с водой, основные оксиды - основания, а амфотерные оксиды могут взаимодействовать и с кислотами и с основаниями.
Одним из наиболее известных оксидов металлов является оксид железа (Fe2O3), который образуется при окислении железа. Он имеет красную окраску и используется в производстве красителей и шлифовальных материалов.
Другим примером оксидов металлов является оксид алюминия (Al2O3), который образуется при окислении алюминия. Он обладает высокой термической стабильностью и используется в производстве керамики, абразивных материалов и литейной продукции.
Некоторые оксиды металлов, такие как оксиды цинка и меди, обладают полупроводниковыми свойствами и используются в электронике и солнечных батареях.
Оксиды металлов также обладают различными физическими и химическими свойствами. Например, оксиды некоторых металлов могут быть растворимыми в воде, образуя щелочные растворы, тогда как другие оксиды металлов малорастворимы в воде.
Оксиды металлов играют важную роль в различных отраслях промышленности и технологии, а также являются основой для получения других соединений металлов.
Реакция с кислородом

Многие металлы обладают свойством реагировать с кислородом воздуха, что приводит к образованию оксидов металла. Эти реакции могут происходить с разной интенсивностью и зависят от типа металла и условий окружающей среды.
Некоторые металлы реагируют с кислородом более активно, например, натрий и калий. При контакте с кислородом они немедленно горят, образуя соответствующие оксиды, сопровождаясь яркими пламенем и выделением тепла.
Другие металлы, такие как алюминий и железо, реагируют с кислородом медленнее, образуя покрытие оксидов на поверхности металла. Этот оксидный слой может служить защитным барьером от дальнейшего окисления, так как препятствует проникновению кислорода к металлической поверхности.
Реакция с кислородом может иметь и коррозионный характер. Например, железо при длительном воздействии кислорода окисляется, образуя ржавчину. Это приводит к разрушению структуры металла и ухудшению его свойств.
Воздействие влаги

Металлы, контактирующие с влагой, подвергаются окислению и коррозии, что может существенно повлиять на их свойства и качество. Например, железо и его сплавы при воздействии воды образуют гидроксид железа (III), более известный как ржавчина. Ржавчина может привести к потере прочности и долговечности конструкций из стали.
Другие металлы, такие как алюминий, магний и цинк, также реагируют с влагой, образуя оксиды и гидроксиды, которые могут привести к образованию пленки на поверхности металла. Эта пленка может защитить металл от дальнейшей коррозии, но при сильном воздействии влаги и наличии других агрессивных сред, защитная пленка может быть повреждена и коррозия продолжится.
Кроме окислительного воздействия, влага может также способствовать электролитической коррозии. В присутствии электролита, такого как соль или кислота, металлы могут вступать в электрохимическую реакцию, приводящую к разрушению поверхности металла. Поэтому при проектировании и эксплуатации металлических конструкций необходимо учитывать воздействие влаги и принимать меры по защите металла от коррозии, такие как покрытия или антикоррозионная обработка.
Реакция металлов на воздухе: взаимодействие с газами

Металлы обычно реагируют с воздухом, образуя оксиды. Это происходит из-за взаимодействия металла с кислородом, присутствующем в воздухе. Однако, помимо кислорода, в атмосфере также содержатся другие газы, которые также могут влиять на реакцию металлов.
Один из таких газов - азот. Взаимодействие металлов с азотом может привести к образованию нитридов. Нитриды - это соединения металлов с азотом, которые обычно обладают повышенной твердостью и стойкостью к окислению. Нитриды могут быть использованы в различных отраслях промышленности, например, для создания прочных материалов или покрытий.
Другим газом, с которым металлы могут реагировать, является водород. Взаимодействие металлов с водородом может привести к образованию гидридов. Гидриды - это соединения металлов с водородом, которые обычно обладают особыми химическими и физическими свойствами. Например, гидриды некоторых металлов могут служить важными средствами для хранения и переноса водорода.
Кроме того, некоторые металлы могут реагировать с другими газами, такими как хлор, фтор, сероводород и другие. Реакция металлов с этими газами может привести к образованию сложных химических соединений, которые могут иметь различные применения в промышленности, науке и технологии.
Вопрос-ответ

Какие металлы реагируют с воздухом?
Некоторые металлы реагируют с воздухом, образуя оксидную пленку на своей поверхности. Например, натрий, калий и магний быстро реагируют с воздухом, образуя оксиды.
Что происходит с металлами, когда они взаимодействуют с воздухом?
Когда металлы взаимодействуют с воздухом, они могут ржаветь, окисляться или образовывать оксидные пленки на своей поверхности. Это может привести к коррозии металла или изменению его внешнего вида.
