Щелочные металлы – это группа элементов, которые находятся в первой группе периодической таблицы. К ним относятся литий, натрий, калий, рубидий, цезий и франций. Эти металлы отличаются реактивностью и химическими свойствами, что делает их интересными для изучения.
Если ты хочешь узнать больше о щелочных металлах, тогда наш бесплатный видеоурок идеально подойдет для тебя! Мы расскажем о свойствах каждого из этих элементов, их влиянии на окружающую среду и применении в промышленности.
Видеоурок будет насыщенным и информативным, а наш преподаватель – экспертом в области химии – сделает изучение этой темы увлекательным и понятным. Он расскажет о физических и химических свойствах каждого металла, даст примеры его применения в повседневной жизни и поделится интересными фактами.
Присоединяйся к нашему видеоуроку, чтобы узнать больше о щелочных металлах и их значении в мире науки и промышленности. Вместе мы пройдем путь от лития до франция и окунемся в захватывающий мир элементов!
Понятие и свойства щелочных металлов

Щелочные металлы - это группа элементов периодической системы химических элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они относятся к первой группе периодической системы и характеризуются своими уникальными свойствами.
Первое свойство щелочных металлов - их мягкость и пластичность. Благодаря низкой температуре плавления и высокой пластичности, они могут быть легко расплавлены и отформованы в различные формы. Это делает их ценными материалами в различных промышленных отраслях.
Второе важное свойство щелочных металлов - их химическая активность. Они очень реактивны и легко реагируют с кислородом, водой, аммиаком и другими субстанциями. Поэтому они хранятся в защищенных средах, чтобы предотвратить их реакцию с влагой и воздухом.
Третье особенное свойство щелочных металлов - их способность образовывать ионы. Они легко отдают свой внешний электрон, образуя положительно заряженные ионы. Это свойство делает щелочные металлы хорошими проводниками электричества.
Химические реакции и активность
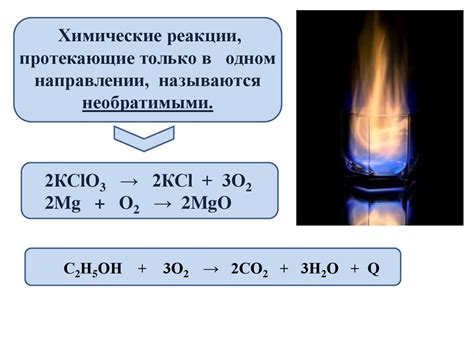
Химические реакции являются основным объектом изучения химии. Они происходят при взаимодействии различных веществ и приводят к образованию новых веществ с изменением их физических и химических свойств. Химические реакции могут быть обратимыми и необратимыми.
Активность элемента определяется его способностью взаимодействовать с другими веществами. Щелочные металлы, такие как литий, натрий и калий, являются очень активными элементами. Они способны реагировать с водой, кислородом и многими другими веществами.
При реакции щелочных металлов с водой происходит образование щелочи (щелочного гидроксида) и выделение водорода. Данная реакция является реакцией окисления-восстановления, так как щелочные металлы окисляются, а молекулярный кислород воды восстанавливается.
Активность щелочных металлов возрастает с увеличением номера периода в Периодической системе элементов. Литий является наиболее активным щелочным металлом, а калий - наименее активным. Активность элементов в группе щелочных металлов убывает сверху вниз.
Химические реакции щелочных металлов имеют различные практические применения. Например, натрий используется при производстве стекла и мыла, калий - при производстве удобрений, а литий - в производстве аккумуляторов.
Физические свойства и состояния
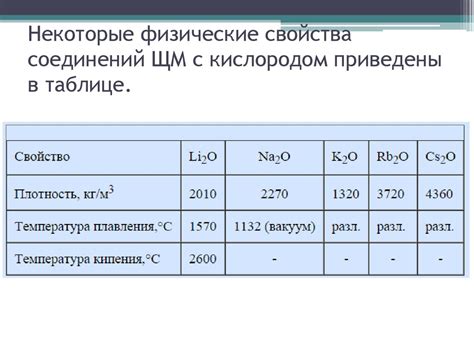
Щелочные металлы - это группа элементов, которые обладают сходными физическими свойствами. Они включают литий, натрий, калий, рубидий, цезий и франций. Одной из основных характеристик щелочных металлов является их низкая плотность. Например, литий, наиболее легкий из них, имеет плотность всего 0,53 г/см³.
Они также хорошо проводят электричество и тепло. Щелочные металлы обладают высокой электропроводностью благодаря наличию одной внешней электрона в своей внешней оболочке, который легко перемещается между атомами. Это делает их ценными материалами для производства аккумуляторов и других электрических устройств.
Кроме того, щелочные металлы характеризуются низкой температурой плавления и кипения. Так, литий плавится при температуре всего около 180 градусов Цельсия, а его температура кипения составляет около 1342 градусов Цельсия. Это делает их подходящими для использования в различных технических приложениях, где требуется низкая температура плавления.
Также щелочные металлы хорошо растворяются в воде и образуют гидроксиды, которые имеют щелочную реакцию. Например, натрий реагирует с водой, образуя гидроксид натрия и выделяющийся водород. Эта реакция широко используется в химической промышленности и в бытовых целях, например, в мыле и чистящих средствах.
В целом, физические свойства и состояния щелочных металлов делают их важными и интересными для исследования. Изучение их свойств помогает нам понять особенности химических реакций, а также разработать новые материалы и технологии, обладающие уникальными свойствами.
Исторический обзор щелочных металлов
Щелочные металлы - группа элементов, относящихся к первой группе периодической таблицы. Они включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). История открытия и исследования этих металлов уходит в глубокую древность.
Первым щелочным металлом, который был известен людям, является натрий. Известно, что его соединения использовались еще в древнем Египте и Месопотамии для приготовления различных продуктов и веществ. Однако, сам металл был получен в чистом виде только в начале XIX века.
История открытия других щелочных металлов тесно связана с развитием науки и технологий. Например, в конце XVIII века ученые начали исследовать натрий и калий с помощью электричества, используя электролиз. Это позволило получить натрий и калий в чистом виде и установить их химические свойства.
В XIX веке было открыто несколько новых щелочных металлов, таких как литий, рубидий, цезий и франций. Они были получены из минералов и природных источников, исследованы и использованы в различных областях науки и промышленности.
Сегодня щелочные металлы широко применяются в различных отраслях, таких как производство батарей, стекла, синтез органических соединений и других веществ. Изучение их свойств и возможностей продолжается, и каждый новый открытый факт приводит к расширению представлений о щелочных металлах.
Древние открытия и первые исследования
Интерес к щелочным металлам существует с давних времен. Уже в древних цивилизациях замечались особенные свойства этих металлов и открылись первые их соединения. Однако, полное понимание и изучение щелочных металлов началось лишь в последние несколько веков.
Одним из первых важных открытий было извлечение искусственного щелочного металла, калия, из его минеральной соли. Это событие произошло в 1807 году благодаря усилиям ученых Джона Дальтона и Хамфри Дэви.(используйте теги )
Последующие исследования позволили расширить знания о свойствах щелочных металлов и их соединений. Были открыты и описаны другие щелочные металлы, такие как натрий, литий, рубидий, цезий и франций. Отдельные качества этих металлов были изучены в деталях, включая их химический состав, физические свойства и возможное применение.(используйте теги )
Одновременно с экспериментами, ученые проводили математические расчеты и создали теоретические модели, которые помогли объяснить некоторые свойства и реакции щелочных металлов. Это позволило попытаться предсказать реакции с другими веществами и использовать щелочные металлы в различных отраслях промышленности.(используйте теги )
С появлением современных методов исследования, таких как спектроскопия, микроскопия и рентгеновская кристаллография, было возможно более детально изучить щелочные металлы и их соединения. Все эти открытия и исследования позволили значительно расширить наши знания о щелочных металлах и использовать их в различных областях науки и технологий.(используйте теги )
Открытие и систематизация щелочных металлов
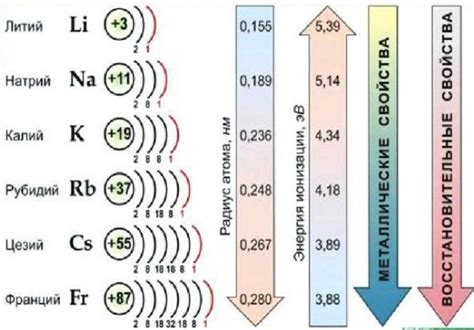
Открытие и систематизация щелочных металлов являются значимыми вехами в развитии химии и науки в целом. Щелочные металлы были открыты в разное время и разными учеными, но только благодаря систематизации и классификации они получили свое место в периодической системе элементов.
Первым из щелочных металлов был открыт калий в 1807 году химиком Хамфри Дэви. Затем исследования продолжили другие ученые, такие как Генри Квиттер, который открыл натрий в 1809 году, и Роберт Баннистер, открывший литий в 1817 году.
Систематизация щелочных металлов проводилась с учетом их химических свойств, электронной конфигурации и химической активности. В результате было установлено, что все щелочные металлы имеют одинаковое число внешних электронов в своей электронной оболочке, что определяет их общие химические свойства.
В периодической таблице элементов щелочные металлы расположены в первой группе, которая также называется "группой 1" или "группой IA". К этой группе относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они обладают высокой реактивностью, легкостью воспламенения, образованием гидроксидов и способностью образовывать ионы, имеющие положительный заряд.
Применение щелочных металлов в повседневной жизни

Щелочные металлы, такие как литий, натрий и калий, имеют широкое применение в повседневной жизни человека. Они находят применение в различных сферах, включая электронику, медицину, промышленность и сельское хозяйство.
Один из наиболее распространенных примеров использования щелочных металлов - это элементы батарей. Литиевые батареи, содержащие литий, используются в широком спектре устройств, от портативных электронных устройств до электрических автомобилей. Благодаря своей высокой энергетической плотности и низкому весу, литиевые батареи обеспечивают эффективное и долговечное электропитание для многих устройств.
Натрий также находит широкое применение в повседневной жизни, особенно в пищевой и химической промышленности. Натрий используется в процессе консервирования пищевых продуктов, чтобы предотвратить разрушение и обеспечить их длительное хранение. Кроме того, натрий используется в производстве множества химических продуктов, включая моющие средства, стекло и мыло.
Калий, в свою очередь, является одним из основных элементов, необходимых для здоровья растений. Он широко используется в сельском хозяйстве в виде удобрений, чтобы обеспечить растения необходимыми питательными веществами. Калий также используется в процессе очистки воды и производства стекла.
Таким образом, щелочные металлы находят множество практических применений в повседневной жизни, более того, они являются неотъемлемой частью современной технологии и индустрии.
Опасности и меры предосторожности при работе с щелочными металлами
Щелочные металлы (в частности, литий, натрий и калий) представляют опасность для здоровья и безопасности при работе с ними. Они обладают высокой реактивностью и могут вызывать серьезные ожоги, токсичные эффекты и реакции с водой.
Одним из основных способов предотвращения опасностей при работе с щелочными металлами является использование защитного снаряжения. Рекомендуется надевать хорошо прокладываемую халат с длинными рукавами, резиновые перчатки, специальную защитную маску для лица и сапоги или непроницаемую обувь.
Необходимо также обеспечить правильное хранение и транспортировку щелочных металлов. Они должны храниться в непроницаемых контейнерах, удаленных от источников огня или тепла. При транспортировке необходимо принимать меры предосторожности, чтобы избежать воздействия влаги, повреждений упаковки или случайного разбрызгивания металлов.
Работникам, занимающимся работой с щелочными металлами, необходимо проводить тренинг по безопасности. Это включает в себя обучение по правилам работы с металлами, опасными свойствами металлов и мерам предосторожности. Также важно знать, как обращаться с аварийными ситуациями, включая загрязнение окружающей среды, пожары или поражение электрическим током.
Важно также соблюдать гигиенические меры при работе с щелочными металлами. После окончания работы необходимо тщательно вымыть руки с мылом и водой. Также рекомендуется регулярно проводить гигиеническое обслуживание рабочего места, очищая его от остатков металлов, пыли или других загрязнений.
В итоге, соблюдение мер предосторожности при работе с щелочными металлами является важным условием для обеспечения безопасности и предотвращения возможных опасностей. Знание правил работы с металлами, использование защитного снаряжения, правильное хранение и обращение с металлами, а также соблюдение гигиенических мер позволяют минимизировать риск производственных происшествий и сохранить здоровье работников.
Бесплатный видеоурок: основы работы с щелочными металлами

Добро пожаловать на бесплатный видеоурок, который поможет вам освоить основы работы с щелочными металлами. Щелочные металлы, такие как литий, натрий и калий, являются важными элементами в химической промышленности и имеют множество практических применений.
В этом видеоуроке вы узнаете о свойствах щелочных металлов, их реакции с водой, кислородом и другими веществами. Вы также узнаете о безопасности работы с этими металлами и правилах их хранения.
Видеоурок будет включать в себя демонстрацию практических экспериментов с щелочными металлами, а также объяснение основных концепций и терминов. Вы сможете лучше понять, как работать с этими металлами и какие меры предосторожности необходимо соблюдать.
По завершении видеоурока вы будете иметь более глубокое представление о щелочных металлах и их использовании в различных областях, а также сможете применить полученные знания на практике.
Вопрос-ответ

Что такое щелочные металлы?
Щелочные металлы - это элементы, принадлежащие к первой группе периодической таблицы: литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они обладают низкой плотностью, мягкостью, высокой реактивностью и химически активны при обычных условиях.
Какие свойства у щелочных металлов?
У щелочных металлов есть несколько общих свойств. Во-первых, они обладают низкой плотностью и малой твердостью, что делает их мягкими и легко режущимися. Во-вторых, они очень реактивны и легко реагируют с водой, кислородом и другими веществами. В-третьих, они имеют низкую температуру плавления и кипения. Кроме того, у них светло-серый металлический блеск и хорошая электропроводность.
Зачем изучать щелочные металлы?
Изучение щелочных металлов важно, потому что они имеют широкое применение в различных областях. Например, натрий используется в производстве стекла, калий - в удобрениях, литий - в аккумуляторах электромобилей. Кроме того, щелочные металлы играют важную роль в химической промышленности и научных исследованиях.
Какие опасности связаны с использованием щелочных металлов?
Щелочные металлы могут быть опасными при неправильном обращении с ними. Они очень реактивны и могут взрываться при контакте с водой или кислородом. Кроме того, они могут вызывать ожоги при контакте с кожей или глазами. Поэтому при работе с щелочными металлами необходимо соблюдать соответствующие меры предосторожности и работать в хорошо проветриваемом помещении.
Где можно найти бесплатные видеоуроки по щелочным металлам?
Бесплатные видеоуроки по щелочным металлам можно найти на различных образовательных платформах и видеохостингах, таких как YouTube. Также некоторые университеты и научные организации предлагают бесплатные онлайн-курсы, включающие видеоуроки по химии и щелочным металлам.
