Оксиды металлов – это химические соединения, состоящие из металлического элемента и кислорода. Они являются основными компонентами множества природных и искусственных материалов.Однако, не все вещества с формулой, содержащей металлический элемент и кислород, относятся к оксидам металлов.
Одной из причин этого является наличие оксидов металлов, которые образуются только с определенными группами металлов, такими как металлы переходных элементов. Например, оксид железа (Fe2O3) является одним из наиболее распространенных оксидов металлов. С другой стороны, оксид алюминия (Al2O3) также является оксидом металла, но не металла переходного периода, алюминия, не относящегося к этой группе металлов.
Кроме того, вещества с формулой, содержащей металлический элемент и кислород, могут относиться к другим классам химических соединений, таким как соли металлов или кислоты. Например, соединения металлов с кислородом, входящие в состав кислот, называются оксокислотами. Они имеют более сложную структуру и выполняют различные функции в химических реакциях.
Оксиды: что это такое?
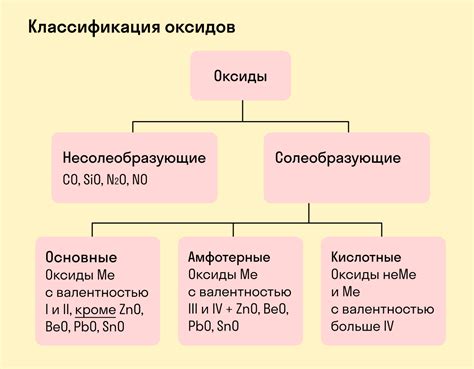
Оксиды – это химические соединения, состоящие из кислорода и других элементов. Формула оксида состоит из символа химического элемента, который соединяется с кислородом. Оксиды широко распространены в природе и высоко реактивны.
Оксиды могут иметь различные свойства в зависимости от элементов, с которыми они соединены. Они могут быть кислородными и некислородными, а также солевыми или некислотными.
Кислородные оксиды содержат кислород в составе и чаще всего обладают кислотными свойствами. Они могут реагировать с водой, образуя кислоты, а также способны образовывать кислотные соединения при взаимодействии с основаниями.
Некислородные оксиды не содержат кислород и могут обладать различными физическими и химическими свойствами. Они часто используются в промышленности и имеют широкий спектр применения.
Солевые оксиды, или основные оксиды, образуют соли при реакции с кислотами. Они могут быть щелочными или амфотерными и обычно обладают щелочными свойствами.
Оксиды являются важными веществами в химии и имеют множество применений. Они используются в производстве металлов, стекла, керамики и других материалов. Некоторые оксиды также используются в медицине, косметике и пищевой промышленности.
Оксиды металлов: особая форма

Оксиды металлов являются важной группой химических соединений. Они образуются при взаимодействии металлов с кислородом. Однако среди оксидов металлов можно выделить особую форму, которая отличается от обычных оксидов. Речь идет об оксидах металлов, у которых формула не соответствует стандартной стехиометрической формуле.
Примером таких оксидов может служить оксид меди(II), чья формула необычна и записывается как Cu2O. Это медный оксид с красноватым оттенком, который получается при взаимодействии меди с кислородом. Его неправильная формула объясняется наличием специфических свойств меди и особыми условиями синтеза данного соединения.
Также можно привести пример другого оксида металла, имеющего нестандартную формулу - оксида железа(III) Fe2O3. По стандартной стехиометрической нотации, оксиды железа записываются как FeO и Fe2O3, однако Formula не соответствует формуле FeO.
Такие необычные оксиды металлов не только представляют научный интерес, но и находят применение в различных отраслях промышленности и научных исследованиях. Например, оксид меди(II) Cu2O используется в качестве полупроводникового материала, а оксид железа(III) Fe2O3 представляет собой одну из разновидностей ржавчины и применяется в производстве красок и пигментов.
Химические свойства оксидов металлов
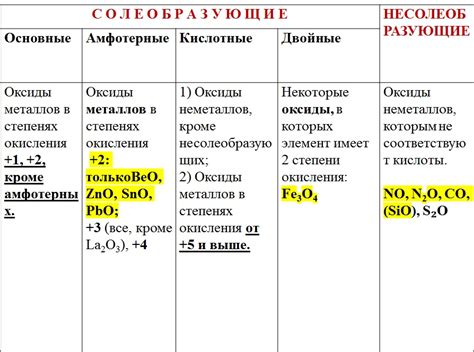
Оксиды металлов представляют собой химические соединения, состоящие из металлической частицы и кислорода. Эти вещества обладают рядом характеристических химических свойств. Например, большинство оксидов металлов обладают основными свойствами, то есть они способны образовывать основные растворы и реагировать с кислотами.
Оксиды металлов также могут проявлять амфотерные свойства, то есть они могут реагировать как с кислотами, так и с основаниями. Это обусловлено наличием в их структуре оксидной группы, которая может образовывать кислотные или основные реакции в зависимости от условий.
Еще одной характеристикой оксидов металлов является их способность образовывать соли при реакции с кислотами. Это связано с реакцией оксидов металлов с кислородом, который является компонентом кислот. При этом образуется соль металла и вода.
Некоторые оксиды металлов могут также образовывать пероксиды при реакции с кислородом. Эти соединения обладают повышенной активностью и могут использоваться в качестве катализаторов или окислителей.
Кроме того, оксиды металлов могут обладать свойствами катализаторов, то есть они могут ускорять химические реакции без участия в них. Это делает оксиды металлов важными компонентами в различных промышленных процессах и химическом производстве.
Способы получения оксидов металлов

Оксиды металлов – это бинарные неорганические соединения, состоящие из металла и кислорода. Они широко используются в различных отраслях промышленности и науке. Оксиды металлов можно получить с помощью нескольких способов, которые будут рассмотрены ниже:
- Термический способ. Этот метод основан на нагревании металла в присутствии кислорода. У многих металлов есть способность реагировать с кислородом при высоких температурах, образуя оксид. Например, при нагревании железа воздухе образуется оксид железа III (Fe2O3). Этот способ широко используется в металлургии.
- Химический способ. В химическом способе получения оксидов металлов используются различные реакции, основанные на взаимодействии металла с кислородом. Например, может быть применена реакция окисления металла в присутствии кислородного перекиси. При этом образуется оксид металла. Этот метод часто используется в лабораторных условиях для получения оксидов металлов в чистом виде.
- Электролиз. Электролиз также может быть использован для получения оксидов металлов. При этом металл окисляется на аноде, а кислород выделяется на катоде. Таким образом, образуется оксид металла. Этот метод активно применяется в электрохимии и позволяет получать оксиды металлов высокой чистоты.
Способ получения оксидов металлов зависит от свойств самого металла и требований к оксиду. Оксиды металлов имеют различные свойства и применяются в разных областях. Например, оксид алюминия используется в производстве керамики, а оксид цинка применяется в производстве лакокрасочных материалов. Поэтому выбор способа получения оксидов металлов играет важную роль в их применении и использовании.
Влияние оксидов металлов на окружающую среду

Оксиды металлов – это химические соединения, состоящие из отрицательно заряженного кислородного и положительно заряженного металлического иона. Они широко распространены в природе и представляют собой важную группу химических веществ. Однако, оксиды металлов могут оказывать негативное влияние на окружающую среду.
Одним из основных негативных последствий присутствия оксидов металлов в окружающей среде является загрязнение воздуха. В результате промышленной деятельности, сгорания топлива и других процессов в атмосферу попадают оксиды серы, азота и другие оксиды металлов. Воздействие этих веществ на организмы живых существ может привести к проблемам с дыхательной системой, включая бронхиты, астму и даже рак легких.
Оксиды металлов также могут загрязнять поверхностные и подземные воды. В результате вымывания из почвы и осадков в окружающих водоемах, оксиды металлов могут накапливаться в воде и создавать опасность для растений и животных. Они могут вступать в реакцию с другими веществами и образовывать токсические соединения, которые могут нанести ущерб экосистемам.
Некоторые оксиды металлов также обладают фитотоксичностью – способностью оказывать негативное воздействие на растения. Так, оксиды свинца и кадмия могут попадать в почву, где они являются источниками тяжелых металлов. Они могут снижать плодородие почвы и мешать росту растений, что в конечном итоге может привести к снижению урожайности и повреждению сельскохозяйственных культур.
Таким образом, оксиды металлов оказывают негативное влияние на окружающую среду. Их присутствие в воздухе, воде и почве может привести к загрязнению экосистем и нанести вред живым организмам. Поэтому, необходимо контролировать выбросы оксидов металлов и разрабатывать способы их утилизации, чтобы минимизировать их негативное воздействие на окружающую среду.
Применение оксидов металлов в промышленности

Оксиды металлов широко применяются в различных отраслях промышленности благодаря своим уникальным свойствам и возможностям. Они используются как основные компоненты в производстве различных материалов и продуктов.
Одним из основных применений оксидов металлов является их использование в производстве керамики и стекла. Например, оксиды алюминия и титана добавляются для придания прочности и термостойкости керамическим изделиям, таким как посуда, изоляционные материалы и строительные элементы. Оксиды железа и хрома используются в стекольной промышленности для получения различных оттенков стекла.
Оксиды металлов также широко применяются в производстве красок и лаков. Некоторые оксиды металлов имеют яркие и стойкие цвета, что делает их отличным выбором для получения различных оттенков красок. Например, оксид железа используется для получения коричневого и красного цветов, а оксид титана - для получения белого цвета. Оксиды металлов также обладают хорошими адгезионными свойствами, что позволяет им стойко удерживаться на поверхностях и сохранять яркость цвета.
Оксиды металлов применяются также в качестве катализаторов в различных химических процессах. Они способны активировать реакции, ускоряя их протекание и улучшая химическую эффективность. Некоторые оксиды металлов, например, оксид цинка и оксид меди, используются в производстве синтетических материалов, пластиков и резиновых изделий. Оксиды таких металлов, как рутений и иридий, применяются в процессах глубокого каталитического окисления в промышленности очистки отходов и загрязнений.
Оксиды металлов также имеют широкое применение в электронике и электротехнике. Они используются как проводники электричества и материалы для изготовления различных электронных компонентов. Некоторые оксиды металлов обладают полупроводниковыми свойствами и используются в производстве полупроводниковых приборов, таких как диоды и транзисторы.
Из всего вышесказанного можно сделать вывод о значимости и разнообразии применения оксидов металлов в промышленности. Они не только служат основой для производства различных материалов, но и играют важную роль в электротехнике и химической промышленности, обеспечивая эффективность и надежность процессов.
Вопрос-ответ

Какие вещества относятся к оксидам металлов?
Оксиды металлов – это соединения, состоящие из металла и кислорода. Такие вещества обладают характерной формулой, в которой металл обозначается символом, а кислород - O. Примерами таких веществ являются оксиды железа (FeO), оксиды алюминия (Al2O3), оксиды меди (CuO) и др.
Какие вещества не относятся к оксидам металлов?
Не относятся к оксидам металлов вещества, которые не обладают характерной формулой металла и кислорода. Например, соль (NaCl), которая состоит из натрия и хлора, или вода (H2O), состоящая из водорода и кислорода, не являются оксидами металлов. В состав оксидов металлов не входят также кислоты и основания.
