Щелочные металлы – это группа химических элементов, которые входят в первую группу периодической системы элементов. К ним относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они названы так из-за своего способности образовывать водород (щелочь), когда они реагируют с водой.
Свойства щелочных металлов:
- Металлический блеск: щелочные металлы имеют яркий металлический блеск на свежем воздухе.
- Мягкость и низкая плотность: они очень мягкие и имеют низкую плотность, что делает их легкими для обработки и формовки.
- Высокая реактивность: щелочные металлы являются очень реактивными и быстро соединяются с другими элементами или соединениями.
- Хорошие проводники электричества: они обладают высокой электропроводностью и широко используются в электронике и электротехнике.
Применение щелочных металлов:
Щелочные металлы имеют широкое применение в различных отраслях промышленности и научных исследованиях. Натрий широко используется в промышленности пищеварения, производстве стекла, металлургии и производстве щелочей. Калий находит применение в сельском хозяйстве в качестве удобрений, а также в производстве игральных карт и взрывчатых веществ. Литий используется в производстве литий-ионных аккумуляторов, а также в производстве стекла и керамики. Рубидий, цезий и франций находят применение в научных исследованиях и в различных электронных устройствах.
Щелочные металлы играют важную роль в нашей жизни, они находят применение не только в научных исследованиях, но и в различных отраслях промышленности. Благодаря своим уникальным свойствам и распространенности, они широко используются и имеют большой потенциал в будущих технологиях и разработках.
Химические свойства щелочных металлов
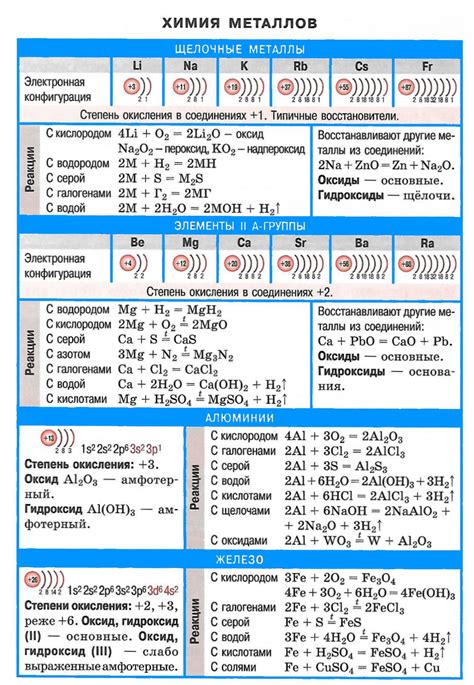
Щелочные металлы - это группа химических элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они относятся к первой группе периодической системы элементов и характеризуются высокой химической активностью.
Щелочные металлы имеют относительно низкую температуру плавления и кипения, что делает их мягкими и легкоплавкими. Они обладают высокой электроотрицательностью, что делает их реактивными в отношении воды и кислорода.
Химические свойства щелочных металлов проявляются в их способности образовывать ионы положительного заряда при химических реакциях. Они легко отдают свой внешний электрон, образуя ионы с однозарядным положительным зарядом.
Одной из основных химических реакций щелочных металлов является их реакция с водой. При контакте с водой щелочные металлы образуют гидроксиды и выделяются водород. Например, натрий реагирует с водой, образуя гидроксид натрия (NaOH) и выделяя водородный газ (H2).
Щелочные металлы также активно реагируют с кислородом, образуя оксиды. Например, литий сгорает в кислороде, образуя оксид лития (Li2O).
Щелочные металлы широко используются в различных промышленных процессах. Натрий и калий, например, являются необходимыми элементами в составе пищевых продуктов и используются в пищевой промышленности. Калий также является важным компонентом удобрений. Литий используется в производстве аккумуляторов и лекарственных препаратов. Рубидий и цезий находят применение в научных исследованиях и в технологии языков.
Применение щелочных металлов в различных отраслях

Щелочные металлы, такие как литий, натрий и калий, находят широкое применение в различных отраслях нашей жизни благодаря своим уникальным свойствам.
Электроэнергетика: Литий используется в производстве литий-ионных аккумуляторов, которые являются одними из самых эффективных и перспективных источников электроэнергии. Калий и натрий используются в создании щелочных аккумуляторов, которые нашли широкое применение в беспроводных устройствах.
Металлургия: Натрий и калий широко применяются в металлургической промышленности как восстановительные агенты при профессиональной обработке металлов. Они также используются в создании сплавов и легировании различных металлов, повышая их прочность и стойкость к коррозии.
Химическая промышленность: Щелочные металлы являются важными ингредиентами при производстве щелочей, каустических сод и других химических соединений. Они также используются в качестве катализаторов и реагентов во многих химических процессах, таких как производство биодизельного топлива и синтез органических соединений.
Фармацевтическая и медицинская промышленность: Литий применяется в фармацевтической промышленности для производства лекарств от биполярного расстройства и депрессии. Калий используется в медицине для поддержания нормального уровня электролитов в организме и для лечения сердечной недостаточности.
Стекольная и керамическая промышленность: Щелочные металлы используются в производстве стекла и керамики для повышения стойкости и прозрачности материалов. Они также улучшают электропроводность и теплопроводность, делая их идеальными для применения в электронике и электротехнике.
Нефтегазовая промышленность: Калий широко используется в буровых растворах для поддержания стабильности геологических структур и защиты стенок скважин от обрушений. Кроме того, натрий используется в процессе очистки газа и нефти от серы.
Щелочные металлы безусловно имеют огромное значение в многих отраслях промышленности и науке, что делает их незаменимыми компонентами нашей современной жизни.
Вопрос-ответ

Каково определение щелочных металлов?
Щелочные металлы – это группа элементов, которые входят в первую группу периодической системы. К ним относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Щелочные металлы характеризуются тем, что они образуют гигроскопичные оксиды и гидроксиды, обладают низкой плотностью и низкой температурой плавления, а также обладают химической активностью.
Каковы свойства щелочных металлов?
Свойства щелочных металлов включают в себя низкую плотность, низкую температуру плавления, мягкость, металлический блеск, химическую активность и способность образовывать ионы с положительным зарядом. Они также хорошо проводят тепло и электричество. Кроме того, щелочные металлы образуют гигроскопичные оксиды и гидроксиды и реагируют с водой, выделяя гидроген.
Каковы основные применения щелочных металлов?
Щелочные металлы имеют широкий спектр применения. Натрий широко используется в пищевой промышленности, производстве мыла и стекла, а также в качестве охлаждающего вещества в некоторых реакторах ядерных электростанций. Калий применяется в сельском хозяйстве в качестве удобрения, а также в производстве стекла и медикаментах. Литий используется в производстве легких сплавов и аккумуляторов. Рубидий и цезий находят применение в науке и технике, например, в оптических приборах и атомных часах.
Что происходит при взаимодействии щелочных металлов с водой?
При взаимодействии щелочных металлов с водой происходит реакция, в результате которой образуется гидроксид металла и выделяется водород. Например, натрий реагирует с водой, образуя гидроксид натрия и выделяя водород. Эта реакция является очень бурной и сопровождается выделением тепла.
