Металлы - это химические элементы, которые обладают высокой электропроводностью и металлическим блеском. Они широко используются в различных отраслях промышленности, строительства и электротехники. Важной характеристикой металлов является их способность образовывать соединения с кислотными оксидами.
Кислотные оксиды - это соединения, образованные в результате реакции кислоты с кислородом. Они обладают выраженной кислотностью и способностью взаимодействовать с щелочными оксидами и гидроксидами. Когда кислотный оксид реагирует с металлом, образуется соль, которая имеет свои уникальные физические и химические свойства.
Примерами веществ, образованных в результате взаимодействия металлов с кислотными оксидами, являются сульфиды металлов, нитриды металлов, карбиды металлов и многое другое. Каждое из этих веществ имеет свою особенную структуру и свойства. Сульфиды металлов, например, широко используются в производстве различных материалов и электроники, благодаря своим полупроводниковым свойствам.
Вещества металлы с кислотными оксидами имеют большую практическую значимость во многих областях деятельности человека. Изучение их свойств позволяет разрабатывать новые материалы, повышать эффективность процессов производства и создавать новые технологии. Поэтому изучение взаимодействия металлов с кислотными оксидами является важной задачей современной науки и техники.
Оксиды металлов в кислотах: основные свойства и классификация
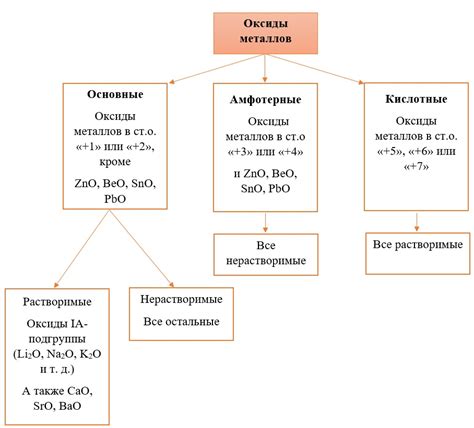
Оксиды металлов в кислотах являются важными соединениями, которые обладают своеобразными свойствами. Они образуются при соединении оксида металла с кислотой и играют важную роль в химических реакциях и промышленности.
Главным свойством оксидов металлов в кислотах является их способность реагировать с основаниями, образуя соли. Это основополагающее свойство и классификационный признак для данных соединений.
Оксиды металлов в кислотах могут быть классифицированы в соответствии с некоторыми основными характеристиками. Одним из основных критериев является способность оксида металла растворяться в воде. По этому признаку оксиды можно разделить на гидроксоксиды (растворимые в воде) и несолубильные оксиды.
Другим критерием классификации оксидов металлов в кислотах является их реакционная активность. Существуют оксиды, которые обладают высокой активностью и легко реагируют с различными кислотами, в то время как некоторые оксиды являются менее активными и могут оставаться неизменными в присутствии кислоты.
Таким образом, оксиды металлов в кислотах обладают разнообразными свойствами и представляют собой важные соединения в химии и промышленности. Изучение этих свойств позволяет лучше понять особенности их взаимодействия с другими веществами и использовать их в различных сферах деятельности.
Вещества с кислотными оксидами: примеры и применение
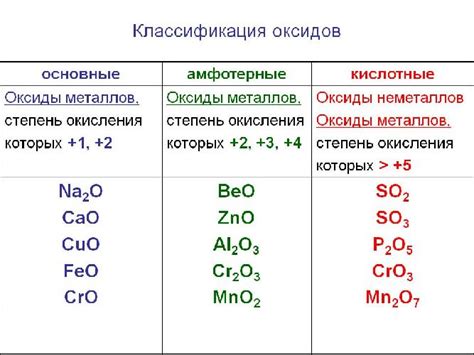
Кислотные оксиды – это оксиды, которые образуются при взаимодействии кислот с кислородом. Они имеют высокую кислотность и часто выступают в качестве основных компонентов различных химических соединений.
Одним из наиболее известных и широко применяемых кислотных оксидов является серный оксид (SO2). Он образуется при сгорании серы и применяется в производстве серной кислоты, в процессе десульфурации газов, а также в качестве дезинфицирующего средства и консерванта.
Еще одним примером кислотного оксида является углеродный диоксид (CO2). Он образуется при сгорании углерода и применяется для создания газового эффекта в безалкогольных напитках, в процессе дыхания растений и животных, а также в качестве огнетушителя.
Кроме того, кислотные оксиды применяются в процессе производства стекла, цемента, керамики, металлургии и других отраслях промышленности. Они активно используются для установления кислотности и алкальности различных сред, а также для получения различных химических соединений.
- Серный оксид (SO2)
- Углеродный диоксид (CO2)
- Азотный оксид (NO)
- Фосфорный пентоксид (P2O5)
- Кремниевый диоксид (SiO2)
В результате, вещества с кислотными оксидами широко используются в различных отраслях промышленности и находят применение в обычной жизни.
Свойства металлических оксидов: электропроводность и термоустойчивость
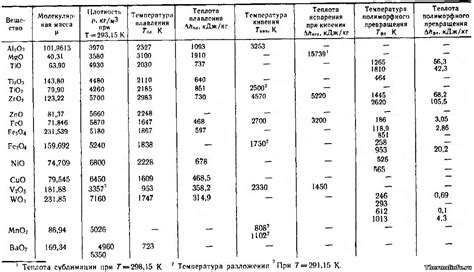
Электропроводность является одним из наиболее важных свойств металлических оксидов. Металлы обладают высокой электропроводностью благодаря свободным электронам в их структуре. Оксиды металлов, образованные из соответствующих металлов и кислорода, сохраняют эти свойства, поскольку содержат свободные электроны. Это позволяет им проводить электрический ток, делая их полезными в различных областях, таких как электроника, электротехника и энергетика.
Термоустойчивость также является важным свойством металлических оксидов. Металлические оксиды обычно обладают высокой степенью термоустойчивости, что означает, что они способны выдерживать высокие температуры без деградации или разрушения структуры. Это делает металлические оксиды идеальными для использования в условиях высоких температур, таких как при производстве стали или в качестве катализаторов в химических процессах. Кроме того, термоустойчивость металлических оксидов может помочь им сохранять свои электропроводящие свойства даже при высоких температурах.
Металлы и их оксиды: влияние на окружающую среду и здоровье

Металлы и их оксиды играют существенную роль во взаимодействии с окружающей средой и здоровьем человека. Оксиды металлов, такие как оксиды железа, алюминия, меди и других, выполняют различные функции в природе. Они могут быть как естественными, так и искусственно созданными.
Взаимодействие оксидов металлов с окружающей средой основано на их химических свойствах. Например, оксиды железа активно взаимодействуют с влажным воздухом, приводя к образованию ржавчины. Это явление негативно влияет как на внешний вид окружающей среды, так и на структуру и прочность различных металлических конструкций.
Влияние оксидов металлов на здоровье человека может быть как положительным, так и отрицательным. Некоторые металлы и их соединения используются в медицине в качестве лекарственных препаратов. Например, оксид магния применяется в качестве желудочных антацидов, а оксид цинка используется в лечении различных кожных заболеваний.
Однако, неконтролируемое воздействие на окружающую среду и длительный контакт с некоторыми оксидами металлов могут иметь негативные последствия для здоровья человека. Некоторые оксиды металлов являются ядовитыми и могут вызывать различные заболевания, такие как рак, нервные расстройства и проблемы с дыхательной системой. Поэтому, строгий контроль и соответствующие меры предосторожности необходимы при работе с металлами и их оксидами для минимизации вредного воздействия на окружающую среду и здоровье человека.
Перспективы использования металлов с кислотными оксидами в промышленности

Металлы с кислотными оксидами представляют собой класс веществ, обладающих уникальными свойствами и широким спектром применения в промышленности. Одним из наиболее перспективных направлений использования этих веществ является их применение в качестве катализаторов.
Катализаторы на основе металлов с кислотными оксидами имеют высокую активность и стабильность, что делает их идеальными для использования в реакциях, протекающих в агрессивных условиях. Они могут быть использованы в различных отраслях промышленности, включая нефтехимию, органическое синтез и фармацевтику.
Способность металлов с кислотными оксидами взаимодействовать с различными соединениями позволяет использовать их для очистки воды и воздуха от загрязняющих веществ. Они могут превращать токсичные соединения в безопасные или удалять их с поверхности материалов. Такое применение металлов с кислотными оксидами особенно актуально в условиях растущей экологической проблематики.
Еще одним перспективным направлением использования металлов с кислотными оксидами является их применение в производстве энергетических устройств. Они могут служить материалами для создания электродов батарей, суперконденсаторов и солнечных элементов. Благодаря своим уникальным электрохимическим свойствам, эти материалы могут повысить эффективность и долговечность энергетических устройств.
В целом, металлы с кислотными оксидами представляют огромный потенциал для развития промышленности. Их уникальные свойства позволяют использовать их в широком спектре областей, от катализа до энергетики. Развитие и исследования в этой области могут привести к созданию новых технологий и материалов, способных решить множество современных проблем и повысить уровень развития общества.
Вопрос-ответ

Какие металлы могут образовывать кислотные оксиды?
Среди металлов, которые могут образовывать кислотные оксиды, можно назвать такие элементы, как медь, железо, свинец, цинк, никель, марганец и другие.
Что такое кислотные оксиды?
Кислотные оксиды – это неорганические соединения, состоящие из металла и кислорода. Они обладают кислотными свойствами и способны реагировать с водой, образуя кислоты.
Какие свойства имеют кислотные оксиды?
Кислотные оксиды обладают следующими свойствами: они растворяются в воде, образуя кислоты, реагируют с щелочами, нейтрализуя их, могут реагировать с солями, образуя соли и воду, и т.д.
Какие примеры металлов, образующих кислотные оксиды?
Примеры металлов, которые образуют кислотные оксиды, включают медь (CuO), железо (Fe2O3), цинк (ZnO), свинец (PbO) и другие.
В чем заключается роль кислотных оксидов в химических реакциях?
Кислотные оксиды играют важную роль в различных химических реакциях. Они могут служить источником кислорода для горения, а также участвовать в реакциях нейтрализации с щелочами и солями.
