Металлы являются одной из основных групп элементов в периодической таблице химических элементов. Каждый металл обладает своими уникальными свойствами, которые определяют его активность в химических реакциях. Активность металлов может быть определена по их способности образовывать ионы и вступать в реакции с другими веществами.
Периодическая таблица является графическим представлением всех элементов, из которых состоит наш мир. В таблице элементы расположены в порядке возрастания их атомного номера. Металлы в периодической таблице расположены слева от ступенчатой линии, которая разделяет металлы и неметаллы.
Активность металлов возрастает с увеличением их положения в периодической таблице. Самыми активными металлами являются щелочные металлы - литий, натрий, калий и др. Они вступают в реакции с водой и кислородом, образуя ионы и соли. Менее активные металлы, такие как цинк, железо и магний, образуют соли только с некоторыми кислотами и не реагируют с водой.
Активность металлов играет важную роль в промышленности и науке. Металлы используются во множестве отраслей, включая строительство, электротехнику, автомобильную промышленность и т.д. Понимание активности металлов позволяет предсказывать их поведение в реакциях и разработывать новые материалы и технологии.
Активность металлов в таблице: основные характеристики

Активность металлов - это способность металла образовывать соединения с другими веществами. Она определяется электрохимическим потенциалом металла и показывает его склонность к окислению или восстановлению.
В таблице активности металлов по убыванию электрохимического потенциала металлы расположены в определенном порядке. Чем выше металл на таблице, тем большую активность он проявляет. Топ активных металлов включает литий, натрий, калий, магний, алюминий, цинк, железо, свинец, медь и серебро.
Активные металлы имеют высокую способность к окислению. Они легко отдают электроны и реагируют с кислородом, образуя оксиды. В свою очередь, неактивные металлы имеют низкую активность и реагируют с кислородом только при высоких температурах.
Активность металлов определяет их способность реагировать с кислотами. Например, активные металлы реагируют с кислыми веществами, образуя соли и выделяя водород. Неактивные металлы практически не реагируют с кислотами и не образуют солей.
Активность металлов также связана с их способностью быть анодами или катодами в электрохимических процессах. Активные металлы обычно выступают в качестве анодов и подвергаются коррозии. Неактивные металлы, напротив, могут использоваться в качестве катодов и не подвергаться коррозии.
Первый ряд таблицы Менделеева: анализ активности металлов

Первый ряд таблицы Менделеева содержит ряд металлов, которые отличаются высокой активностью. В этом ряду находятся литий, бериллий, гидроген и другие элементы. Активность металлов определяется их способностью вступать в химические реакции и образовывать соединения.
Наиболее активным металлом в первом ряду является литий. Он обладает высокой реакционной способностью и быстро вступает в реакцию с водой или кислородом. Бериллий, расположенный дальше по ряду, также обладает высокой активностью, хотя несколько ниже, чем у лития.
Активные металлы первого ряда обладают свойствами, которые делают их полезными в различных отраслях промышленности. Например, литий используется в производстве легких аккумуляторов и лекарственных препаратов. Бериллий применяется в электронике и аэрокосмической промышленности благодаря своим высоким термическим и электрическим свойствам.
Однако высокая активность металлов первого ряда также может приводить к их реакции с окружающей средой, что может вызывать опасность. Например, литий может вступать во взаимодействие с водой воздуха и образовывать взрывоопасные газы. Поэтому при работе с этими металлами необходимо соблюдать особые меры предосторожности и работать в соответствии с инструкциями и правилами безопасности.
Активные металлы: свойства и химическая реактивность
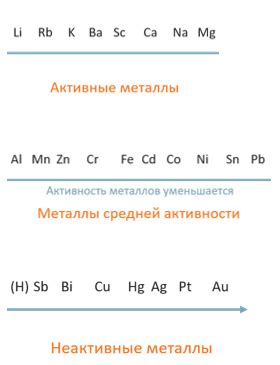
Активные металлы – это элементы, которые легко вступают в химические реакции с другими веществами. Они обладают высокой химической активностью и обычно находятся в левой части периодической системы.
Основные свойства активных металлов – высокая электроотрицательность, низкая ионизационная энергия и хорошая проводимость электричества и тепла. Эти свойства обуславливают их способность активно вступать в реакции с кислотами, водой, кислородом и другими веществами.
Активные металлы реагируют с кислородом, образуя основные оксиды. Например, натрий горит в контакте с воздухом, образуя натриевый оксид. Они также реагируют с водой, выделяя водород. При этом некоторые активные металлы очень реактивны и могут вступать в реакцию с водой даже с выделением пламени и выбросом веществ.
Активные металлы также образуют соли при реакции с кислотами. Например, натрий реагирует с соляной кислотой, образуя хлорид натрия и выделяя водород. Эта реакция является одной из основных реакций активных металлов.
Важно отметить, что активные металлы могут быть опасны для работы с ними из-за их реактивности. Их необходимо хранить в специальных условиях и обращаться с ними с осторожностью.
Неактивные металлы и их значимость в промышленности

Неактивными металлами называются элементы таблицы, которые обладают низкой активностью и не реагируют с водой или кислотами при обычных условиях. В промышленности эти металлы играют важную роль благодаря своим уникальным свойствам.
Одним из наиболее известных неактивных металлов является золото. Этот благородный металл обладает высокой устойчивостью к окружающей среде и химическим веществам, что делает его незаменимым материалом для ювелирной промышленности. Золото также используется в электронике, медицине и научных исследованиях.
Серебро - еще один неактивный металл, который имеет широкое применение в промышленности. Оно отличается высокой тепло- и электропроводностью, что делает его незаменимым материалом для производства электроники, фото- и видеоаппаратуры, а также вариантами бижутерии. Кроме того, серебро имеет антибактериальные свойства и используется для производства медицинского оборудования и инструментов.
Платина, несмотря на свою высокую стоимость, является незаменимым материалом в химической и автомобильной промышленности. Она обладает высокой устойчивостью к коррозии и высокой температурой плавления, что делает ее идеальным материалом для производства катализаторов, электродов и других высокотехнологичных продуктов.
Также важным неактивным металлом является свинец. Он используется в производстве аккумуляторов, кабельных оболочек и печатных плат благодаря своей высокой плотности и устойчивости к коррозии.
В заключение, неактивные металлы играют значимую роль в промышленности, обеспечивая надежность, высокую эффективность и долговечность в различных областях производства. Их уникальные свойства делают их незаменимыми материалами для создания разнообразных продуктов.
Переходные металлы: особенности и применение

Переходные металлы являются группой элементов, которые занимают центральное положение в таблице периодических элементов. Они имеют свои особенности, которые делают их уникальными и важными для различных промышленных и химических процессов.
Особенностью переходных металлов является наличие неполного заполнения внешней оболочки электронов. Это позволяет им образовывать различные степени окисления и образовывать соединения с другими элементами. Они также обладают высокой термической и электрической проводимостью.
Использование переходных металлов широко распространено в различных отраслях промышленности и науке. Например, многие переходные металлы используются в качестве катализаторов, которые активируют и ускоряют химические реакции. Они также применяются в производстве сплавов, которые обладают высокой прочностью и стойкостью к коррозии.
Некоторые переходные металлы, такие как железо, медь и никель, широко используются в производстве металлических изделий, электроники, автомобилей, строительства и многих других областях. Они также являются важными элементами для биологических систем, таких как гемоглобин и ферменты.
В целом, переходные металлы играют важную роль в современной промышленности и науке. Их многообразие и уникальные свойства делают их незаменимыми для различных технологических процессов и разработок новых материалов и соединений.
Платиновые металлы и их роль в современных технологиях

Платиновые металлы - это группа химических элементов, которые включают в себя платину, палладий, родий, иридий, рутений и осмий. Они являются одной из самых ценных групп металлов и представляют большой интерес в современных технологиях.
Платина, палладий и родий широко применяются в катализе, особенно в автомобильной промышленности, где они используются в выхлопных системах для снижения выбросов вредных веществ в атмосферу. Благодаря своей химической активности, платиновые металлы могут ускорять химические реакции, что делает их незаменимыми в процессе очистки отработавших газов.
Иридий, рутений и осмий, в свою очередь, обладают особыми свойствами, которые делают их непременными компонентами в современных электронных устройствах. Эти металлы применяются в создании электродов, сенсоров, покрытий и других элементов, которые являются ключевыми в электронных устройствах, таких как телефоны, компьютеры, планшеты и прочие гаджеты.
Кроме того, платиновые металлы играют важную роль в производстве ювелирных изделий, где они используются в качестве основного материала для создания эксклюзивных украшений. Высокая прочность и красота этих металлов делают их очень ценными и популярными среди ювелиров и покупателей.
В целом, платиновые металлы являются неотъемлемой частью современных технологий и находят широкое применение в различных областях. Их уникальные свойства и высокая ценность делают их незаменимыми компонентами во многих процессах и изделиях, которые мы используем ежедневно.
Уникальная активность металлов в органической химии

Металлы играют важную роль в органической химии благодаря своей уникальной активности. Они способны участвовать во множестве реакций и образовывать стабильные соединения с органическими молекулами.
Одним из примеров уникальной активности металлов является их способность катализировать различные реакции. Металлические катализаторы широко используются в промышленности и лабораториях для ускорения химических превращений. Такие реакции включают гидрирование, окисление, гидролиз и другие.
Другой важной особенностью металлов в органической химии является их способность образовывать координационные связи с органическими молекулами. Такие связи играют роль в реакциях, связанных с выделением или приобретением электрона. Например, металлы могут образовывать координационные соединения с аминокислотами, нуклеиновыми кислотами и другими органическими молекулами.
Металлы также проявляют свою активность в органической химии через способность образовывать комплексы с органическими соединениями. У металлов существует большое разнообразие органических комплексов, которые обладают различными свойствами и используются в различных областях, включая катализ, медицину и материаловедение.
Влияние внешних условий на активность металлов в реакциях

Активность металлов в реакциях может существенно зависеть от внешних условий, в которых происходят эти реакции. Одним из важных факторов, влияющих на активность металлов, является температура окружающей среды. Многие металлы проявляют большую активность при повышенных температурах, поскольку реакции протекают быстрее и с большей интенсивностью.
Другим важным фактором, влияющим на активность металлов, является концентрация реагентов. Если концентрация металла в реакционной смеси низкая, то скорость реакции может быть недостаточно высока, и реакция будет протекать медленно. В случае, если концентрация металла высока, реакция будет проходить более интенсивно.
Еще одним фактором, который может влиять на активность металлов, является наличие катализаторов. Некоторые существуют реакции, в которых активность металлов значительно увеличивается при наличии определенного катализатора. Катализаторы могут изменять характер и скорость процессов, участвующих в реакциях металлов.
Кроме того, активность металлов может зависеть от pH среды. Некоторые металлы проявляют большую активность в кислой среде, другие – в щелочной. Таким образом, изменение pH среды может значительно влиять на скорость и характер реакций металлов.
Вопрос-ответ

Какие металлы считаются активными в таблице?
Активными считаются металлы, которые имеют склонность к химическим реакциям. Обычно это элементы в левой части таблицы по форме Менделеева, такие как натрий, калий, магний и т. д.
Как активность металлов влияет на их реакцию с кислородом?
Активные металлы, такие как натрий или калий, имеют высокую склонность к реакции с кислородом. Они быстро окисляются и образуют оксиды металлов. Некоторые металлы, такие как золото или платина, менее активны и практически не реагируют с кислородом.
Какие факторы влияют на активность металлов?
Активность металлов зависит от нескольких факторов, включая электроотрицательность, размер атома и структуру кристаллической решетки металла. Чем ниже электроотрицательность металла, тем более он активен. Более маленькие металлические атомы также обычно более активны, чем более большие атомы. Кроме того, структура кристаллической решетки металла может влиять на его активность.
