Валентность металлов - это число, обозначающее количество электронов, которое металл может потерять или добавить при реакции. Это одно из основных понятий в химии, особенно в 8 классе. Знание валентности металлов позволяет понять, какие ионы металлов образуются в химических реакциях и как эти реакции протекают.
Валентность металлов определяется на основе их электронной конфигурации. Если у атома металла образуется ион с положительным зарядом (катион), то валентность металла равна числу электронов, которые атом теряет. Например, если металл образует ион с зарядом +2, то его валентность равна 2. Если же атом металла образует ион с отрицательным зарядом (анион), то его валентность равна количеству электронов, которые атом получает. Например, если металл образует ион с зарядом -3, то его валентность равна -3.
Например, железо имеет валентность +2 и +3. Это значит, что атом железа может потерять 2 или 3 электрона при реакции. Магний имеет валентность +2, что означает, что атом магния может потерять 2 электрона. Алюминий имеет валентность +3, что означает, что атом алюминия может потерять 3 электрона.
Валентность металлов
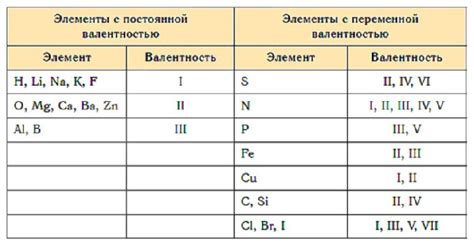
Валентность металлов - это способность металлов образовывать ионные соединения путем отдачи электронов. Она характеризуется числом электронов, которые металл может отдать или принять при образовании соединения.
Валентность металла может быть как постоянной, так и переменной. Постоянная валентность означает, что металл вступает в соединение, отдавая или принимая определенное количество электронов, например, медь всегда имеет валентность +2. Переменная валентность означает, что металл может образовывать несколько типов ионов с разной валентностью.
Например, железо может иметь валентность +2 и +3. В соединении с кислородом оно может образовывать ионы Fe2+ и Fe3+. Алюминий может иметь валентность +3 и образовывать соединения с ионами Al3+.
Валентность металлов определяется по их месту в периодической таблице. Металлы в левой части таблицы имеют положительную валентность, так как они отдают электроны. Металлы в правой части таблицы могут иметь и положительную, и отрицательную валентность, так как они и отдают, и принимают электроны.
Знание валентности металлов позволяет предсказывать их способность образовывать соединения и понимать их свойства и химическую активность.
Основные понятия
Валентность металлов в химии это показатель количества электронов, участвующих в химических реакциях элемента. Валентность металлов может быть положительной или отрицательной, в зависимости от их способности отдавать или принимать электроны. Валентность металлов обычно определяется по степени окисления элемента.
Валентность металлов играет важную роль в образовании химических связей и соединений. Металлы с положительной валентностью могут образовывать ионные соединения, в которых они отдают электроны и образуют положительно заряженные ионы, называемые катионами.
Например, металлом с валентностью +2 является железо. В реакциях с кислородом железо отдает два электрона, образуя положительно заряженный ион Fe2+. В реакциях с серой, железо также отдает два электрона, образуя ион Fe2+.
Металлы с отрицательной валентностью могут образовывать соединения, в которых они принимают электроны и образуют отрицательно заряженные ионы, называемые анионами.
Например, металлом с валентностью -3 является алюминий. В реакциях с кислородом алюминий принимает три электрона, образуя отрицательно заряженный ион Al3-. В реакциях с хлором, алюминий также принимает три электрона, образуя ион Al3-.
Примеры в химии 8 класс
В химии 8 класса учащиеся изучают различные примеры валентности металлов. Валентность металла определяется по его способности участвовать в химических реакциях и образовании химических связей.
Например, железо (Fe) имеет валентность 2 и 3. Это означает, что оно может образовывать двойные или тройные химические связи соответственно. Железо находится во многих соединениях, таких как оксиды, гидроксиды и соли.
Еще один пример - алюминий (Al) с валентностью 3. Алюминий широко используется в промышленности и находится во многих соединениях, включая сульфаты, хлориды и оксиды.
Также важным примером является медь (Cu) с валентностью 1 и 2. Медь используется в производстве электротехнических изделий и находится во многих соединениях, таких как купруманганит и медные сульфаты.
Ртуть (Hg) - еще один пример металла с переменной валентностью. Она может иметь валентность 1 и 2. Ртути используется в лаборатории, в качестве амальгамы и в некоторых клапанах и подшипниках.
Эти примеры демонстрируют взаимосвязь между валентностью металлов и их химическими свойствами, а также показывают, как металлы могут образовывать различные химические соединения.
Вопрос-ответ

Что такое валентность металлов в химии?
Валентность металлов в химии - это способность атома металла образовывать химические связи. Она показывает, сколько электронов может отдать металл при образовании связи с другими атомами. Она указывает на количество электронов во внешней оболочке атома металла и является основным свойством, влияющим на химическую активность металла.
Как определить валентность металлов?
Валентность металлов можно определить, исходя из их положения в таблице Менделеева и электронной конфигурации атомов. Если последняя цифра в номере группы металла совпадает с числом электронов во внешней оболочке, то это и будет его валентность. Например, у натрия (Na) внешняя оболочка состоит из одного электрона, поэтому его валентность равна 1.
Какие примеры можно привести для пояснения валентности металлов?
Примером металла с валентностью 1 может служить натрий (Na). Он имеет всего один электрон во внешней оболочке. Примером металла с валентностью 2 может быть магний (Mg), у которого внешняя оболочка состоит из двух электронов. Для металла с валентностью 3 можно взять алюминий (Al), у которого внешняя оболочка содержит три электрона.
Влияет ли валентность на химическую активность металлов?
Да, валентность металлов имеет прямое влияние на их химическую активность. Чем выше валентность металла, тем более активным он является. Металлы с низкой валентностью обычно имеют меньшую химическую активность и могут образовывать стабильные соединения, а металлы с высокой валентностью могут образовывать более нестабильные соединения и проявлять большую активность.
Может ли у металлов быть разная валентность?
Да, у металлов может быть разная валентность. Она может изменяться в зависимости от условий и соединений, с которыми металл взаимодействует. Например, железо (Fe) может иметь валентность 2+ или 3+, а свинец (Pb) может иметь валентность 2+ или 4+. Это связано с тем, что металлы могут отдавать разное количество электронов при образовании связей с другими атомами.
