Металлы обладают уникальными свойствами, которые делают их неотъемлемой частью нашей жизни. Однако, при контакте с окружающей средой, металлы могут вступать в различные химические реакции, которые приводят к их окислению или коррозии. В данной статье мы рассмотрим уравнения взаимодействия металлов с кислородом воды и кислотами, а также их последствия для металлических изделий и сооружений.
Вода, являясь обычным растворителем, может взаимодействовать с металлами и вызывать их окисление. Когда металл контактирует с водой, между ними происходит электрохимическая реакция. Реакция окисления металла в воде может быть представлена следующим уравнением:
2M + 2H2O → 2MOH + H2
Где M - металл, MOH - гидроксид металла, H2 - молекула водорода. Эта реакция приводит к образованию гидроксида металла и выделению водорода.
Кроме воды, металлы также могут взаимодействовать с кислотами. Кислоты содержат ионы водорода (H+), которые образуются при диссоциации кислоты в воде. При контакте с металлами, гидроксиды металлов образуются из-за реакции между ионами водорода и металлами. Например, уравнение взаимодействия алюминия с соляной кислотой может быть представлено:
2Al + 6HCl → 2AlCl3 + 3H2
Где Al - алюминий, HCl - соляная кислота, AlCl3 - хлорид алюминия, H2 - молекула водорода. При этой реакции происходит образование хлорида алюминия и выделение водорода.
Уравнения металлов с кислородом воды
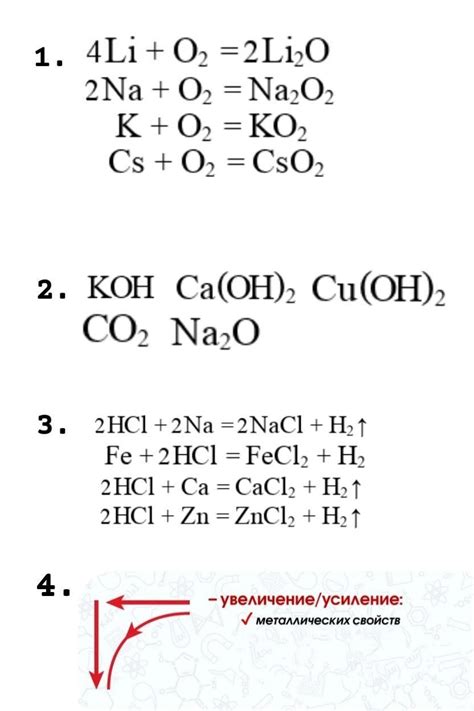
Металлы имеют способность вступать во взаимодействие с кислородом воды, образуя оксиды металлов. Это химические реакции, которые играют важную роль в различных процессах, начиная от коррозии металлов до получения водорода.
Уравнения реакций металлов с кислородом воды могут быть представлены следующим образом:
- Алюминий (Al) + кислород (O2) + вода (H2O → оксид алюминия (Al2O3)
- Железо (Fe) + кислород (O2) + вода (H2O) → оксид железа (Fe2O3)
- Магний (Mg) + кислород (O2) + вода (H2O) → гидроксид магния (Mg(OH)2)
Кроме того, металлы могут взаимодействовать с кислородом воды и кислотами, образуя оксиды металлов и соли кислот. Например:
- Цинк (Zn) + кислород (O2) + вода (H2O) → оксид цинка (ZnO)
- Цинк (Zn) + кислород (O2) + серная кислота (H2SO4) → сульфат цинка (ZnSO4)
Уравнения металлов с кислородом воды являются основой для изучения химических реакций и применения металлов в различных отраслях промышленности.
Вода — химическое соединение

Вода — одно из основных химических соединений, состоящее из молекул, которые состоят из двух атомов водорода и одного атома кислорода. Она является необходимой и незаменимой для жизни субстанцией, которая составляет около 70% массы человеческого тела и присутствует практически во всех природных средах.
Вода обладает рядом уникальных свойств, которые обусловлены ее структурой и химическими взаимодействиями. Например, вода является универсальным растворителем и способна растворять множество веществ благодаря своей полярности. Она также обладает высокой теплоемкостью, что делает ее эффективным регулятором температуры в природе и организмах.
Вода играет важную роль в биохимических процессах, таких как дыхание, пищеварение и фотосинтез. Она также является реагентом во многих химических реакциях, в том числе в процессе взаимодействия металлов с кислородом и кислотами. При этом образуются различные химические соединения и ионы.
Более того, вода обладает поверхностно-активными свойствами и способна образовывать пленки, пены и капли. Эти свойства объясняют проявление поверхностного натяжения и капиллярных явлений. Кроме того, вода обладает высокой удельной теплотой испарения, что делает ее важным элементом в процессе охлаждения и кондиционирования.
Металлы и их взаимодействие с водой
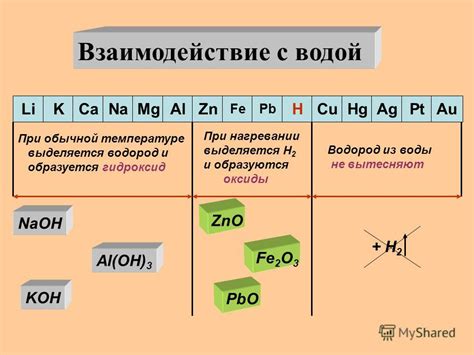
Металлы – это химические элементы, которые обладают хорошей электропроводностью и гибкостью. Они широко используются в различных сферах, таких как строительство, электроника и авиационная промышленность. Однако, металлические поверхности могут подвергаться различным процессам взаимодействия с окружающей средой, включая воду.
Вода является естественным растворителем и может оказывать влияние на металлы. Взаимодействие металлов с водой может приводить к различным химическим реакциям, таким как окисление, растворение и образование соединений. Некоторые металлы, такие как натрий и калий, реагируют с водой с выделением газа в виде пузырьков. Это происходит из-за образования гидроксидов и выделения водорода.
Однако, не все металлы взаимодействуют с водой активно. Некоторые металлы, такие как золото и платина, имеют высокую устойчивость к воздействию воды и не реагируют с ней. Некоторые металлы могут реагировать только с горячей водой или с присутствием определенных реагентов.
Исследование взаимодействия металлов с водой имеет большое значение для понимания и применения этих материалов в различных отраслях промышленности. Это помогает определить их стойкость к коррозии и сделать правильный выбор металла при проектировании различных конструкций и изделий.
Уравнения реакций металлов с водой

Металлы могут взаимодействовать с водой, что приводит к образованию гидроксидов металлов и выделению водорода. Данные реакции обладают большой практической значимостью и широко используются в различных сферах.
Например, натрий (Na) реагирует с водой по следующему уравнению:
2Na + 2H2O → 2NaOH + H2
Подобным образом, калий (K) взаимодействует с водой, образуя гидроксид калия и выделяя водород:
2K + 2H2O → 2KOH + H2
Реакция железа (Fe) с водой приводит к образованию гидроксида железа и выделению водорода:
3Fe + 4H2O → Fe(OH)3 + H2
Также можно отметить, что металлы, находящиеся выше в ряду активности, более активно взаимодействуют с водой, причем реакция протекает более интенсивно. Например, калий реагирует с водой гораздо быстрее, чем железо.
В результате реакции металлов с водой образуются гидроксиды, которые являются щелочными веществами. Получившийся водород может быть использован в различных процессах и является важным реагентом во многих областях науки и промышленности.
Уравнения металлов с кислотами

Когда металлы вступают во взаимодействие с кислотами, происходит химическая реакция, в результате которой образуются соответствующие соли и выделяется водород. Эти реакции можно описать с помощью уравнений.
Например, реакция железа со соляной кислотой может быть представлена следующим уравнением:
Fe + 2HCl → FeCl2 + H2
В этом случае, железо (Fe) взаимодействует с соляной кислотой (HCl), образуется хлорид железа (FeCl2) и выделяется молекулярный водород (H2).
Аналогично, уравнение реакции цинка (Zn) с серной кислотой (H2SO4) будет выглядеть так:
Zn + H2SO4 → ZnSO4 + H2
Здесь цинк (Zn) реагирует с серной кислотой (H2SO4), образуется сульфат цинка (ZnSO4) и выделяется молекулярный водород (H2).
Таким образом, уравнения металлов с кислотами позволяют описать химические реакции, которые происходят при взаимодействии этих веществ. Эти уравнения являются основой для понимания и изучения различных химических процессов и применяются в химической промышленности и научных исследованиях.
Взаимодействие металлов с кислотами

Металлы имеют способность взаимодействовать с кислотами, что приводит к образованию солей и выделению водорода. Это происходит в результате химических реакций между металлами и кислотами.
Во время взаимодействия металлов с кислотами происходит образование ионов металла и ионов водорода. Ионы металла образуют соли, которые растворяются в растворе. Выделение водорода происходит в газообразной форме и может быть обнаружено с помощью специальных реакций.
Сила взаимодействия металла с кислотой зависит от ряда металлов и их электрохимической активности. Некоторые металлы, такие как натрий или калий, реагируют с кислотами с выделением большого количества водорода и образованием солей. Другие металлы, например, железо или цинк, могут реагировать только с некоторыми кислотами и образовывать менее активные соли и меньшее количество водорода.
Взаимодействие металлов с кислотами является важной химической реакцией, которая используется в промышленности и лабораторных исследованиях. Эта реакция позволяет получать различные химические соединения, используемые в производстве и научных целях.
Уравнения реакций металлов с кислотами
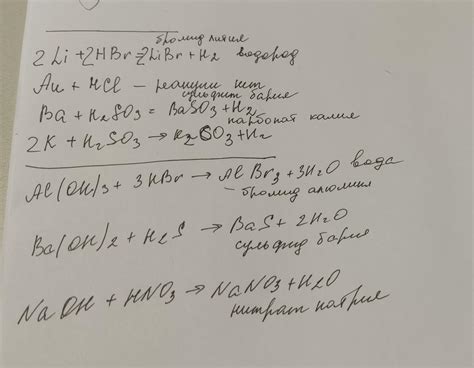
Реакции металлов с кислотами являются одним из основных типов химических взаимодействий. В ходе этих реакций происходит образование солей и выделение водорода. Уравнения реакций можно записывать в общем виде следующим образом: металл + кислота → соль + водород.
При этом следует учитывать, что разные металлы могут взаимодействовать с разными кислотами. Например, щелочные металлы, такие как натрий и калий, реагируют с водой, причем уравнение реакции имеет вид: металл + вода → щелочь + водород. Эта реакция является экзотермической и сопровождается выделением тепла.
С другой стороны, большинство металлов не реагируют с водой, но реагируют с кислотами, например, соляной, уксусной или серной. Уравнения этих реакций представляют собой общий вид металл + кислота → соль + водород. Например, железо при взаимодействии с соляной кислотой даёт соль железа и выделяет водород: Fe + HCl → FeCl₂ + H₂.
Также есть металлы, которые реагируют только с определенными кислотами. Например, цинк реагирует с серной кислотой, но не реагирует с соляной кислотой. Уравнение реакции цинка с серной кислотой выглядит следующим образом: Zn + H₂SO₄ → ZnSO₄ + H₂.
Важно отметить, что уравнения реакций металлов с кислотами можно использовать для определения активности металлов. Активные металлы быстро реагируют с кислотами, выделяя большое количество водорода, в то время как менее активные металлы реагируют медленнее или не реагируют вообще.
Вопрос-ответ

Как происходит взаимодействие металлов с кислородом воды?
Взаимодействие металлов с кислородом воды происходит путем окисления металла. При этом металл отдает электроны кислороду, образуя положительные ионы металла и гидроксиды металла. Реакция взаимодействия металла с кислородом воды может протекать с различной интенсивностью в зависимости от химической активности металла.
Какие металлы реагируют с кислородом воды?
С кислородом воды могут реагировать различные металлы, такие как натрий, калий, кальций, магний, алюминий, цинк, железо и многие другие. Однако химическая активность металлов различна, поэтому некоторые из них активно реагируют с кислородом воды, а некоторые реагируют слабо или вообще не реагируют.
Какие продукты образуются при взаимодействии металлов с кислородом воды?
При взаимодействии металлов с кислородом воды образуются гидроксиды металла. Например, при реакции натрия с кислородом воды образуется гидроксид натрия (натрогидроксид) и выделяется водород. Образование гидроксида металла является результатом окисления металла и получения положительного иона металла. Гидроксид металла обычно имеет щелочную реакцию и может действовать как основание.
Какие реакции металлов с кислородом воды могут быть опасными?
Некоторые реакции металлов с кислородом воды могут быть опасными из-за выделения водорода. Водород является горючим газом, и если его скапливается в закрытом пространстве, может произойти взрыв. Поэтому при обращении с металлами, реагирующими с кислородом воды, необходимо соблюдать меры предосторожности и работать в хорошо проветриваемых помещениях.
Какая роль играют металлы при взаимодействии с кислотами?
Металлы играют роль восстановителей при взаимодействии с кислотами. При этом металл отдает свои электроны атомам водорода из кислоты, образуя положительные ионы металла и соединение водорода. Такие реакции протекают особенно активно с сильными кислотами, например, соляной или серной.
