Щелочные металлы - это группа элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они являются самыми активными металлами в периодической системе и легко реагируют с другими веществами.
Для записи химических реакций с щелочными металлами используется химическое уравнение. В химическом уравнении указываются исходные вещества (реагенты) слева от знака равенства и получаемые вещества (продукты реакции) справа от знака равенства. Коэффициенты перед формулами веществ показывают их стехиометрическое соотношение.
С щелочными металлами можно проводить различные реакции, такие как реакции с кислородом, с водой, со солями и другие.
Например, реакция лития с водой может быть записана следующим образом:
2Li + H2O → 2LiOH + H2
Реакция натрия с кислородом выглядит следующим образом:
4Na + O2 → 2Na2O
Таким образом, запись химических реакций с щелочными металлами является важным инструментом для изучения и понимания их химических свойств и взаимодействий с другими веществами.
Запись химических реакций с щелочными металлами

Щелочные металлы – это элементы I группы периодической системы, которые вступают в реакцию с водой, кислородом, галогенами и другими веществами. Запись химических реакций с щелочными металлами осуществляется в соответствии с принципами балансировки и учетом степени окисления.
Для записи химических реакций с щелочными металлами необходимо указать формулы реагентов и продуктов, а также уравновесить уравнение, чтобы соблюсти законы сохранения массы и заряда. Например, реакцию щелочного металла с кислородом можно записать следующим образом: 2M + O2 → 2MO, где M – щелочный металл, а MO – оксид щелочного металла.
Важно отметить, что щелочные металлы образуют ионы со степенью окисления +1. Поэтому, при записи реакций с участием щелочных металлов, необходимо учесть изменение степени окисления в реагентах и продуктах. Например, реакцию между щелочным металлом и кислородом можно записать в виде: 4M + O2 → 2M2O.
Для удобства и наглядности, реакции с щелочными металлами также можно записывать в виде таблицы или перечисления. Например:
- Реакция щелочного металла с водой: 2M + 2H2O → 2MOH + H2, где M – щелочный металл, MOH – гидроксид щелочного металла.
- Реакция щелочного металла с кислородом: 4M + O2 → 2M2O, где M – щелочный металл, MO – оксид щелочного металла.
Запись химических реакций с щелочными металлами требует понимания основных принципов и правил балансировки уравнений. Корректная запись реакций позволяет проанализировать взаимодействие щелочных металлов с другими веществами и установить зависимости между их химическими свойствами.
Щелочные металлы: определение и свойства
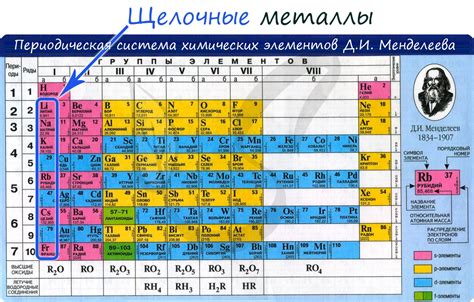
Щелочные металлы - это группа элементов периодической таблицы, которая включает в себя литий, натрий, калий, рубидий, цезий и франций. Они имеют характерные химические свойства, обусловленные их электронной структурой.
Основными характеристиками щелочных металлов являются их низкая плотность, низкая температура плавления и высокая химическая реакционность. Они хорошо проводят тепло и электричество, и выделяют яркий огонь при сгорании. Кроме того, щелочные металлы легко растворяются в воде и образуют гидроксиды.
Одной из характерных особенностей щелочных металлов является их способность образовывать стабильные катионы с положительным зарядом. Например, литий образует ион Li+, натрий - Na+, калий - K+ и так далее. Благодаря этой особенности щелочные металлы активно взаимодействуют с другими веществами и участвуют во множестве химических реакций.
Другим важным свойством щелочных металлов является их способность образовывать сплавы с другими металлами. Такие сплавы обладают улучшенными механическими свойствами и находят широкое применение в различных областях промышленности.
В целом, щелочные металлы являются важными элементами в химической промышленности и научных исследованиях. Их свойства и реакционность позволяют использовать их в различных процессах, включая создание электрических батарей, производство сплавов, очистку воды и многое другое.
Вопрос-ответ

Как записать реакцию между щелочным металлом и кислородом?
Чтобы записать реакцию между щелочным металлом и кислородом, нужно сначала указать химический символ щелочного металла, например, Na для натрия. Затем ставим знак "+" и пишем символ кислорода, который обычно обозначается как O. Далее указываем соотношение количества атомов, например, 2Na + O2. Наконец, указываем стрелку вправо и записываем символы получившихся продуктов, которые получаются в результате реакции. В случае реакции щелочного металла с кислородом, продуктами будут щелочная основа, например, Na2O.
Как записать реакцию между щелочным металлом и водой?
Для записи реакции между щелочным металлом и водой, сначала указываем символ щелочного металла, например, Na для натрия, а затем ставим знак "+" и пишем символ воды - H2O. Далее указываем стрелку вправо и записываем символы получившихся продуктов. При реакции щелочного металла с водой образуется щелочная основа (например, NaOH) и выделяется водород (например, H2). Итоговая реакция будет выглядеть как Na + H2O -> NaOH + H2.
Как записать реакцию между щелочным металлом и кислотой?
Для записи реакции между щелочным металлом и кислотой, сначала указываем химический символ щелочного металла, например, Na для натрия. Затем ставим знак "+" и пишем символ кислоты, которая обычно записывается в виде HX, где X - какой-либо атом или группа атомов (например, HCl). После этого, указываем стрелку вправо и записываем символы получившихся продуктов. В случае реакции щелочного металла с кислотой, продуктами будут соль (например, NaCl) и вода (например, H2O). Итоговая реакция будет выглядеть как 2Na + 2HX -> 2NaX + H2O.
