Углерод - химический элемент, обладающий атомным номером 6. Этот элемент широко известен своими разнообразными свойствами и способен образовывать огромное количество соединений. Но стоит ли отнести его к металлам или неметаллам?
Углерод обладает особым положением в периодической таблице элементов. Он находится во втором периоде, между бором и азотом. Несмотря на то, что основное состояние углерода является неметаллическим, в некоторых условиях он может образовывать своеобразные металлические формы.
Одной из наиболее известных металлических форм углерода является алмаз. При нагревании и высоком давлении, алмаз превращается в графит - неметаллическую форму углерода. Также существует металлическая форма углерода - фуллерены, которые обладают металлическими свойствами и могут быть использованы в различных отраслях науки и промышленности.
Углерод: свойства и структура
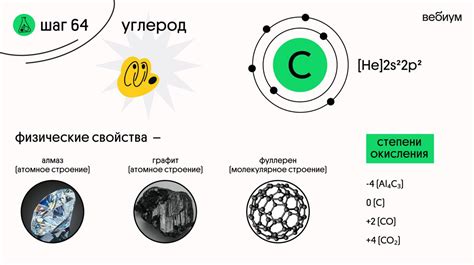
Углерод - химический элемент, который является основой для создания огромного разнообразия соединений. Он имеет атомный номер 6 и относится к группе 14 периодической системы элементов. Углерод является неметаллом и известен человечеству с древних времен.
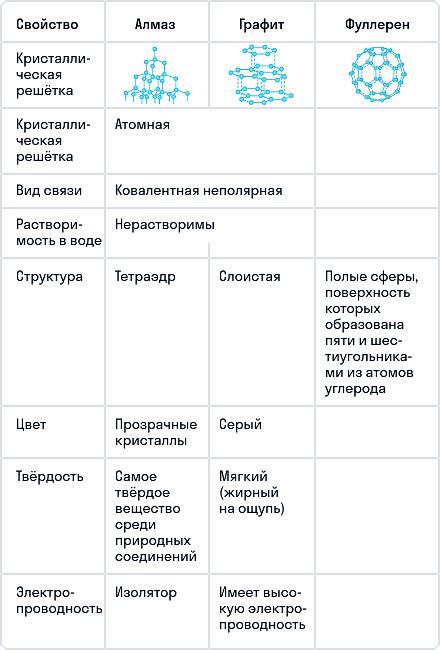
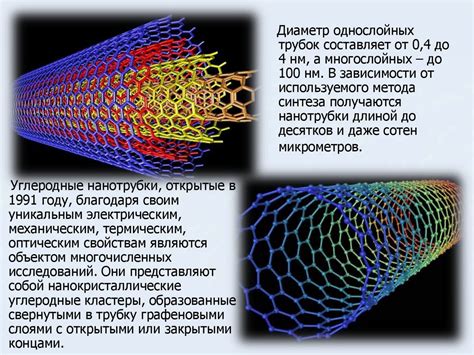
Одна из главных особенностей углерода - его способность образовывать длинные цепочки и ветвистые структуры. Это объясняет его важное место в органической химии и его многочисленные аллотропные формы, такие как алмазы, графит и фуллерены. Графит представляет собой слоистую структуру, состоящую из атомов углерода, связанных друг с другом в плоскости шестиугольников.
Углерод также обладает высокой устойчивостью к теплу и химическим реагентам. Он может образовывать сильные связи с другими атомами, включая себя, что позволяет ему образовывать стабильные молекулы. Например, в алмазе каждый атом углерода связан с четырьмя соседними атомами в трехмерной структуре.
Углерод также способен образовывать различные двойные и тройные связи, что важно для его участия в образовании сложных молекул и органических соединений. Это придает углероду уникальную химическую активность и делает его основным строительным элементом живых организмов, так как он образует основу для большинства биологических молекул, включая углеводы, жиры, белки и нуклеиновые кислоты.
Углерод в периодической таблице
Углерод (C) – элемент, расположенный в четвертом периоде периодической таблицы Менделеева. Он является основным элементом органических соединений и играет ключевую роль в жизни на Земле. Углерод также имеет много различных аллотропных форм, которые отличаются по структуре и свойствам.
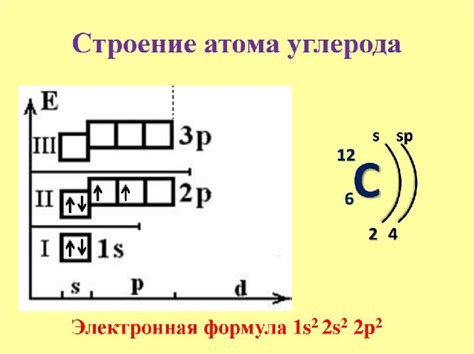
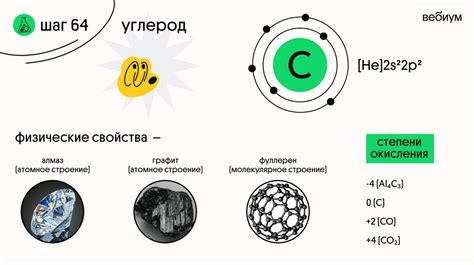
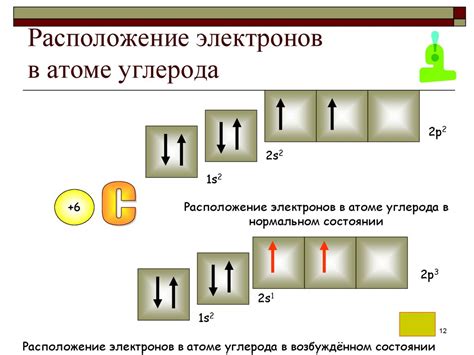
Атом углерода имеет 6 электронов, расположенных на электронных оболочках. Он имеет электронную конфигурацию 1s2 2s2 2p2. Из-за наличия 4 валентных электронов, углерод образует большое количество соединений с другими элементами.
Углерод также имеет свойство образовывать двойные и тройные связи с другими атомами углерода. Это позволяет ему образовывать сложные и разнообразные структуры, включая решетки алмазов и графита, а также цепи и кольца в органических молекулах.
Углеродная нить – одна из форм углерода, обладающая высокой прочностью и электропроводностью. Она широко применяется в различных областях, включая производство композитных материалов, электронику и энергетику.
В периодической таблице углерод находится между бором (B) и азотом (N). Он относится к неметаллам и имеет среднюю электроотрицательность. Углерод также является одним из элементов, входящих в группу 14 и период 2. Его атомный номер равен 6.
Физические свойства углерода
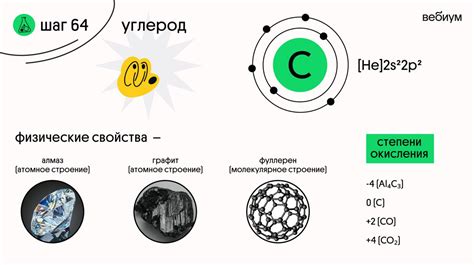
1. Кристаллическая структура: Углерод образует кристаллические решетки различных форм, таких как алмаз, графит, фуллерены и нанотрубки. Алмаз и графит являются наиболее распространенными формами углерода и имеют разную структуру и свойства. Алмаз обладает твердостью и прозрачностью, в то время как графит является мягким и проводящим материалом.
2. Плотность: Плотность углерода зависит от его формы и условий. Например, плотность алмаза составляет около 3,5 г/см³, тогда как плотность графита намного ниже и составляет около 2,2 г/см³.
3. Точка плавления и кипения: Углерод не имеет точной точки плавления и кипения, так как его аллотропные формы переходят в состояние газа при высоких температурах без фазовых переходов. Однако, аллотропы углерода имеют различные температурные диапазоны стабильности. Например, алмаз стабилен при высоких температурах, в то время как графит стабилен при обычных условиях.
4. Проводимость: Углеродные материалы имеют разные уровни проводимости. Например, графит является хорошим проводником электричества и тепла, в то время как алмаз ведет тепло и электричество плохо. Эти различия в проводимости обусловлены структурой и связями между атомами углерода в разных аллотропных формах.
5. Легкость соединения с другими элементами: Углерод образует множество соединений с другими элементами, включая водород, кислород, азот, серу. Такие соединения играют важную роль в областях, таких как органическая химия, пищевая промышленность, медицина и промышленность строительных материалов.
6. Термическая устойчивость: Углерод обладает высокой термической устойчивостью, что позволяет использовать его в процессах, связанных с высокими температурами, таких как производство стали и керамики.
7. Эластичность: Углеродные материалы, такие как графен и углеродные нанотрубки, обладают высокой эластичностью и прочностью, что делает их потенциально важными материалами для различных промышленных и технических приложений.
Химические свойства углерода

Углерод — уникальный элемент, обладающий множеством химических свойств. Он способен образовывать огромное количество соединений, благодаря своей способности образовывать четыре ковалентных связи. Это делает его одним из основных элементов органической химии, поскольку он является основой для образования множества органических соединений, таких как углеводороды и аминокислоты.
Однако углерод также может образовывать соединения с неорганическими элементами, например, оксид углерода, карбиды и нитриды углерода. Большая часть неорганических соединений углерода характеризуется высокой термической и химической стойкостью.
Углерод также является основой для образования ряда материалов с различными свойствами. Например, алмаз и графит являются кристаллическими формами углерода, при этом алмаз является одним из самых твердых известных материалов, а графит обладает свойством смазки и используется в карандашах.
Особенно интересно, что углерод может образовывать длинные цепочки атомов, что позволяет создавать полимеры. Такие материалы, как пластик и резина, являются примерами полимеров, которые состоят из длинных цепочек углеродных атомов. Благодаря этому свойству углерода возможно создание широкого спектра полимерных материалов с различными физическими и химическими свойствами.
Углеродные соединения

Углерод – химический элемент, обладающий уникальной способностью образовывать бесконечное разнообразие соединений. Углеродные соединения являются основой для жизни на Земле и широко применяются в различных областях нашей жизни.
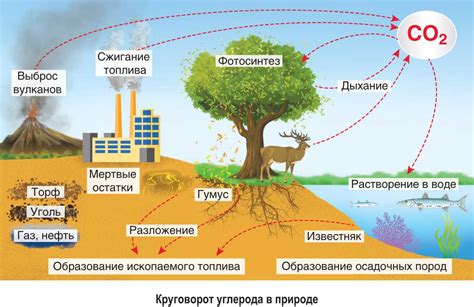
Одно из самых известных углеродных соединений – углекислый газ (СО2). Он образуется при сгорании углеводородов и играет важную роль в природных циклах. Углекислый газ используется в пищевой промышленности, например, для газирования напитков, а также в процессе ферментации при производстве хлеба и пива.
Углеводороды – это класс соединений, состоящих из углерода и водорода. Они являются основным источником энергии и используются в качестве топлива. Углеводороды также используются в производстве пластиков, резиновых изделий и многих других материалов.
Органические кислоты – важные классы углеродных соединений, которые часто встречаются в природе. Они имеют кислотные свойства и широко используются в производстве пищевых продуктов, косметики и лекарственных препаратов.
Углерод – элемент базовых органических соединений, таких как углеводы, жиры и белки. Он играет ключевую роль в жизнедеятельности организмов и является основой для образования сложных молекул, необходимых для существования жизни.
Органические соединения
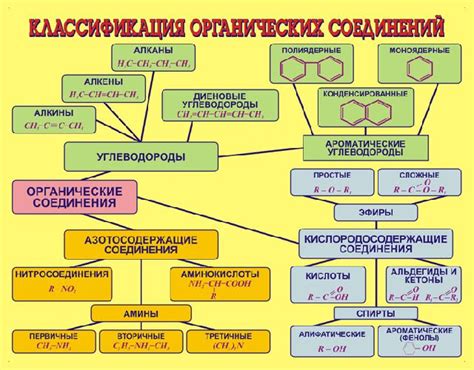
Органические соединения - это химические соединения, основанные на углероде, который образует основу их молекул. Они могут содержать атомы водорода, кислорода, азота, фосфора, серы и других элементов. Органические соединения обширно изучаются в органической химии и играют важную роль в жизни всех организмов на Земле.
Углерод является основным строительным блоком органических соединений и обладает уникальными свойствами. Он образует четыре ковалентные связи с другими атомами, что позволяет разнообразным комбинациям углерода создавать огромное количество различных соединений. Эта способность к образованию связей делает углерод основой жизни на Земле и позволяет синтезировать сложные органические соединения, такие как белки, углеводы и жиры.
Органические соединения широко распространены в природе и встречаются во многих органических системах, включая животные, растения и микроорганизмы. Мы каждый день сталкиваемся с органическими соединениями, такими как пища, лекарства, пластик, топливо и многое другое.
Органические соединения могут быть классифицированы на основе своей структуры и свойств. Они могут быть простыми или сложными, насыщенными или несаитированными, а циклические соединения могут образовывать ароматические или алициклические системы. Примеры органических соединений включают метан, этан, этилен, ацетон, глюкозу и многое другое.
Органические соединения имеют огромное значение для нашей жизни и являются основой для различных отраслей промышленности и науки. Их изучение помогает понять основные процессы, происходящие в живых системах, и разрабатывать новые материалы и препараты. Открытие и использование новых органических соединений составляет основу для развития медицины, фармацевтики, сельского хозяйства и других областей науки и технологий.
Неорганические соединения
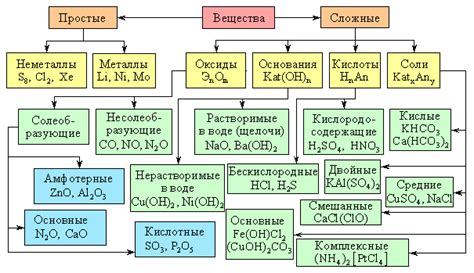
Неорганические соединения - это химические соединения, которые содержат элементы, за исключением углерода. Эти соединения образуются между атомами металлов и неметаллов и характеризуются разнообразием свойств и структур.
Неорганические соединения играют важную роль в различных отраслях промышленности и науки. Они используются как катализаторы, пигменты, добавки в пищевую и фармацевтическую промышленность, а также в качестве материалов для строительства и электроники.
Важной особенностью неорганических соединений является их структура и связи между атомами. Некоторые неорганические соединения образуют кристаллическую решетку, в которой каждый элемент связан с окружающими атомами определенным образом. Эти связи обусловливают многие физические и химические свойства соединений.
Неорганические соединения могут быть представлены в различных формах: в виде солей, оксидов, карбидов и других соединений. Они обладают широким спектром свойств и могут быть магнитными, проводить электричество, образовывать кислотные или основные растворы.
Для изучения и использования неорганических соединений проводятся различные исследовательские и прикладные работы. Изучение их свойств и реакций позволяет углубить наши знания о данной группе химических соединений и применить их в различных сферах деятельности.
Применение углерода
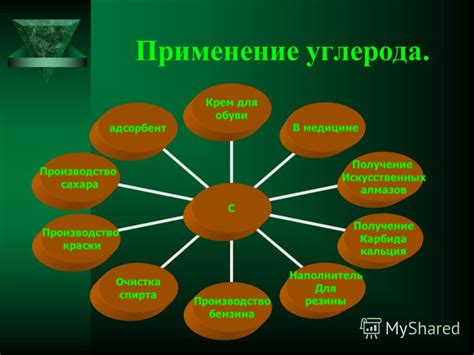
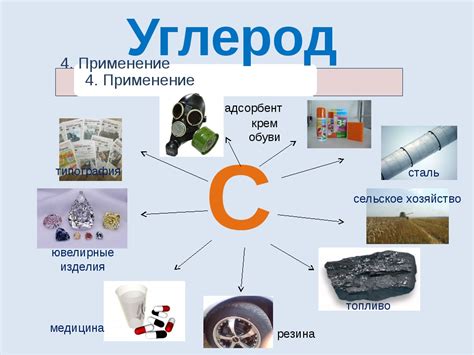
Углерод – универсальный и широко используемый элемент, который находит применение во многих областях нашей жизни. Его свойства и химические связи делают его идеальным материалом для различных применений.
1. Производство стали: Углерод играет ключевую роль в металлургической промышленности. Он добавляется в железную руду для создания сплава, известного как сталь. Углерод придает стали прочность и жесткость, делая ее одним из самых важных строительных материалов.
2. Производство пластиковых изделий: Углерод используется для производства различных пластиковых изделий. Он является основной составляющей многих типов пластиков и придает им необходимую прочность и упругость.
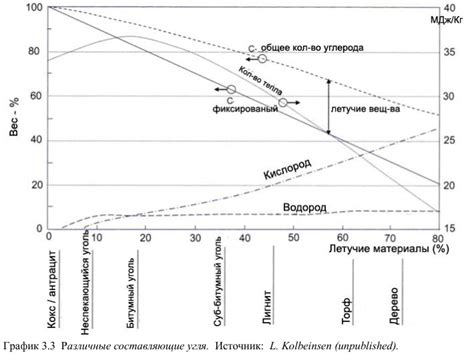
3. Энергетика: Уголь является одним из основных источников энергии в мире. Он используется для производства электроэнергии в электростанциях и в домашнем отоплении. Уголь является важным источником топлива для промышленных предприятий.
4. Изготовление электродов: Углеродные электроды широко применяются в различных областях, включая металлургию, электрохимию и электротехнику. Они используются в процессе плавления и сварки металлов, а также в производстве батарей и аккумуляторов.
5. Производство композитных материалов: Углеродные волокна и углеродно-армирующие материалы имеют высокую прочность и легкость, что делает их идеальными для использования в авиационной и автомобильной промышленности, строительстве и других отраслях, где требуются материалы с высокими механическими свойствами.
Углерод имеет множество других применений, включая производство масел и смазок, материалов для электроники и многое другое. Благодаря своим уникальным свойствам, углерод остается одним из наиболее востребованных и важных элементов для различных отраслей промышленности.
Вопрос-ответ

Углерод - металл или неметалл?
Углерод является неметаллом.
Почему углерод считается неметаллом?
Углерод считается неметаллом из-за его химических свойств и положения в периодической таблице.
Какие химические свойства углерода указывают на его неметаллическую природу?
Углерод образует основные оксиды и обладает высокой электроотрицательностью, что указывает на его неметаллическую природу.
Влияет ли температура на свойства углерода?
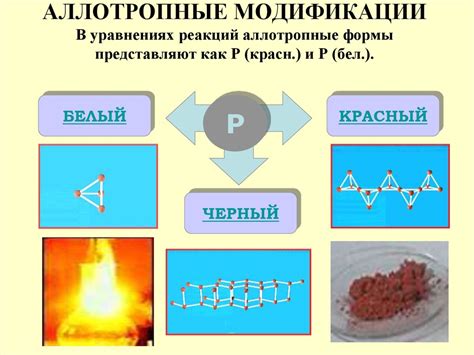
Да, температура может влиять на свойства углерода. Например, при высоких температурах углерод может образовывать аллотропные формы, такие как графит и алмаз.