Галогены металлы побочных подгрупп – это группа химических элементов, которые обладают уникальными металлическими свойствами. Одним из основных признаков галогенов является высокая электроотрицательность, что позволяет им быть хорошими окислителями. Благодаря этому, галогены образуют необычные соединения с другими элементами, включая металлы. Особенно ярко эти свойства проявляются у металлов побочных подгрупп – криптона и монтана.
Один из наиболее интересных аспектов металлических свойств галогены металлы побочных подгрупп – это их способность к образованию стабильных искусственных соединений. Например, криптон образует соединения с другими галогенами, такие как тетрафторид криптона, которые обладают высокой стабильностью и остаются газообразными при комнатной температуре. Также, монтана образует многочисленные соединения с различными галогенами, которые обладают высокой устойчивостью и ярким цветом.
Еще одним интересным свойством галогены металлы побочных подгрупп является их способность к образованию металлических кластеров. Кластеры – это кристаллические структуры, состоящие из множества металлических атомов, которые могут образовать различные формы и размеры. Многие галогены металлы побочных подгрупп способны образовывать трех-, четырех- и более атомные кластеры, что делает их особенно привлекательными для исследования и применения в различных отраслях науки и техники.
Особенности металлических свойств галогеновых металлов
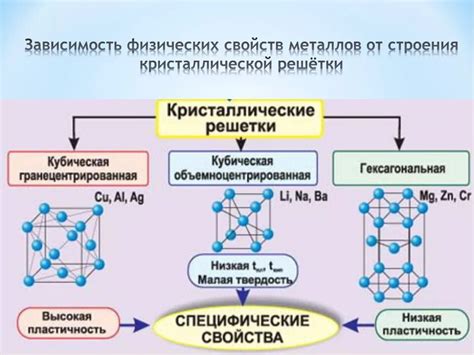
Галогены – элементы химической группы VIIА периодической системы. Они характеризуются высокой электроотрицательностью и проявляют ярко выраженные неметаллические свойства. Тем не менее, некоторые галогены, в частности металлы побочных подгрупп, обладают определенными металлическими характеристиками.
Одной из особенностей металлических свойств галогеновых металлов является их способность образовывать катионы с положительной зарядом. Например, хлор превращается в катион хлоридный (Cl+), фтор – в катион фтористый (F+) и так далее. Это позволяет галогенам образовывать ионы, которые могут участвовать в различных химических реакциях и обладать металлическими свойствами.
Другой характерной особенностью галогеновых металлов является их относительная электропроводность. Причиной этого является наличие свободных электронов в зоне проводимости у некоторых галогенов. Например, бром и иод, при определенных условиях, способны проявлять металлическую проводимость. Эта электропроводность может быть использована в различных технических и технологических целях.
Также стоит отметить, что галогеновые металлы обладают специфическими металлическими свойствами, которые проявляются при взаимодействии с другими элементами. Например, металлы побочных подгрупп (такие, как хлор, бром, йод) могут образовывать разнообразные соединения с металлами основных подгрупп периодической системы, обладающие металлическими свойствами и применяемые в различных отраслях науки и техники.
В целом, хотя галогены обычно проявляют неметаллические характеристики, некоторые из них все же обладают определенными металлическими свойствами, что делает их уникальными и интересными объектами изучения в научных исследованиях и применения в различных сферах деятельности.
Яркое выражение металлических свойств металлов побочных подгрупп

Металлы побочных подгрупп, такие как галогены металлы, обладают рядом ярко выраженных металлических свойств, которые отличают их от других элементов.
Во-первых, металлы побочных подгрупп обладают высокой электропроводностью. Это означает, что они легко передают электрический ток. При этом они обладают низким сопротивлением, что позволяет им быть эффективными проводниками электричества.
Во-вторых, металлы побочных подгрупп обладают высокой теплопроводностью. Они способны передавать тепло весьма эффективно и равномерно. Именно поэтому металлы часто используются для изготовления нагревательных элементов и теплообменников.
Третьим важным свойством металлов побочных подгрупп является их распространенность. Эти металлы легко обнаруживаются в земной коре и имеют широкий спектр применений в различных отраслях промышленности, таких как металлургия, электроника, строительство и другие.
Кроме того, металлы побочных подгрупп обладают высокой пластичностью и прочностью. Они могут быть легко обработаны и изменены в форме без потери своих основных металлических свойств. Благодаря этому, они широко применяются в производстве различных изделий и конструкций.
Таким образом, металлы побочных подгрупп, включая галогены металлы, проявляют яркое выражение металлических свойств, которые делают их особенно полезными и востребованными в различных сферах человеческой деятельности.
Сравнение галогеновых и металлов побочных подгрупп по металлическим свойствам
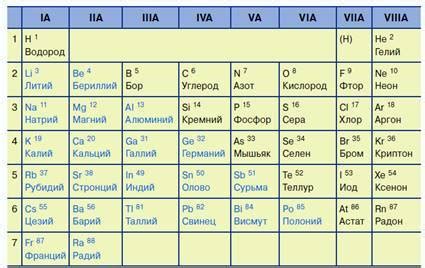
Галогены - это элементы, принадлежащие к группе 17 периодической системы химических элементов. В отличие от металлов побочных подгрупп, галогены не обладают металлическими свойствами, такими как хорошая электропроводность, блеск и пластичность.
Вместо этого галогены проявляют следующие характеристики: они являются неметаллами, обладают высокой электроотрицательностью и химической активностью. Галогены образуют сильные кислоты, обладают высокой способностью к образованию солей с металлами побочных подгрупп.
В отличие от галогеновых элементов, металлы побочных подгрупп обладают металлическими свойствами. Они обычно отличаются блеском, хорошей электропроводностью и пластичностью. Металлы побочных подгрупп также обладают более низкой электроотрицательностью и химической активностью по сравнению с галогенами.
Важной особенностью металлов побочных подгрупп является их способность формировать ионные соединения с галогенами. В результате реакции образуются соли, которые могут иметь разнообразные применения, от промышленности до медицины.
Таким образом, галогены и металлы побочных подгрупп имеют существенные различия в своих металлических свойствах. Галогены являются неметаллами с высокой электроотрицательностью и химической активностью, в то время как металлы побочных подгрупп обладают характерными металлическими свойствами и меньшей активностью.
Вопрос-ответ

Какие металлические свойства имеют галогены металлы побочных подгрупп?
Галогены металлы побочных подгрупп могут обладать некоторыми металлическими свойствами, такими как электропроводность и теплопроводность. Однако, это свойства являются относительно слабыми по сравнению с настоящими металлами.
В чем особенности металлических свойств галогенов металлов побочных подгрупп?
Особенностью металлических свойств галогенов металлов побочных подгрупп является то, что они могут проявляться только при определенных условиях, например, при высоких температурах или при наличии определенного количества других элементов. Кроме того, эти свойства могут иметь яркое выражение лишь в некоторых случаях, когда происходит особая реакция с окружающей средой.
Как проявляются металлические свойства галогенов металлов побочных подгрупп?
Металлические свойства галогенов металлов побочных подгрупп могут проявляться различными способами. Например, они могут быть электропроводными и теплопроводными, что позволяет им проводить электрический ток и тепло. Кроме того, некоторые из этих элементов могут иметь металлический блеск и быть деформируемыми под воздействием силы.
