Металлы - это широко распространенный класс элементов в периодической таблице Менделеева. Они обладают рядом характеристик, которые делают их уникальными и важными для нашей повседневной жизни.
Во-первых, металлы обладают высокой электропроводностью, что позволяет им легко передавать электрический ток. Это делает металлы идеальными материалами для создания проводников и электрических контактов.
Кроме того, металлы имеют высокую теплопроводность, что позволяет им эффективно передавать тепло. Это делает металлы очень полезными в промышленности для создания теплопроводящих материалов и систем охлаждения.
Один из самых важных аспектов металлических материалов - их прочность. Металлы обладают высокими механическими свойствами, такими как твердость и устойчивость к деформации. Благодаря этим свойствам металлы широко используются в конструкционных материалах, машиностроении и авиационной промышленности.
Металлы периодической таблицы Менделеева
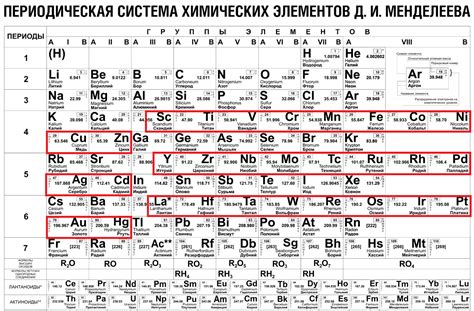
Металлы составляют большую часть периодической таблицы Менделеева и являются одной из основных групп химических элементов. Они обладают рядом характеристик, которые делают их уникальными и важными в различных областях науки и промышленности.
Физические свойства: металлы обладают высокой теплопроводностью и электропроводностью, это связано с особенностями их внутренней структуры. Кроме того, металлы обладают высокой пластичностью и прочностью, что делает их идеальными материалами для конструкций и производства различных изделий.
Химические свойства: металлы обычно образуют ионные соединения с неметаллами, что делает их важными реагентами в химических реакциях. Металлы также химически активны и способны реагировать с другими веществами, что приводит к возникновению окислительно-восстановительных реакций.
Применение: металлы имеют широкое применение в различных отраслях промышленности. Например, железо используется для производства стали, медь - для проводов и электрических устройств, алюминий - для производства авиационных и автомобильных деталей. Металлы также играют важную роль в медицине, электронике и многих других областях.
Распределение в периодической таблице: металлы расположены слева от черты, которая разделяет металлы и неметаллы. В периодической таблице Менделеева металлы представлены в нескольких группах: щелочные металлы, щелочноземельные металлы, переходные металлы, постпереходные металлы и лантаниды и актиниды.
Определение и классификация
Металлы - это класс элементов периодической таблицы Менделеева, обладающих рядом характеристик, отличающих их от других классов элементов. Основные характеристики металлов включают хорошую электропроводность, теплопроводность, гибкость и блеск. Они также обладают высокой плотностью и температурой плавления.
Металлы могут быть классифицированы по различным признакам, включая их физические свойства, химические свойства и их положение в периодической таблице. Физические свойства металлов включают плотность, твердость, точку плавления и теплопроводность. Химические свойства металлов определяются их способностью образовывать положительные ионы и вступать в химические реакции. По положению в периодической таблице металлы могут быть разделены на блоки, группы и периоды.
Металлы в периодической таблице Менделеева расположены слева от ступицы в виде ступеней и групп. Они включают основные металлы (литий, натрий, калий итд), переходные металлы (железо, медь, цинк) и металлы блока п (алюминий, олово, свинец). Основные металлы относятся к группам 1 и 2 периодической таблицы, переходные металлы - группа 3-12, а металлы блока п - группы 13-16. Каждая группа металлов имеет свойство образовывать положительные ионы.
Классификация металлов является важным инструментом для изучения и понимания их свойств и использования в различных областях науки и промышленности. Знание о классификации позволяет ученым более точно определить свойства и возможности каждого металла, а также их влияние на окружающую среду и человеческое здоровье.
Основные свойства и характеристики

Металлы периодической таблицы Менделеева – это большая группа элементов, которые обладают рядом основных свойств и характеристик. Вот некоторые из них:
- Проводимость электричества и тепла: Металлы являются отличными проводниками как электричества, так и тепла. Благодаря свободно движущимся электронам в их структуре, они обладают высокой электропроводностью и теплопроводностью.
- Гибкость и пластичность: Металлы обладают способностью к деформации без разрушения. Они могут быть легко прокатаны в листы, вытянуты в проволоку или отлиты в различные формы, что делает их удобными для производства разнообразных изделий.
- Металлический блеск: Металлы обладают своеобразным блеском, известным как металлический блеск. Это свойство связано с отражением света от поверхности металла и является одной из причин, по которой многие металлы используются в ювелирном деле и декоративных изделиях.
- Высокая плотность: Металлы обладают высокой плотностью по сравнению с другими элементами. Плотность металлов обусловлена их атомной структурой, где атомы плотно упакованы друг к другу.
Кроме того, металлы имеют низкую электроотрицательность, что делает их способными образовывать ионные связи с не металлами и создавать различные соединения. Металлические элементы также обладают хорошими механическими свойствами, такими как прочность и устойчивость к различным воздействиям.
Щелочные металлы
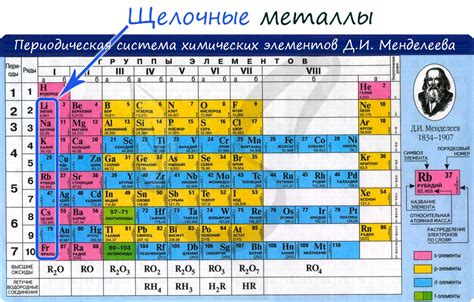
Щелочные металлы - это элементы первой группы периодической таблицы Менделеева. В эту группу входят литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Щелочные металлы обладают рядом характерных особенностей. Они являются положительно заряженными ионами, образуя одновалентные катионы M+. Эти металлы имеют низкую плотность и низкую температуру плавления, что делает их мягкими и легкими в обработке. Они также обладают низкой твердостью, что делает их хорошими материалами для изготовления ложек, кастрюль и других кухонных принадлежностей.
В свежем состоянии щелочные металлы имеют серебристо-белый цвет, однако, они быстро окисляются на воздухе и приобретают оксидную пленку. Этот процесс делает поверхность металлов матовой и покрывает их характерной патиной. Кроме того, щелочные металлы легко сочетаются с водой, образуя гидроксиды и выделяя водородный газ. Этот процесс сопровождается сильным выделением тепла и является хорошим химическим тестом на наличие щелочного металла.
Щелочные металлы являются очень активными химическими элементами. Они образуют соли и соединения, которые широко используются в различных отраслях промышленности. Например, карбонаты, гидроксиды и нитраты щелочных металлов применяются в производстве стекла, мыла, удобрений и пищевых добавок. Благодаря своей активности и высокой реакционной способности, щелочные металлы находят применение в химической синтезе и катализе реакций.
В заключение, щелочные металлы - это группа элементов, характеризующихся низкой плотностью, низкой твердостью и химической активностью. Их способность образовывать соли и соединения делает их неотъемлемыми компонентами многих промышленных процессов и повседневной жизни.
Химические свойства и реактивность

Химические свойства металлов периодической таблицы Менделеева обусловлены их структурой и электронной конфигурацией. Металлы обладают способностью образовывать ионные соединения с неметаллами, образуя соли. Это связано с тем, что металлы имеют мало электронов во внешней оболочке и легко отдают их, становясь положительно заряженными ионами.
Металлы также проявляют способность к окислению, что означает потерю электронов. Окислительными свойствами обладают особенно активные металлы, такие как литий и калий. Они реагируют с кислородом или халогенами, сжигаясь или образуя соответствующие оксиды или галогениды.
Однако не все металлы одинаково активны. Активность металлов восходит к их электродному потенциалу, который показывает их способность к переходу в ионное состояние. Чем выше электродный потенциал металла, тем более активным он является и тем проще его окисление.
Металлы также могут проявлять способность к растворению в различных растворителях. Например, алкалии и щелочноземельные металлы растворяются в воде, образуя щелочные растворы. Алюминий и цинк растворяются в кислотах, образуя соответствующие соли.
Одной из ключевых характеристик металлов является их способность проводить электрический ток. Такая способность связана с наличием свободных электронов в металлической решетке, которые легко передвигаются под воздействием электрического поля.
Применение в промышленности и повседневной жизни

Металлы, присутствующие в периодической таблице Менделеева, играют важную роль в промышленности и повседневной жизни человека. Они широко используются в различных сферах и процессах благодаря своим уникальным свойствам.
Некоторые металлы, например, железо и алюминий, являются основными компонентами в производстве различных материалов. Железо используется для создания структурных элементов, таких как балки и колонны, в строительстве зданий и мостов. Алюминий используется в авиационной промышленности для создания легких и прочных конструкций. Оба металла также используются в производстве автомобилей, электроники, бытовой техники и многих других товаров.
Другие металлы, вроде меди и цинка, имеют хорошую электропроводимость и используются в производстве электрических проводов и компонентов. Они также находят применение в производстве медных труб для водопровода и отопления, а также в производстве различных сплавов.
Металлы, такие как свинец и кадмий, используются в аккумуляторах и батареях, и они являются важными компонентами в производстве электроэнергии. Еще одно интересное применение металлов в промышленности - это их использование в катализаторах для химических реакций, что значительно ускоряет процессы производства и повышает эффективность.
В повседневной жизни металлы также неотъемлемая часть. Они присутствуют во многих предметах, которые мы используем ежедневно. Металлические посуда, приборы, монеты, ключи, замки - все это изделия из металлов. Металлические украшения, такие как серьги, кольца и цепочки, пользуются популярностью в мире моды и стиля.
Кроме того, металлы используются в сфере медицины для создания медицинского оборудования, имплантатов, стоматологических инструментов и протезов. Некоторые металлы обладают антимикробными свойствами и используются в производстве противомикробных поверхностей, дверных ручек и медицинских инструментов для предотвращения распространения инфекций.
Щелочноземельные металлы
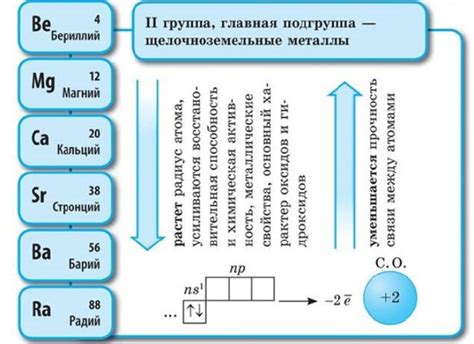
Щелочноземельные металлы - это группа элементов периодической таблицы Менделеева, расположенных во второй группе. В эту группу входят следующие элементы: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Щелочноземельные металлы обладают рядом характеристик, которые отличают их от других элементов. Они являются металлами средней активности и имеют два валентных электрона. Природные щелочноземельные металлы встречаются в земной коре в виде соединений, таких как оксиды, карбонаты и сульфаты.
Одной из основных характеристик щелочноземельных металлов является их химическая реактивность. Эти металлы реагируют с кислотами, образуя соли и выделяя водород. Они также реагируют с водой, образуя гидроксиды и выделяя водород. Это делает щелочноземельные металлы хорошими реагентами для различных химических процессов.
Щелочноземельные металлы также имеют важное применение в промышленности и технологии. Их соединения используются в производстве стекла, керамики, лекарственных препаратов и удобрений. Они также широко использовались в прошлом для изготовления сплавов и материалов с высокой прочностью.
Важными свойствами щелочноземельных металлов являются их характеристики как проводников электричества и тепла. Они обладают высокой электропроводностью и хорошо проводят тепло, что делает их важными материалами для производства электроники, электротехники и теплообменных систем.
Вопрос-ответ

Какие металлы входят в периодическую таблицу Менделеева?
В периодическую систему Менделеева входит большое количество металлов, таких как железо, алюминий, свинец, медь, золото, серебро, цинк, никель, титан и многие другие.
Какие основные характеристики металлов периодической таблицы Менделеева?
Основные характеристики металлов включают высокую теплопроводность и электропроводность, глянец и блеск, формирование ионов положительного заряда (катионов) при химических реакциях, способность образовывать металлические связи и проводить ток, а также быть тяжелыми и пластичными. Металлы также обычно отличаются высокой плотностью, высокой плавкостью и низкой электроотрицательностью.
