Водород является химическим элементом, который широко используется в различных промышленных процессах и является существенной составной частью многих соединений. Одним из таких соединений являются оксиды металлов, которые могут реагировать с водородом, образуя различные продукты.
Реакции водорода с оксидами металлов могут проходить по различным механизмам и приводить к образованию разных соединений. Одним из таких типов реакций является реакция восстановления, при которой водород выступает в качестве восстановителя. В результате этой реакции происходит снижение степени окисления металла, а водород окисляется до воды.
Еще одним типом реакции водорода с оксидами металлов является реакция протекания гидридного обмена. В этом случае водород осуществляет обмен с атомом металла, занимая его место в соединении. Эта реакция обратима и может протекать в обе стороны в зависимости от условий.
Также известны случаи, когда водород реагирует с оксидами металлов, образуя гидриды. В этом типе реакции водород и оксид металла соединяются, образуя новое вещество, которое имеет гидридную структуру. Гидриды могут обладать различными свойствами и широко применяться в различных отраслях промышленности и научных исследованиях.
Реакции водорода с оксидами

Водород - химический элемент в группе алкалиновых металлов давно привлекает внимание ученых и инженеров из-за своей высокой химической активности и уникальных свойств. Один из способов использования водорода - его реакция с оксидами металлов.
Оксиды металлов - соединения, содержащие кислород и металл. Известно множество различных оксидов металлов, и каждый из них может реагировать с водородом. Такие реакции могут быть экзотермическими (выделяющими тепло) или эндотермическими (поглощающими тепло) в зависимости от условий и химических свойств реагирующих веществ.
Реакция водорода с оксидами металлов может приводить к образованию воды и металла. Например, при реакции водорода с оксидом железа (FeO) образуется вода (H2O) и металлическое железо:
| Реакция | Уравнение |
|---|---|
| Водород + оксид железа | 3H2 + FeO → Fe + H2O |
- Примером другой реакции может быть реакция водорода с оксидом магния (MgO), при которой образуется вода и металл:
| Реакция | Уравнение |
|---|---|
| Водород + оксид магния | H2 + MgO → Mg + H2O |
Такие реакции могут быть полезными в различных промышленных процессах, а также в лабораторной практике. Они позволяют получать полезные продукты, такие как металлы, и энергию в виде тепла. Кроме того, реакции водорода с оксидами металлов могут использоваться в качестве метода выделения и очистки водорода.
В целом, реакции водорода с оксидами металлов являются важным аспектом изучения химических реакций и применения водорода в различных областях науки и технологий.
Реакции водорода с оксидами металлов

Водород является химическим элементом, который активно реагирует с оксидами металлов. Эти реакции происходят с образованием гидроксидов металлов и выделением водорода.
Реакция водорода с оксидами металлов может происходить при различных условиях, таких как температура и давление. Однако общим для всех реакций является образование водорода в результате разложения молекулы воды.
Водородное значение металла определяется его способностью образовывать соединения с водородом. Чем выше водородное значение металла, тем быстрее и интенсивнее протекает реакция с водородом.
Реакции водорода с оксидами металлов можно представить в виде следующей таблицы:
| Металл | Оксид | Гидроксид | Реакционное уравнение |
|---|---|---|---|
| Натрий | Na2O | NaOH | H2O + Na2O → 2NaOH |
| Магний | MgO | Mg(OH)2 | H2O + MgO → Mg(OH)2 |
| Алюминий | Al2O3 | Al(OH)3 | H2O + Al2O3 → Al(OH)3 |
Реакции водорода с оксидами металлов являются важными процессами в химической промышленности и используются для получения гидроксидов металлов, которые находят широкое применение в различных областях, например, в производстве стекла, водоочистке и медицине.
Термогенерирующая реакция гидридов металлов

Термогенерирующая реакция – это реакция, при которой выделяется значительное количество тепла. Гидриды металлов, в свою очередь, представляют собой соединения металлов с водородом.
При взаимодействии гидридов металлов с кислородсодержащими соединениями происходит термогенерирующая реакция. Например, реакция водорода с оксидами металлов.
В результате этой реакции образуется вода и соответствующий металл. Выделение тепла при этой реакции обусловлено высокой энергетической активностью гидридов металлов и энергетической нейтральностью соединений, которые образуются в результате реакции.
Данная реакция может использоваться для получения энергии в химических и термических процессах. Также она может быть использована в процессе получения водорода из гидридов металлов.
Термогенерирующая реакция гидридов металлов имеет широкое применение в различных отраслях науки и промышленности и является одной из важных химических реакций с выделением тепла.
Водородные реакции с оксидами благородных металлов
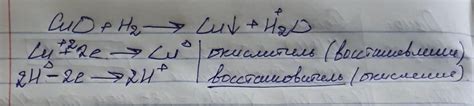
Водородные реакции с оксидами благородных металлов представляют собой важное исследовательское направление в химии. Такие реакции имеют большое значение как синтетического, так и теоретического характера. Они позволяют изучать особенности взаимодействия водорода с оксидами благородных металлов и определять их реакционную способность. Такие данные являются важной информацией для разработки новых катализаторов и процессов в различных отраслях промышленности.
Водородные реакции с оксидами благородных металлов могут протекать при различных условиях, их характер может быть кислотным, основным или амфотерным. При кислотных условиях водород реагирует с оксидом благородного металла, образуя соответствующий гидроксид и выделяя воду. При основных условиях происходит обратная реакция, когда гидроксид благородного металла разлагается на оксид и водород. Амфотерное поведение благородных металлов означает, что они могут выступать как в качестве кислотного, так и в качестве основного компонента.
Водородные реакции с оксидами благородных металлов также могут быть использованы для получения интересных соединений и материалов. Например, при реакции между водородом и оксидом платины образуется платиновый губка, который имеет высокую поверхностную активность и может использоваться, например, в качестве катализатора. Подобные материалы могут быть полезны в различных промышленных процессах, таких как очистка газов от вредных примесей или водородное хранение.
Геттерные реакции водорода с оксидами металлов
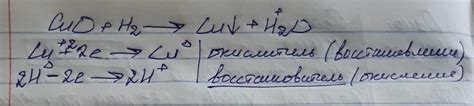
Геттерные реакции водорода с оксидами металлов представляют собой химические процессы, при которых водород вступает в реакцию с оксидами металлов, образуя соответствующие гидроксиды. Эти реакции являются важными в различных промышленных процессах и имеют большое значение в химии и материаловедении.
Оксиды металлов, вступая в реакцию с водородом, играют роль геттеров, то есть они поглощают водород и образуют несвязанный с ним продукт. В результате реакции образуется гидроксид металла, который может быть дальше использован в различных процессах и приложениях.
Геттерные реакции водорода с оксидами металлов часто используются в электронной индустрии, когда необходимо удалять следы водорода из вакуумных систем или материалов. Например, при изготовлении полупроводниковых устройств используются реакции водорода с оксидами металлов для удаления водорода, который может негативно влиять на процесс и свойства материалов.
Одним из примеров геттерной реакции водорода можно привести реакцию между водородом и оксидом железа(III). При нагревании оксида железа(III) с водородом происходит реакция, в результате которой образуется гидроксид железа(III) и выделяется водород. Эта реакция может быть использована для удаления водорода из процесса или среды.
Геттерные реакции водорода с оксидами металлов являются важными инструментами в различных отраслях промышленности, научных исследований и технологий. Они позволяют эффективно удалять водород из систем и материалов, повышая их качество и стабильность.
Вопрос-ответ

Какие типы реакций возможны между водородом и оксидами металлов?
Между водородом и оксидами металлов могут происходить различные типы реакций, в зависимости от условий. Например, возможна реакция окисления, при которой водород переходит в состояние ионов гидроксида, а металл в состояние ионов оксида. Также может происходить реакция редукции, при которой водород принимает электроны и переходит в металлическое состояние, а металл окисляется.
Что происходит при реакции окисления водорода с оксидами металлов?
При реакции окисления водорода с оксидами металлов водород переходит в состояние ионов гидроксида, а металл окисляется и переходит в состояние ионов оксида. Например, при реакции между водородом и оксидом железа образуется вода и ион оксида железа. Такие реакции обычно протекают при высоких температурах и/или в присутствии катализаторов.
Как происходит реакция редукции водорода с оксидами металлов?
При реакции редукции водород принимает электроны и переходит в металлическое состояние, а металл окисляется. Например, при реакции между водородом и оксидом меди образуется металлическая медь и вода. Такие реакции могут протекать при комнатной температуре и обычно требуют наличия катализаторов, таких как платина или никель.
Какие факторы могут повлиять на тип реакции между водородом и оксидами металлов?
Факторы, которые могут повлиять на тип реакции между водородом и оксидами металлов, включают температуру, наличие катализаторов, концентрацию веществ, давление и pH-среду. Например, при высоких температурах и наличии катализаторов реакции окисления могут протекать быстрее, а при низких температурах и без катализаторов может происходить реакция редукции.
