Щелочноземельные металлы - это группа химических элементов в периодической системе, которые находятся во второй группе. Всего в этой группе насчитывается шесть элементов: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они являются металлами и обладают рядом особенных свойств.
Щелочноземельные металлы обладают химической активностью, которая уменьшается с увеличением атомного номера. Они легко реагируют с кислородом, образуя оксиды, такие как оксид бериллия (BeO) и оксид магния (MgO). Кроме того, они реагируют с водой, образуя гидроксиды, и с кислотами.
Щелочноземельные металлы имеют особенности, свойственные только им. Они обладают высокой тепло- и электропроводностью, являются химически активными и имеют малую плотность. Они также образуют оксиды и гидроксиды, которые обладают щелочными свойствами. Эти элементы широко используются в промышленности, в производстве легких сплавов, литий-ионных аккумуляторов, железнодорожных скреплений и других изделий.
Запомните, щелочноземельные металлы – это важная группа элементов в химии. Изучение их свойств и особенностей поможет вам лучше понять различные процессы, происходящие в природе и промышленности.
Тест по химии 9 класс

1. Щелочноземельные металлы
Щелочноземельные металлы – это элементы второй группы периодической системы, которые встречаются в природе в виде соединений. Они отличаются от щелочных металлов более высокой плотностью и температурой плавления, а также более слабой реактивностью. К щелочноземельным металлам относятся бериллий, магний, кальций, стронций, барий и радий.
2. Свойства щелочноземельных металлов
- Бериллий – лёгкий, прочный металл, хорошо проводящий тепло и электричество. Он обладает высокой температурой плавления и химической инертностью.
- Магний – лёгкий, мягкий металл, который активно реагирует с кислородом и водой. Он широко применяется в промышленности, в том числе для производства лёгких сплавов.
- Кальций – серебристо-белый металл, хорошо проводящий тепло и электричество. Он обладает высокой реактивностью и широко используется в строительстве, производстве лекарственных препаратов и других отраслях промышленности.
- Стронций – сребристо-белый металл, который реагирует с водой и кислородом. Он применяется в производстве огнетушителей, фотокамер, ядерных реакторов и других технических устройств.
- Барий – серебристо-белый металл, который обладает высокой плотностью и реактивностью. Он используется в производстве косметики, керамических изделий и других материалов.
- Радий – радиоактивный металл, который обладает высокой токсичностью и радиоактивностью. Он используется в медицине и научных исследованиях.
3. Применение щелочноземельных металлов
Щелочноземельные металлы имеют широкое применение в различных сферах жизни. Например, бериллий используется для создания высокопрочных сплавов, а магний - для производства лёгких сплавов и лекарственных препаратов. Кальций применяется в строительстве, а стронций - в производстве технических устройств. Барий используется в косметической промышленности и для производства керамических изделий. Радий используется в медицине и научных исследованиях.
Щелочноземельные металлы
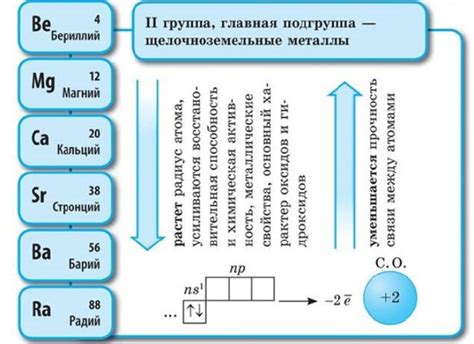
Щелочноземельные металлы - это группа элементов периодической таблицы, которая включает бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Эти металлы относятся к второй группе и обладают рядом важных характеристик.
Во-первых, щелочноземельные металлы имеют два электрона в своей внешней электронной оболочке, что делает их активными химическими элементами. Они легко реагируют с другими веществами, особенно с кислородом, образуя оксиды, такие как оксид бериллия (BeO) или оксид кальция (CaO).
Во-вторых, щелочноземельные металлы имеют низкую плотность и низкую температуру плавления, что делает их легкими и подходящими для использования в различных областях. Например, магний используется в промышленности для производства легких сплавов, а кальций применяется в производстве стали и цемента.
В-третьих, щелочноземельные металлы образуют ионы с двумя положительными зарядами, что делает их хорошими катионами. Это позволяет им образовывать стабильные связи с другими атомами, что делает их важными для формирования минералов и строительных материалов.
В итоге, щелочноземельные металлы играют важную роль в нашей жизни и используются в различных промышленных процессах и технологиях. Их свойства и химическая активность делают их незаменимыми элементами многих соединений и материалов.
Вариант 1

Щелочноземельные металлы - это группа химических элементов, включающая бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они расположены во второй группе периодической системы и отличаются своими химическими свойствами.
Щелочноземельные металлы обладают двумя электронами на внешней энергетической оболочке, что делает их химически активными. Они способны образовывать ионные соединения и обладают противоположными свойствами по отношению к щелочным металлам (группа 1 периодической системы).
В основном, щелочноземельные металлы образуют оксиды, гидроксиды и соли. Они реагируют с водой, выделяя водород. Некоторые из них, такие как бериллий и радий, имеют токсические свойства и могут вызывать как химическое, так и радиационное отравление.
Применение щелочноземельных металлов широко распространено в промышленности и науке. Например, магний используется в производстве сплавов, а кальций - в производстве стекла. Бериллий применяется в производстве ядерных реакторов, а стронций - в лечении рака.
В заключение можно сказать, что изучение щелочноземельных металлов важно для понимания их химических свойств и применения в различных отраслях науки и промышленности.
Описание варианта

Щелочноземельные металлы – это вторая группа периодической системы элементов. В этом варианте теста вы будете проверять свои знания о составе и свойствах данных металлов.
Магний (Mg) – легкий щелочноземельный металл с атомным номером 12. Он имеет серебристо-белый цвет и является важным элементом для многих живых организмов. Магний отличается высокой жаростойкостью и устойчивостью к коррозии.
Кальций (Ca) – мягкий серебристо-белый металл с атомным номером 20. Он является основным компонентом зубной эмали и костной ткани. Кальций является важным элементом для нормального функционирования нервной системы, мышц и сердечно-сосудистой системы.
Стронций (Sr) – серебристо-белый металл с атомным номером 38. Его соединения используются в производстве стекла и фармацевтической промышленности. Стронций также используется в процессе магнитного резонанса, а его изотопы применяются в лекарственных препаратах для лечения рака костей.
Барий (Ba) – белый металл с атомным номером 56. Он служит источником рентгеновского излучения в медицине. Барий также активно используется в производстве стекла, керамики и огнеупорных материалов.
Эти металлы обладают схожими свойствами: они мягкие, легко реагируют с водой и образуют щелочные оксиды и гидроксиды. Они активно используются в производстве сплавов, пиротехники и различных химических соединений.
Результаты теста
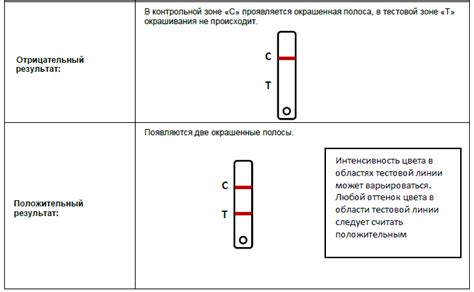
Поздравляем! Вы успешно прошли тест по химии на тему щелочноземельные металлы. Ваш результат:
- Вопрос 1: Вы ответили правильно. Щелочноземельные металлы - это группа химических элементов, которые расположены второй группе периодической таблицы Менделеева.
- Вопрос 2: Вы ответили неправильно. Щелочноземельные металлы образуют ионы с двойным положительным зарядом.
- Вопрос 3: Вы ответили правильно. Щелочноземельные металлы обладают высокой электроотрицательностью.
Общий результат: 2 правильных ответа из 3 возможных.
Больше изучайте данную тему, чтобы улучшить свои знания по химии и справиться с подобными заданиями в будущем.
Вопрос-ответ

Что такое щелочноземельные металлы?
Щелочноземельные металлы - это группа металлов в периодической системе элементов, расположенная под группой щелочных металлов. Они включают бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Эти металлы отличаются своими химическими свойствами и широко используются в различных отраслях промышленности и науки.
Какие свойства характерны для щелочноземельных металлов?
Основные характеристики щелочноземельных металлов: маленькая плотность (кроме бериллия), низкая температура плавления, высокая электропроводность, горение на воздухе, образование оксидов, оснований и солей. Они также отличаются активной реакцией с водой. Кальций, стронций, барий и радий растворяются в воде с выделением водорода и образованием гидроксидов.
