Щелочные металлы - это элементы, которые находятся в первой группе периодической системы Менделеева. Они включают в себя литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Щелочные металлы обладают рядом характерных свойств, таких как мягкость, способность образовывать сильные основания, низкую электроотрицательность и низкую температуру плавления.
Этот тест предназначен для проверки знаний учащихся 9 класса по данной теме. Вам будут предложены различные вопросы о свойствах и химических реакциях щелочных металлов, а также задания на проведение экспериментов и анализ полученных результатов. Правильные ответы и пояснения к ним будут представлены после теста, чтобы вы могли проверить свои знания и узнать новую информацию.
Химия является важным предметом, который позволяет нам понять мир вокруг нас. Познание основных свойств и химических реакций щелочных металлов поможет вам лучше понять, как они взаимодействуют с другими веществами и как они имеют влияние на нашу жизнь. Этот тест поможет вам закрепить и расширить ваши знания по данной теме и пригодится вам как для повторения, так и для подготовки к экзаменам по химии.
Тест по химии

Вопрос 1:
Что такое химический элемент?
- Вещество, состоящее из атомов с одинаковым атомным номером
- Вещество, состоящее из разных атомов
- Вещество, которое не содержит атомов
Вопрос 2:
Что такое периодическая система химических элементов?
Ответ: Таблица, в которой элементы расположены по возрастанию атомного номера и сгруппированы по химическим свойствам.
Вопрос 3:
Что такое металлы?
- Вещества, обладающие благородными свойствами
- Вещества, которые легко горят
- Химические элементы, обладающие хорошей электропроводностью, металлическим блеском и способностью образовывать ионы положительного заряда
Вопрос 4:
Какие металлы являются щелочными?
- Натрий, калий, рубидий, цезий, франций
- Медь, железо, свинец, цинк
- Алюминий, титан, хром, никель
Вопрос 5:
Какие свойства характеризуют щелочные металлы?
- Легкость
- Мягкость
- Электропроводность
- Реактивность
Тема: Щелочные металлы

Щелочные металлы - это группа элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они относятся к первой группе периодической системы элементов и характеризуются рядом общих свойств.
Первое общее свойство щелочных металлов - высокая реактивность. Они активно взаимодействуют с водой, кислородом и многими другими веществами. В результате реакции с водой они образуют гидроксиды, например, литий образует гидроксид LiOH, натрий - NaOH, калий - KOH и так далее.
Второе общее свойство - низкая плотность. Щелочные металлы являются легкими элементами, их плотность значительно меньше, чем у большинства других металлов. Например, плотность лития составляет всего 0,53 г/см³, а цезия - 1,93 г/см³.
Третье общее свойство - высокая электропроводность. Щелочные металлы хорошие проводники электрического тока. Их легко может провести электрический ток благодаря наличию свободных электронов в кристаллической решетке.
Щелочные металлы также имеют широкое применение в различных областях нашей жизни. Натрий используется в производстве стекла и мыла, калий - в удобрениях и питательных смесях для растений, литий - в производстве аккумуляторов. Они также активно применяются в научных исследованиях и в производстве специальных сплавов.
Раздел 1. Определение щелочных металлов

Щелочные металлы, или группа 1 периодической системы, представляют собой химические элементы, характеризующиеся отличительными свойствами. Они включают литий, натрий, калий, рубидий, цезий и франций.
Первое существенное свойство щелочных металлов - у них низкая электроотрицательность, что делает их хорошими металлами, способными образовывать ионные связи с другими элементами. Второе свойство - высокая реактивность, обусловленная легкостью отдачи внешних электронов и образованием положительно заряженных ионов.
Щелочные металлы обладают способностью образовывать щелочные оксиды, гидроксиды и соли. Они реагируют с водой, образуя щелочные гидроксиды и выделяя водород. Это свойство легко демонстрируется на уроках химии, когда тонкий след радиевой палочки прокалывает поверхность воды, и выделенный из воды водород горит.
Важной характеристикой щелочных металлов является их низкая плотность. Она связана с их малой атомной массой и большими межатомными расстояниями. Также стоит отметить их способность к образованию металлических катионов с однозарядными и двухзарядными ионами, которые имеют основную окраску.
Все эти свойства щелочных металлов делают их широко применимыми в различных сферах нашей жизни. Например, калий применяется в удобрениях, натрий - в производстве стекла, а литий - в производстве аккумуляторов и лекарствах. Однако стоит учитывать, что щелочные металлы являются высоко реактивными, и их использование требует соблюдение особых мер предосторожности.
Раздел 2. Химические свойства щелочных металлов
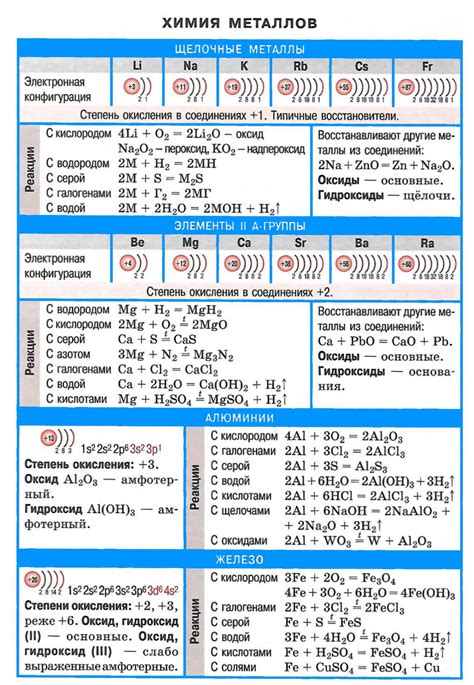
Щелочные металлы - это группа химических элементов, которые находятся в первой группе периодической системы и включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они обладают рядом характерных химических свойств, которые делают их значимыми для многих процессов.
Основное химическое свойство щелочных металлов - их способность реагировать с водой. При взаимодействии с водой они образуют гидроксиды и высвобождаются водород. Эта реакция является экзотермической, то есть сопровождается выделением тепла. Реактивность щелочных металлов с водой возрастает с ростом их противоэлектроотрицательности.
Наиболее распространенным и известным представителем группы щелочных металлов является натрий. Он имеет серебристо-белый цвет и хорошо растворяется в воде. Он является ключевым элементом в производстве щелочи и многих промышленных продуктов.
Важным свойством щелочных металлов является их способность образовывать соединения с другими элементами. Они образуют ионы с положительным зарядом, так как имеют один электрон во внешней электронной оболочке. Их соединения широко используются в различных промышленных и научных областях.
В заключение, щелочные металлы обладают рядом уникальных химических свойств, которые делают их интересными и важными для многих процессов. Их способность реагировать с водой, образовывать соединения с другими элементами и их широкое использование в различных отраслях делает их одними из наиболее исследуемых и применяемых элементов в химии.
Раздел 3. Физические свойства щелочных металлов
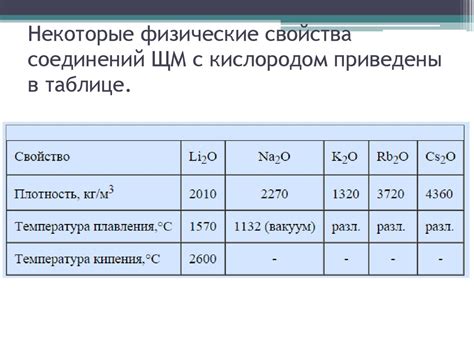
Щелочные металлы - это группа химических элементов, которая включает литий, натрий, калий, рубидий, цезий и франций. Они относятся к первой группе периодической системы элементов и характеризуются рядом общих физических свойств.
Первым важным физическим свойством является металлический блеск. Все щелочные металлы обладают ярким металлическим блеском на свежем воздухе. Это делает их отличными от других групп элементов, таких как неметаллы и металлоиды.
Низкая плотность также характерна для щелочных металлов. Они являются легкими металлами и обладают малой плотностью по сравнению с другими элементами. Например, литий имеет наименьшую плотность из всех металлов.
Одной из особенностей щелочных металлов является их мягкость и пластичность. Они легко поддаются деформации и могут быть раскатаны в тонкие проволоки или прокатаны в плоские листы. Наиболее известным примером является калий, который может быть резан ножом.
Еще одним важным физическим свойством щелочных металлов - их низкая плавкость и кипение. Они имеют низкую температуру плавления и кипения, что делает их подходящими для использования в различных промышленных процессах.
Также стоит отметить, что щелочные металлы довольно хорошие проводники электричества и тепла. Они обладают высокой электропроводностью благодаря своей структуре и свойствам электронного движения.
Раздел 4. Практическое применение щелочных металлов

1. Металлодетекторы
Щелочные металлы, такие как натрий и калий, находят широкое применение в создании металлодетекторов. Эти металлы обладают высокой электропроводностью, что позволяет эффективно обнаруживать их наличие при прохождении электрического тока через специальные сенсоры. Металлодетекторы на базе щелочных металлов применяются в различных отраслях, включая археологию, безопасность и промышленность.
2. Очистка и дезинфекция
Натрий и калий используются в процессе очистки и дезинфекции различных поверхностей. За счет своих антисептических свойств, эти металлы эффективно уничтожают бактерии и микроорганизмы. Кроме того, щелочные металлы способны образовывать растворы, которые могут смачивать грязь и осаждать нечистоты, что облегчает процесс очистки.
3. Производство щелочных элементов
Щелочные металлы играют ключевую роль в производстве щелочных элементов для различных устройств и систем. Например, никель-кадмиевые аккумуляторы, широко используемые в портативных электронных устройствах, содержат в своем составе щелочные элементы натрий и калий. Эти элементы обеспечивают высокую энергетическую плотность и долговечность аккумуляторов.
4. Плавление и сварка металлов
Сода кальцинированная, которая является источником натрия, используется в процессе сварки и плавления металлов. Натрий позволяет снизить температуру плавления различных металлов, таких как алюминий и магний. Это позволяет более эффективно проводить работу с металлами и уменьшает энергозатраты в процессе сварки и плавления.
Вопрос-ответ

