Химические элементы представлены в виде таблицы, известной как периодическая система Менделеева. Эта система включает в себя все известные на данный момент элементы и упорядочена по возрастанию атомного номера. Одним из важных свойств элементов, которые можно найти в периодической таблице, является их классификация на металлы и неметаллы.
Металлы - это элементы, обладающие свойствами твердого тела при комнатной температуре, хорошей проводимостью электричества и тепла, а также блестящей поверхностью. Они обычно имеют низкую электроотрицательность и тенденцию потерять электроны при реакциях.
Неметаллы, наоборот, обладают характеристиками, противоположными металлам. Они обычно находятся в газообразном или жидком состоянии при комнатной температуре, имеют низкую теплопроводность и электропроводность, их поверхность обычно не блестящая. Неметаллы часто образуют соединения с металлами, что является основой для создания различных материалов и соединений.
Знание о металлах и неметаллах является важным в химии и материаловедении. Изучение их свойств и реакций позволяет нам понять и объяснить множество процессов, происходящих в природе и в нашей жизни.
Металлы и металлоиды в таблице химических элементов
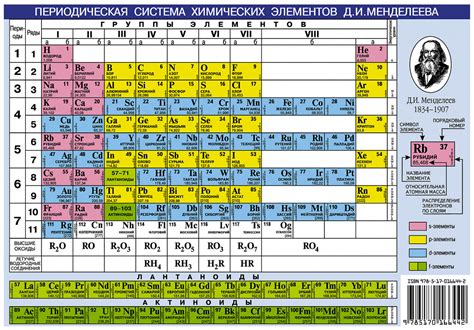
Таблица химических элементов включает в себя различные классы элементов, среди которых наиболее распространены металлы и металлоиды. Металлы являются основными компонентами таблицы и представлены подавляющим большинством элементов.
Металлы обладают такими характеристиками, как блеск, проводимость электричества и тепла, а также прочность и пластичность. Они образуют большую часть периодической системы и относятся к главным группам с 1 по 12.
В таблице химических элементов также присутствуют металлоиды, которые занимают некоторое промежуточное положение между металлами и неметаллами. Металлоиды обладают свойствами, характерными как для металлов, так и для неметаллов.
Некоторые известные металлоиды включают кремний, германий, арсений и антимоний. Они обладают например полупроводниковыми свойствами, используемыми в электронике и промышленности.
Таблица химических элементов является удобным инструментом для изучения различных классов элементов, и включает в себя данные о их свойствах и химической активности. Вся эта информация помогает нам лучше понять и использовать металлы и металлоиды в нашей повседневной жизни.
Металлы в таблице химических элементов
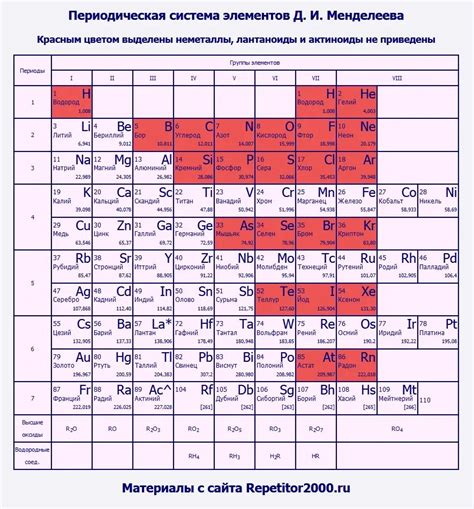
Металлы в таблице химических элементов представлены большим разнообразием и представляют собой большую часть всех элементов таблицы. Они характеризуются своей способностью проводить тепло и электричество, а также обладают блестящей поверхностью.
Металлы обладают высокой пластичностью и способностью к формированию различных структур, что позволяет им быть материалами выбора в различных индустриях, включая машиностроение, электротехнику и металлообработку.
Также металлы проявляют хорошую химическую активность и могут образовывать различные химические соединения. Они обладают разнообразными свойствами, такими как легкость, прочность, коррозионная стойкость и другие, что делает их универсальными материалами для различных применений.
В таблице химических элементов металлы обычно расположены слева, начиная с группы 1 (щелочные металлы) и продолжая до группы 16 (постметаллы). Каждый металл имеет свою уникальную химическую формулу и атомный номер, который определяет его положение в таблице.
Некоторые из наиболее известных металлов, которые можно найти в таблице, включают в себя железо (Fe), алюминий (Al), медь (Cu), свинец (Pb) и золото (Au), а также множество других важных металлических элементов.
Щелочные металлы в таблице химических элементов
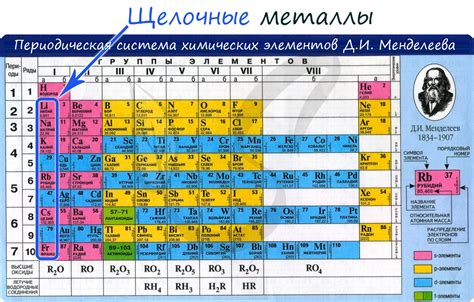
Щелочные металлы – это группа элементов, которые находятся в первой группе таблицы химических элементов. Они характеризуются тем, что имеют один электрон во внешней оболочке своего атома. Все щелочные металлы являются металлами и имеют белый или серебристый цвет.
К группе щелочных металлов относятся элементы литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Все они обладают сходными химическими свойствами, так как имеют одно электронное облако, которое легко участвует в химических реакциях.
Щелочные металлы очень реактивны и легко соединяются с другими элементами. Они образуют ионы с положительным зарядом, поскольку отдают свой один электрон в реакциях с неметаллами или не-металлическими соединениями. Это делает их хорошими основаниями и реагентами для множества химических реакций.
Щелочные металлы активно используются в различных сферах нашей жизни. Например, натрий используется в приготовлении пищи и в производстве стекла, калий является необходимым элементом в почве для роста растений, а литий применяется в литий-ионных аккумуляторах.
Щелочные металлы также являются очень реактивными и опасными веществами при взаимодействии с водой или кислородом, поэтому они хранятся в водонепроницаемых и закрытых контейнерах. Их использование требует осторожности и знания особых мер предосторожности.
Щелочноземельные металлы в таблице химических элементов
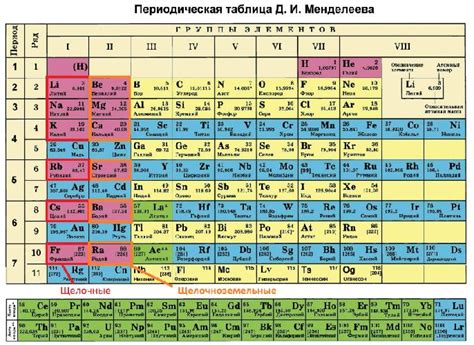
Щелочноземельные металлы - это группа элементов в периодической системе химических элементов, которые находятся во второй группе слева от таблицы. Они включают бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Щелочноземельные металлы обладают общими химическими свойствами, такими как высокая степень реактивности и термической устойчивости. Они являются хорошими проводниками тепла и электричества. Большинство щелочноземельных металлов имеют серебристо-серый цвет и достаточно мягкие.
В таблице химических элементов щелочноземельные металлы представлены внутри группы 2. Они имеют атомные номера от 4 до 12. В периодической системе они представлены в особом блоке, который подсвечен разным цветом для наглядности. Например, бериллий имеет атомный номер 4 и находится в первом столбце, магний имеет атомный номер 12 и находится во втором столбце, и так далее.
Щелочноземельные металлы часто используются в различных областях, включая производство сплавов, строительство, электронику и сельское хозяйство. Бериллий, например, используется в промышленности для создания легких и прочных материалов. Кальций широко распространен в пищевой промышленности и используется для укрепления костей и зубов. Магний используется в производстве автомобилей и в медицине для снятия спазмов и улучшения работы сердечно-сосудистой системы.
Пост-переходные металлы в таблице химических элементов
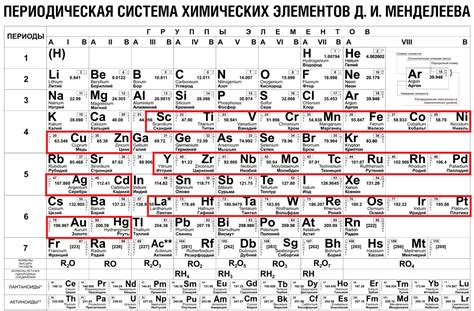
В таблице химических элементов существуют не только металлы и неметаллы, но и группа элементов, которая называется пост-переходными металлами. Они располагаются между блоками металлов и полуметаллов, и их химические свойства находятся между свойствами металлов и неметаллов.
К пост-переходным металлам относятся элементы, находящиеся в блоке п таблицы химических элементов. Они имеют делокализованные электроны в своей внешней электронной оболочке, что придает им свойства как металлов, так и неметаллов.
Пост-переходные металлы обладают различными физическими и химическими свойствами. Некоторые из них являются тяжелыми металлами, обладающими высокой плотностью и тугоплавкостью, например, свинец и бисмут. Другие пост-переходные металлы, такие как галлий и индий, обладают низкой температурой плавления и используются в специальных технологиях и электронике.
Пост-переходные металлы также обладают специфическими химическими свойствами, которые определяются их электронной конфигурацией. Например, цинк и кадмий могут образовывать различные ионы с разными степенями окисления, что дает им возможность проявлять своих свойства в различных химических реакциях.
Важно отметить, что пост-переходные металлы играют значительную роль в промышленности и технологии. Они используются в производстве различных металлических сплавов, аккумуляторах, катализаторах и других материалах, которые находят применение в различных отраслях науки и промышленности.
Металлоиды в таблице химических элементов
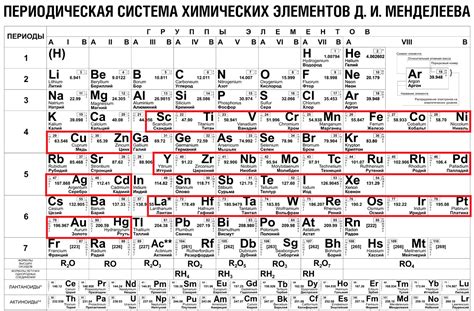
Металлоиды, также известные как полуметаллы или металлоидные элементы, являются группой химических элементов, которые обладают свойствами как металлов, так и неметаллов. Эти элементы находятся между металлами и неметаллами в таблице химических элементов.
Металлоиды обладают специальными свойствами, которые делают их уникальными. Они могут быть полупроводниками электричества и иметь сильную способность варьировать свою электропроводность в зависимости от условий. Также металлоиды обладают высокой температурой плавления и могут образовывать соединения с другими элементами, обладающими различными свойствами.
Примеры металлоидов включают элементы такие как кремний, германий и ятрий. Кремний, например, широко используется в электронике из-за своей способности проводить электричество только в определенных условиях. Германий также используется в технологии полупроводников, а ятрий используется в производстве стекол.
Металлоиды играют важную роль в нашей жизни и технологическом развитии. Благодаря их специальным свойствам и возможностям варьировать свою электропроводность, они широко используются в различных отраслях, таких как электроника, полупроводники, стекловарение и другие области науки и промышленности.
Полуметаллы в таблице химических элементов
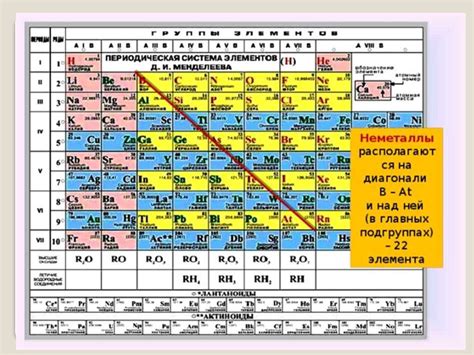
Между металлами и неметаллами находится группа элементов, называемых полуметаллами. Полуметаллы имеют свойства как металлов, так и неметаллов, поэтому они занимают переходную позицию между двумя группами.
Основными полуметаллами, представленными в таблице химических элементов, являются германий (Ge), антимон (Sb), сурьма (Sb) и теллур (Te). Эти элементы обладают хорошей электропроводностью, но также образуют ковалентные связи, характерные для неметаллов.
Полуметаллы играют важную роль в различных отраслях промышленности и науки. Германий широко используется в производстве полупроводников и оптических волокон, антимон применяется в производстве огнеупорных материалов и сплавов. Сурьма используется в производстве пестицидов, а также в солнечных батареях. Теллур применяется в производстве волоконного стекла, пьезоэлектрических устройств и солнечных батарей.
Изучение полуметаллов позволяет расширить наши знания о различных свойствах и химических реакциях элементов. Это помогает ученым разрабатывать новые материалы и технологии для различных отраслей науки и промышленности.
Неметаллы в таблице химических элементов

Неметаллы представляют собой группу элементов, обладающих рядом характеристик, которые делают их противоположностью металлам. В таблице химических элементов неметаллы расположены в верхней правой части, возле крайней правой колонки.
Неметаллы включают в себя такие элементы, как кислород, азот, фосфор, сера, хлор и многие другие. Они обладают особыми физическими и химическими свойствами. Неметаллы обычно хрупкие и не имеют металлического блеска.
Одной из отличительных характеристик неметаллов является их способность к образованию ковалентных связей. Неметаллы, как правило, образуют отрицательные ионы при образовании химических соединений.
Неметаллы играют важную роль во многих сферах жизни. Например, кислород является необходимым для нашего дыхания, азот используется в производстве удобрений, и сера используется в производстве горючих материалов. Неметаллы также широко используются в промышленности, медицине и науке.
В таблице химических элементов неметаллы представлены в виде сокращенных символов и расположены в порядке возрастания атомного номера. На основе этой таблицы можно легко определить химические свойства, вещественное состояние и другие характеристики неметаллов.
Вопрос-ответ

Зачем нужна таблица химических элементов?
Таблица химических элементов является основополагающим инструментом в химии. Она представляет собой удобный способ систематизации и организации информации о химических элементах, их свойствах и характеристиках. Таблица позволяет увидеть логическую структуру химических элементов и помогает понять закономерности и взаимодействия между ними. Это незаменимое средство для химиков, ученых и студентов при изучении и проведении химических экспериментов.
Какие элементы считаются металлами?
Металлами считаются элементы, обладающие характерными физическими и химическими свойствами. Они обычно обладают металлическим блеском, хорошей проводимостью тепла и электричества, высокой пластичностью и твердостью. В таблице химических элементов металлы представлены слева и по середине таблицы.
Что такое неметаллы?
Неметаллы - это химические элементы, обладающие отличными от металлов физическими и химическими свойствами. Они обычно не имеют металлического блеска, плохо проводят тепло и электричество, и часто являются хрупкими. Неметаллы в таблице химических элементов представлены справа и по середине таблицы.
Какие элементы являются самыми известными металлами?
Самыми известными металлами являются железо, алюминий, медь, свинец, золото и серебро. Эти металлы широко используются в различных отраслях промышленности и имеют большое значение в повседневной жизни.
Какие группы элементов находятся на переходе между металлами и неметаллами?
На переходе между металлами и неметаллами находятся такие группы элементов, как полуметаллы или металлоиды. Это элементы, которые обладают свойствами как металлов, так и неметаллов. К ним относятся, например, германий, кремний, антимоний и теллур.
