Концентрированная серная кислота (H2SO4) — одна из наиболее распространенных и химически активных кислот. Взаимодействие этой кислоты с металлами является важным аспектом изучения химических реакций, так как оно может приводить к образованию коррозии, выделению газов и другим химическим превращениям.
Серная кислота обладает сильной окислительной активностью и высокой кислотностью. Она может разрушать металлы, окисляя их до соответствующих солей и выделяя при этом газы. Взаимодействие серной кислоты с металлами может быть описано с помощью так называемой электрохимической серии, которая позволяет определить активность различных металлов по отношению к кислоте.
Приведенная ниже таблица представляет собой обзор взаимодействия концентрированной серной кислоты с различными металлами.
| Металл | Реакция с H2SO4 |
|---|---|
| Алюминий (Al) | Реакция протекает с выделением газа H2 и образованием соли. |
| Цинк (Zn) | Реакция протекает с выделением газа H2 и образованием соли. |
| Железо (Fe) | Реакция протекает с выделением газа H2 и образованием соли. |
| Медь (Cu) | Реакция протекает с выделением газа SO2 и образованием соли. |
Таким образом, взаимодействие концентрированной серной кислоты с металлами может приводить к различным химическим реакциям, в зависимости от активности металла. Эта информация имеет важное практическое значение, так как позволяет предсказать возможность коррозии металлических конструкций и разработать соответствующие меры по их защите.
Реакция металлов на концентрированную серную кислоту

Концентрированная серная кислота (H2SO4) является крайне реакционноспособным веществом и обладает сильно окислительными свойствами. При контакте с металлами происходит химическая реакция, в результате которой образуются соответствующие соли и выделяется водород газ.
Реакция металлов на серную кислоту может протекать с разной степенью интенсивности в зависимости от химических свойств самого металла. Например, щелочные металлы, такие как натрий (Na) и калий (K), активно взаимодействуют с серной кислотой, образуя соответствующие sulfates и выделяя большое количество водорода газа.
- Железо (Fe) образует соединение FeSO4, которое обладает светло-зеленой окраской.
- Медь (Cu), взаимодействуя с серной кислотой, образует соль CuSO4, окрашенную в голубой цвет.
- Алюминий (Al) реагирует с серной кислотой очень интенсивно, выделяя большое количество водорода газа и образуя Al2(SO4)3.
- Свинец (Pb) при взаимодействии с H2SO4 образует PbSO4, обладающий белой окраской.
Не все металлы обладают достаточной активностью для реакции с концентрированной серной кислотой. Например, золото (Au) и платина (Pt) являются химически стойкими металлами и не реагируют с H2SO4.
Взаимодействие металлов с концентрированной серной кислотой может протекать взрывоопасно. При выполнении данного эксперимента необходимо соблюдать все меры предосторожности и проводить его только в специально оборудованных лабораторных условиях.
Химические свойства концентрированной серной кислоты
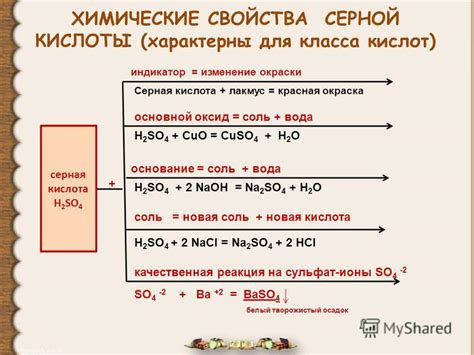
Концентрированная серная кислота – это одно из наиболее сильных оксидирующих и дезоксидирующих веществ, которое обладает рядом химических свойств и реакций.
Одной из главных характеристик серной кислоты является ее кислотность. Она обладает высокой электролитической диссоциацией и позволяет ей реагировать с различными веществами, образуя соли и другие соединения.
Концентрированная серная кислота обладает оксидирующими свойствами. Она способна окислять многие органические и неорганические вещества, в том числе металлы. При взаимодействии с металлами, серная кислота образует соли и выделяет оксид серы.
Кроме того, концентрированная серная кислота проявляет дезоксидирующие свойства. Она способна восстанавливать различные соединения, особенно оксиды. Также серная кислота может действовать как дезоксидант при взаимодействии с многими органическими веществами.
Серная кислота имеет способность образовывать несколько оксоанионов. В зависимости от степени окисления серы, они имеют разную химическую активность и способность образовывать различные соединения с другими элементами.
Серная кислота является также сильным дегидратирующим агентом. Она способна вытягивать из вещества молекулы воды, что приводит к его обезвоживанию и образованию сульфатов.
Взаимодействие концентрированной серной кислоты с металлами описывается в таблице, где представлены химические реакции и образующиеся соединения.
Применение концентрированной серной кислоты в промышленности

Концентрированная серная кислота является важным химическим веществом, широко применяемым в промышленности. Ее использование связано с ее высокой агрессивностью и химической активностью, что позволяет проводить различные процессы обработки и получения конечных продуктов.
Очистка металлов: Серная кислота применяется для очистки различных металлических поверхностей перед нанесением защитных покрытий. Она эффективно удаляет оксидные слои, ржавчину и загрязнения, обеспечивая хорошую адгезию между поверхностью металла и покрытием.
Производство удобрений: Концентрированная серная кислота является важным компонентом для производства различных удобрений. Она используется для синтеза аммиачной селитры, суперфосфата, калийной селитры и других минеральных удобрений. Серная кислота является неотъемлемой частью процесса получения удобрений из природных источников.
Пищевая промышленность: В пищевой промышленности концентрированная серная кислота применяется для регулирования pH продуктов и процессов. Она используется при производстве пищевых добавок, например, виноградной кислоты и лимонной кислоты. Кроме того, серная кислота может использоваться для уничтожения бактерий и микроорганизмов на поверхности продуктов.
Производство химических соединений: Серная кислота служит сырьем для получения многих химических соединений. Например, она используется в производстве салициловой кислоты, аэросилей, полимеров и других соединений. Ее химические свойства позволяют проводить различные реакции с органическими и неорганическими веществами, что делает ее востребованной в химической промышленности.
Полученные продукты путем взаимодействия концентрированной серной кислоты с металлами могут находить применение в различных отраслях промышленности. Благодаря своей высокой активности и агрессивности, серная кислота является важным химическим веществом, способным проводить реакции и обеспечивать необходимые свойства и характеристики конечных продуктов.
Вопрос-ответ

Какой тип взаимодействия происходит между концентрированной серной кислотой и металлами?
Между концентрированной серной кислотой и металлами происходит химическое взаимодействие, при этом происходит образование соответствующих солей и выделение водорода.
Какие металлы реагируют с концентрированной серной кислотой, а какие нет?
Металлы, такие как железо, алюминий, цинк, медь и свинец, реагируют с концентрированной серной кислотой, образуя соответствующие соли и выделяя водород. Однако, металлы, такие как золото, платина и серебро, не реагируют с концентрированной серной кислотой.
Какие металлы реагируют быстрее с концентрированной серной кислотой, а какие медленнее?
Металлы, такие как натрий и калий, реагируют очень быстро с концентрированной серной кислотой и выделяют большое количество водорода. Однако, металлы, такие как железо и медь, реагируют медленнее и выделяют меньшее количество водорода.
