Нитраты металлов - это химические соединения, которые широко используются в различных областях промышленности и науки. Они имеют разнообразные химические свойства, и их разложение может привести к получению ценных продуктов или использованию в различных процессах.
Таблица разложения нитратов металлов представляет собой систематическую схему, которая позволяет определить возможность разложения нитрата металла и получение конкретного продукта. В таблице приведены различные нитраты металлов с указанием их химической формулы и возможного результата разложения.
Разложение нитратов металлов может проходить при нагревании, взаимодействии с другими веществами или под воздействием электролиза. В результате разложения могут образовываться оксиды металлов, оксиды азота, кислород или другие продукты, которые могут быть использованы в производстве различных химических веществ или материалов.
Применение полученных продуктов разложения нитратов металлов может быть очень разнообразным. Например, оксиды металлов могут использоваться в качестве катализаторов в химических процессах, оксиды азота - в производстве удобрений или взрывчатых веществ, а кислород - в медицинской технике или при проведении органических синтезов.
Таблица разложения нитратов металлов является важным инструментом для химиков и научных работников в выборе и оптимизации химических процессов. Она позволяет эффективно использовать нитраты металлов и получать ценные продукты, что способствует развитию химической промышленности и науки в целом.
Нитраты металлов: основные характеристики и классификация
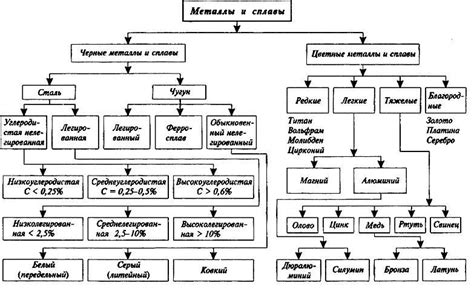
Нитраты металлов – это класс химических соединений, состоящих из металла и нитратного иона NO3-. Нитраты металлов обладают разнообразными свойствами и широко используются в различных отраслях науки и промышленности.
Основные характеристики нитратов металлов:
- Растворимость: большинство нитратов металлов хорошо растворимы в воде, образуя прозрачные растворы.
- Температура плавления: большинство нитратов металлов имеют достаточно низкую температуру плавления, что облегчает их использование в различных процессах.
- Окраска: некоторые нитраты металлов обладают характерной окраской, что может быть использовано для их идентификации и анализа.
- Реакционная способность: нитраты металлов могут проявлять различные реакции, включая окислительные и восстановительные реакции, что делает их полезными в химическом синтезе и аналитической химии.
- Токсичность: некоторые нитраты металлов могут быть ядовитыми и требуют особой осторожности при обращении с ними.
Классификация нитратов металлов:
Нитраты металлов можно классифицировать по различным признакам, включая заряд металла, солевую формулу и химические свойства.
- По заряду металла: нитраты металлов могут быть одновалентными (содержат металл с +1 зарядом), двухвалентными (содержат металл с +2 зарядом) и так далее.
- По солевой формуле: некоторые нитраты металлов могут иметь особую солевую формулу, которая указывает на наличие водной решетки или аниона комплекса.
- По химическим свойствам: некоторые нитраты металлов обладают специфическими химическими свойствами, которые могут быть использованы для их идентификации и отделения от других соединений.
Все эти особенности делают нитраты металлов удобными объектами изучения в химии и имеют важное практическое значение в множестве промышленных процессов и технологий.
Химические свойства нитратов металлов

Нитраты металлов являются солевыми соединениями, образованными отрицательно заряженными нитратными ионами и положительно заряженными ионами металлов. Они обладают рядом уникальных химических свойств, которые определяют их важное место в различных областях науки и промышленности.
Одним из основных свойств нитратов металлов является их растворимость в воде. Большинство нитратов металлов хорошо растворяются в воде, что делает их удобными для использования в различных процессах и реакциях. Растворенные нитраты образуют хорошо проводящие электричество растворы, что позволяет использовать их в электрохимии и производстве электролитов.
Другим важным свойством нитратов металлов является их окислительная активность. Нитраты металлов могут проявлять окислительные свойства при взаимодействии с другими веществами. Например, нитраты металлов могут окислять органические соединения, что находит применение в различных химических реакциях и процессах.
Нитраты металлов также могут быть использованы в качестве удобного источника азота. Ионы нитрата являются доступной формой азота для многих растений и микроорганизмов, что делает нитраты металлов важными компонентами удобрений для сельского хозяйства и растениеводства. Они способствуют росту и развитию растений, что является ключевым фактором в сельском хозяйстве.
Кроме того, некоторые нитраты металлов обладают специфическими свойствами, которые делают их полезными в определенных областях. Например, нитраты металлов могут быть использованы в производстве огнетушителей, фотографических материалов, пиротехнических смесей и даже в медицине для лечения некоторых заболеваний.
В заключение, химические свойства нитратов металлов делают их важными соединениями, которые находят применение в различных областях науки, промышленности и сельском хозяйстве. Растворимость в воде, окислительная активность, удобность в использовании в качестве источника азота, а также специфические свойства делают нитраты металлов универсальными соединениями с широким спектром применения.
Механизм разложения нитратов металлов
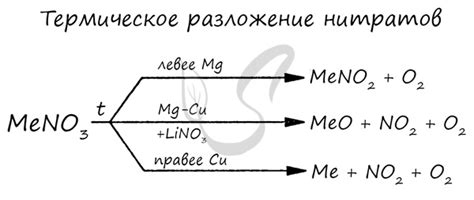
Разложение нитратов металлов происходит в несколько этапов и зависит от специфических химических свойств каждого металла. Однако, основной механизм разложения нитратов металлов включает два основных процесса: термическое разложение и окисление.
Во время термического разложения нитратов металлов, под воздействием высокой температуры, происходит распад нитратной группы на оксид и кислород. Этот процесс может сопровождаться выбросом газов, таких как азотокислоты или оксиды азота. Полученные оксиды металлов обладают различными свойствами и имеют широкое применение в разных областях науки и техники.
Окисление также является важным процессом в разложении нитратов металлов. Окисление происходит в результате взаимодействия нитратных и кислородных групп соединения с окружающей средой. Данный процесс может приводить к образованию окисей металлов с более высокой степенью окисления.
Механизм разложения нитратов металлов является сложным и включает не только термическое разложение и окисление, но и другие факторы, такие как концентрация и состояние окружающей среды, присутствие катализаторов, pH-значение и прочее. Понимание механизма разложения нитратов металлов важно для контроля и оптимизации процессов их синтеза и для развития новых методов получения и применения данных соединений.
Применение таблицы разложения нитратов металлов

Таблица разложения нитратов металлов является важным инструментом в химической лаборатории и применяется в различных областях науки и промышленности.
В аналитической химии таблица разложения нитратов металлов позволяет определить наличие и количество металлов в образце. Путем нагревания образца и наблюдения изменений, можно определить, какие металлы присутствуют в образце и в каком количестве. Такая информация имеет большое значение при анализе различных проб, таких как почва, вода или пищевые продукты, и помогает контролировать качество и безопасность продукции.
Таблица разложения нитратов металлов также широко используется в синтезе химических соединений. Зная свойства нитратов металлов, их разложение можно использовать для получения других соединений. Например, нагревание нитрата металла может привести к образованию оксида металла, который затем может быть использован в различных химических реакциях или в качестве катализатора.
Таблица разложения нитратов металлов также является важным инструментом в фармацевтической и пищевой промышленности. Нитраты металлов могут использоваться в качестве пищевых добавок для консервирования или для придания продукту определенных свойств, например, цвета или вкуса. Зная свойства нитратов металлов, можно контролировать и оптимизировать процессы производства пищевых продуктов и фармацевтических препаратов.
Перспективы исследования нитратов металлов

Нитраты металлов представляют собой особый класс соединений, которые обладают разнообразными химическими свойствами и широким спектром применений. Исследование нитратов металлов открывает новые возможности для развития различных отраслей промышленности и науки.
- Каталитическое применение: нитраты металлов являются важными катализаторами в различных химических реакциях. Исследования в этой области помогают разработать эффективные катализаторы для синтеза различных химических соединений, включая органические соединения и полимеры.
- Энергетическая применимость: изучение нитратов металлов может привести к разработке новых материалов для энергетической промышленности. Например, нитраты металлов могут использоваться в качестве энергоемких материалов для хранения и освобождения энергии.
- Медицинские применения: нитраты металлов также могут найти применение в медицине и фармакологии. Исследования в этой области могут привести к разработке новых препаратов и методов лечения различных заболеваний.
- Экологическая безопасность: исследования нитратов металлов помогают понять их влияние на окружающую среду и разработать способы утилизации и очистки сточных вод, содержащих нитраты металлов.
Таким образом, изучение нитратов металлов имеет огромные перспективы в различных областях, начиная от промышленности и заканчивая медициной. Новые открытия и разработки в этой области могут привести к появлению совершенно новых материалов и методов, которые принесут огромную пользу человечеству.
Вопрос-ответ

Какие металлы могут образовывать нитраты?
Нитраты могут образовываться с многими металлами, включая алюминий, свинец, медь, железо, магний, никель, калий, натрий, серебро и цинк.
Каковы химические свойства нитратов металлов?
Нитраты металлов обычно являются солями, их растворимость в воде обычно высокая. Они обладают окислительными свойствами и могут поддерживать горение.
Для чего используются нитраты металлов?
Нитраты металлов используются в различных отраслях промышленности. Например, они используются в производстве пиротехнических изделий, в производстве взрывчатых веществ, для получения красителей и пигментов, а также в медицине.
Какие из нитратов металлов являются ядовитыми?
Некоторые нитраты металлов, такие как нитраты кадмия и свинца, являются ядовитыми и могут вызывать отравление при попадании в организм. Поэтому необходимо обращать особое внимание на безопасное обращение с этими веществами.
