Металл кальция представляет собой химический элемент, относящийся к группе благородных металлов. Его атомный номер составляет 20, а атомная масса около 40 единиц. Кальций является сравнительно распространенным элементом, встречающимся в земной коре и имеющим множество промышленных применений.
Строение металла кальция можно описать как решетку, состоящую из положительно заряженных ионов кальция и электронов, которые занимают свободные позиции в решетке. Как и другие металлы, кальций обладает металлическим свойством проводить электрический ток и тепло. Это свойство обусловлено наличием свободных электронов, которые могут свободно перемещаться по металлической структуре.
Основной концепцией в строении металла кальция является его кристаллическая структура. Кальций кристаллизуется в кубической решетке, где каждый ион кальция окружен восьмью соседними ионами с отрицательным зарядом. Свободные электроны находятся между ионами кальция и образуют электронное облако. Такая структура позволяет кальцию обладать хорошей пластичностью и прочностью, а также формировать различные связи с другими элементами.
Учитывая свою химическую активность и свободное расположение электронов, металл кальция образует ионы с положительным зарядом, которые легко реагируют с другими элементами и соединяются в различные соединения. Благодаря этим свойствам кальций широко используется в производстве сплавов, в качестве добавки к стали для улучшения ее свойств, а также в производстве цемента и других строительных материалов.
Схема и структура металла кальция: особенности и свойства

Кальций – это щелочноземельный металл, который находится во второй группе периодической таблицы. Его атомный номер равен 20, а атомная масса – 40,08. Кальций известен своей значительной важностью для организма живых организмов, однако металлическая форма этого элемента также имеет свои интересные особенности.
Металл кальция обладает хорошей теплопроводностью и электропроводностью. Эти свойства делают его полезным материалом для различных областей промышленности, включая производство стальных сплавов, алюминия и магния. Кальций также используется в процессе производства цемента, стекла и керамики.
Структура кристаллической решетки металла кальция имеет гранци линейный тип. Она формируется из атомов кальция, которые располагаются в узлах кубической решетки. Такая структура обеспечивает металлу кальция высокую плотность и прочность. Кроме того, кальций обладает характерными металлическими свойствами, такими как пластичность и ударопрочность.
Однако, кальций имеет также свои особенности и недостатки как металл. В чистом виде он очень реактивен и быстро окисляется на воздухе, образуя окись кальция. Это делает его нестабильным и требует особого обращения и хранения. По этой причине кальций обычно используется в виде сплавов, чтобы улучшить его стойкость к окислению и уменьшить его реактивность.
Таким образом, схема и структура металла кальция обладают своими важными особенностями и свойствами, которые определяют его роль и применение в различных отраслях человеческой деятельности.
Исторический обзор открытия и химические свойства кальция

Кальций – это химический элемент с атомным номером 20 и символом Ca. В природе он встречается в виде различных минералов, таких как известняк и мрамор. Кальций был открыт в 1808 году подробнее методом извлечения из его оксида с помощью электролиза, проведенного английским химиком Сиром Хамфримом Дэви. С его помощью была получена чистая форма кальция, которая была белым металлом.
Кальций является активным щелочно-земельным металлом и имеет несколько химических свойств. Он обладает хорошей прочностью и может быть легко деформирован и превращен в различные формы. Кальций реагирует со многими кислотами, образуя соответствующие соли и выделяя водород. Он также может быть использован в качестве восстановителя в химических реакциях и имеет важные производственные применения.
Кальций является необходимым элементом для многих организмов, включая растения и животных. Он играет важную роль в различных биологических процессах, таких как строительство костей и зубов, сократимость мышц и передача нервных импульсов. Недостаток кальция может привести к различным заболеваниям, таким как остеопороз и нарушения свертываемости крови.
- Основные химические свойства кальция:
- Активность: кальций активен и реагирует с водой и кислородом.
- Легкость деформирования: кальций может быть легко деформирован и превращен в различные формы.
- Реакционная способность: кальций реагирует со многими кислотами, образуя соответствующие соли и выделяя водород.
- Восстановительные свойства: кальций может быть использован в качестве восстановителя в химических реакциях.
В целом, кальций является важным химическим элементом с уникальными свойствами и широким спектром применений. Его особенности исследованы в химии и биологии, и его роль в жизнедеятельности организмов продолжает быть исследованной. Кальций имеет несколько полезных свойств и широко применяется в различных отраслях промышленности и медицине.
Кристаллическая структура металла кальция: атомная решетка и кристаллографические особенности
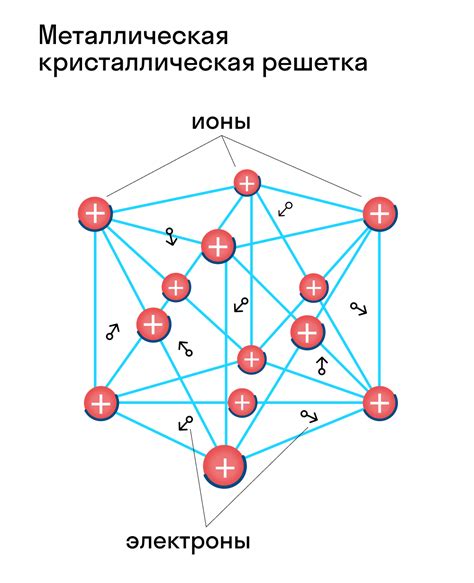
Металл кальций обладает кристаллической структурой, которая представляет собой трехмерную атомную решетку. Каждый атом кальция окружен шестью атомами кислорода, образуя октаэдрический комплекс. Эти октаэдры соединяются друг с другом, образуя кристаллическую решетку, которая характеризуется высокой упорядоченностью и регулярностью.
Кристаллическая структура металла кальция можно описать с помощью кристаллографических осей и плоскостей. Кристаллографическая ось - это вымышленная прямая линия, проходящая через центр атома кальция и пронизывающая всю решетку. Оси могут иметь различное направление и задавать определенное пространственное расположение атомов в кристалле.
Кристаллографические плоскости - это фиктивные плоскости, которые проходят через атомы кальция и делят кристалл на различные части. Плоскости могут быть параллельны друг другу или разделяться определенным углом. Каждая плоскость имеет свой индекс Миллера, который определяет ее положение относительно осей решетки.
Кристаллическая структура металла кальция обладает рядом особенностей. Во-первых, она обладает высокой симметрией, что означает, что решетка выглядит одинаково в любом направлении. Во-вторых, она обладает высокой упакованностью, то есть атомы кальция плотно упакованы в решетке, что объясняет их высокую плотность. В-третьих, кристаллическая структура металла кальция обладает электрической проводимостью, что является характерным свойством металлов.
Физические свойства кальция: плотность, температура плавления и кипения
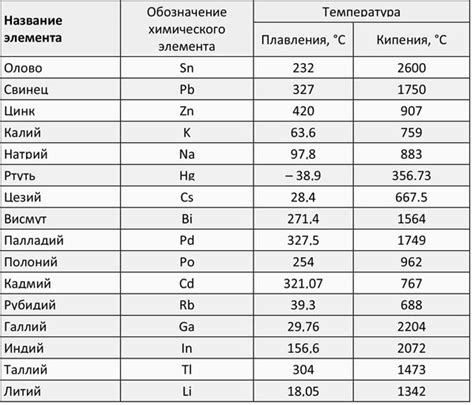
Плотность
Кальций - это химический элемент, который имеет относительно низкую плотность в твердом состоянии. Плотность кальция составляет около 1,55 г/см³. Он является легким металлом с малой массой на единицу объема.
Температура плавления
Кальций обладает низкой температурой плавления, что делает его легким в использовании при промышленном производстве различных материалов. Температура плавления кальция составляет около 842°C. При достижении этой температуры кристаллическая решетка кальция разрушается и вещество переходит из твердого в жидкое состояние.
Температура кипения
Кальций имеет относительно высокую температуру кипения. Его кипение происходит при температуре около 1484°C. При этой температуре металл превращается из жидкого состояния в парообразное.
Особенности взаимодействия кальция с окружающей средой: окисление и реакция с влагой

Кальций – химический элемент, который активно взаимодействует с окружающей средой, проявляя свои уникальные особенности. Одной из таких особенностей является его способность к окислению.
При взаимодействии с кислородом из воздуха кальций мгновенно окисляется, образуя тонкую пленку оксида, которая накапливается на его поверхности. Эта пленка защищает металл от дальнейшего окисления, сохраняя его в инертном состоянии.
Кальций обладает также высокой реактивностью по отношению к влаге. При контакте с водой или влажным воздухом происходит реакция, в результате которой образуется гидроксид кальция. Это соединение обладает амфотерными свойствами и может дополнительно взаимодействовать с другими веществами в окружающей среде.
Также кальций способен реагировать с кислотами, образуя соответствующие соли, и с другими химическими соединениями, что делает его полезным в различных процессах и технологиях.
Использование кальция в промышленности и повседневной жизни: примеры и применение
1. Производство стали:
Кальций широко применяется при производстве стали в виде кальций-кремниевого сплава. Он обладает высокой активностью и способностью дезоксидировать железо, что позволяет улучшить качество и свойства получаемой стали. Кроме того, кальций повышает обработаемость стали, снижает содержание вредных примесей и помогает улучшить вязкость стали при низких температурах.
2. Производство алюминия:
Кальций используется при получении алюминия в виде кальциноальуминатов, которые применяются в алюминиевой промышленности в качестве флюсов для улучшения плавкости и обезжиривания алюминиевых шлаков. Кальциноальуминаты помогают улучшить процесс плавления, снизить энергозатраты и снижают риск образования дефектов в получаемом алюминии.
3. Производство карбида кальция:
Из кальция получают карбид кальция, который имеет широкое применение в промышленности. Карбид кальция используется в производстве ацетилена, карбида кремния, кальция и некоторых других веществ. Ацетилен, получаемый из карбида кальция, используется как промышленное топливо и сырье для синтеза органических соединений, таких как пластик, вещества для синтеза лекарственных препаратов и т.д.
4. Удобрение в сельском хозяйстве:
Кальций используется в сельском хозяйстве в виде различных минеральных удобрений. Он является неотъемлемым элементом для роста и развития растений. Удобрения, содержащие кальций в виде карбонатов, сульфатов и других соединений, помогают улучшить качество и урожайность сельскохозяйственных культур, а также способствуют укреплению структуры почвы и борьбе с некоторыми заболеваниями растений.
5. В производстве специальных сплавов:
Кальций применяется в производстве специальных сплавов, которые используются в различных отраслях промышленности. Например, сплавы с добавлением кальция применяются в авиационной и автомобильной промышленности для улучшения свойств и характеристик металлических изделий, к примеру, для увеличения прочности и упругости.
Кальций является важным и широко применяемым элементом в различных отраслях промышленности и повседневной жизни. Его свойства и способность взаимодействовать с различными веществами делают его незаменимым компонентом в производстве стали, алюминия, карбида кальция, удобрений и специальных сплавов. Благодаря использованию кальция в различных сферах деятельности, достигаются более эффективные процессы и улучшение качества конечной продукции.
Вопрос-ответ

Из чего состоит строение металла кальция?
Строение металла кальция состоит из кристаллической решетки, в которой катионы кальция расположены регулярно и окружены анионами.
Какие особенности присущи строению металла кальция?
Особенности строения металла кальция включают его кристаллическую структуру, взаимное расположение катионов и анионов, а также способность кальция образовывать ионные связи.
Какая схема строения металла кальция?
Схема строения металла кальция представляет собой кристаллическую решетку, в которой каждый ион кальция окружен шестью ионами аниона.
Что можно сказать о расстоянии между ионами кальция в металле?
Расстояние между ионами кальция в металле обычно составляет около 3 Åнгстремов, что является стандартным значением для ионов металлов.
Как взаимодействуют ионы кальция в металле?
Взаимодействие ионов кальция в металле осуществляется через обмен электронами, образуя ионную связь, что обеспечивает устойчивость и прочность структуры металла.
