Исследование связей между атомами в металлах является важным направлением в физико-химической науке и оказывает значительное влияние на различные исследования и технологии. Металлы характеризуются особыми связями между атомами, которые обусловлены их электронной структурой. Металлические связи отличаются от ковалентных и ионных связей, и проявляются в ряде уникальных свойств металлов.
Одной из особенностей металлических связей является возможность электронов свободно перемещаться в кристаллической решетке металла. Это связано с тем, что в металлах валентные электроны не принадлежат отдельным атомам, а формируют так называемое "электронное облако", которое окружает позитивно заряженные атомные ядра. Это облегчает передвижение электронов и позволяет проявиться хорошей электропроводимости и термической проводимости у металлов.
Кроме того, металлические связи характеризуются высокой пластичностью и прочностью материала. Это связано с тем, что электроны могут свободно двигаться в структуре металла и разделяться между соседними атомами. Благодаря этому, металлы имеют способность к деформации без разрушения и обладают высокой ударной прочностью. Кроме того, электроны могут принимать дополнительные энергетические уровни, что способствует легкости создания дефектов в металлической структуре и возможности ковки и отливке металлов.
Исследование связей между атомами в металлах позволяет лучше понять их характеристики и помогает разрабатывать новые сплавы и материалы с улучшенными свойствами. Это изучение не только важно для фундаментальной науки, но и имеет практическое применение в различных отраслях, таких как машиностроение, электроника, аэрокосмическая промышленность и многих других.
Типы связей в металлах

Металлы представляют собой особый класс веществ, в которых атомы образуют определенные типы связей. Основными типами связей в металлах являются металлическая связь, ионная связь и ковалентная связь.
Металлическая связь характеризуется тем, что в металлах электроны перемещаются между атомами, в результате чего образуются положительно заряженные ионные ядра и облако свободных электронов. Это позволяет металлам обладать высокой электропроводностью и теплопроводностью, а также способностью быть гибкими и деформируемыми.
Ионная связь характеризуется тем, что атомы металлов образуют положительно заряженные ионы, которые притягиваются к отрицательно заряженным ионам из других веществ. Это приводит к образованию решетки ионов, взаимодействие которых обеспечивает прочность и твердость металла.
Ковалентная связь характерна для некоторых металлов, в которых атомы образуют молекулярные структуры. В таких металлах атомы связаны между собой с помощью совместно используемых электронных пар. Ковалентная связь обеспечивает высокую прочность и позволяет металлам быть химически стабильными и устойчивыми к коррозии.
Химические особенности связи
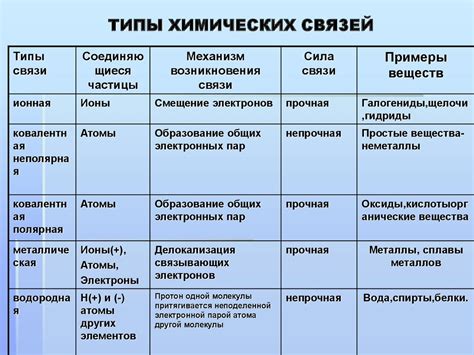
Связь между атомами в металлах отличается от связи, характерной для других веществ. Основными особенностями химической связи в металлах являются металлическая связь и ковалентная связь.
Металлическая связь возникает в результате обмена свободными электронами между атомами металла. В металлах наружные электронные оболочки атомов частично перекрываются, образуя так называемое "электронное море". В этом море электроны могут свободно перемещаться между атомами, что обеспечивает металлам их характерные свойства: высокую электропроводность и теплопроводность.
Ковалентная связь возникает между атомами металла и другими атомами или группами атомов. В ковалентной связи два атома металла делят свои электроны с другими атомами, образуя совместно используемые электронные пары. В результате образуется ковалентная сеть, которая придает металлам определенные химические и физические свойства.
Зависимость химических и физических свойств металлов от особенностей их связи делает возможным создание различных сплавов, имеющих уникальные свойства и применяемых в разных отраслях промышленности.
Физические свойства связи

Связь между атомами в металлах обладает рядом физических свойств, которые определяют их характеристики и поведение. Одним из основных физических свойств связи является электропроводность. Металлы обладают высокой электропроводимостью благодаря наличию свободных электронов, которые легко движутся в кристаллической решетке металла.
Другим важным физическим свойством связи в металлах является теплопроводность. Металлы отличаются высокой теплопроводностью благодаря свободному движению электронов и относительно низкому тепловому сопротивлению. Это делает металлы эффективными материалами для передачи тепла.
Другим важным свойством связи в металлах является пластичность. Металлы обладают способностью к деформации без разрушения благодаря особенностям их связи. Атомы в металлах могут перемещаться, не нарушая связей между соседними атомами, что позволяет металлам изменять форму и удерживать ее.
Кроме того, металлы обладают способностью к диффузии, то есть способности перемещаться в твердом состоянии без изменения своей кристаллической решетки. Это позволяет различным веществам мигрировать через металл, образуя специфические связи и влияя на их механические и химические свойства.
Роль связей в металлической структуре

Одной из основных особенностей металлических структур является наличие межатомных связей, которые играют важную роль в их свойствах и поведении. Металлические связи характеризуются высокой прочностью и эластичностью, что делает металлы прекрасным материалом для строительства, производства инструментов и других промышленных приложений.
Межатомные связи в металлической структуре образуются благодаря перекрытию электронных облаков атомов, что приводит к созданию электронной оболочки, общей для всех атомов в кристаллической решетке. Это обеспечивает высокую подвижность электронов, которые могут свободно перемещаться в металле и обеспечивать проводимость тепла и электричества.
Кроме того, металлические связи также влияют на механические свойства металлов, такие как пластичность и деформационность. Благодаря свободному движению электронов, металлы обладают способностью к деформации без разрушения, что позволяет им быть легко обрабатываемыми и формоваться в различные конструкции и изделия.
Межатомные связи также имеют значительное влияние на физические свойства металлов, такие как температура плавления и кипения. Высокая энергия связи между атомами обуславливает высокую температуру плавления и кипения металлов, что позволяет им быть применяемыми в условиях высоких температур и экстремальных условиях.
В целом, связи в металлической структуре определяют множество уникальных свойств металлов, делая их незаменимыми материалами во многих отраслях промышленности и технологии.
Влияние связей на свойства металлов

Связи между атомами в металлах играют ключевую роль в определении их свойств. Одной из особенностей связей в металлах является наличие свободных электронов, которые образуют "море" электронов внутри металлической решетки.
Это способствует высокой электропроводности металлов, так как свободные электроны легко перемещаются по структуре. Это также объясняет блеск металлов, их способность отражать свет.
Связи в металлах также обуславливают их высокую пластичность и деформируемость. Из-за свободных электронов, атомы металлов могут легко сдвигаться относительно друг друга без разрушения связей.
Важной особенностью связей в металлах является их теплопроводность. Свободные электроны эффективно передают энергию в виде тепла от одних атомов к другим, что делает металлы хорошими проводниками тепла.
Также, связи в металлах влияют на их магнитные свойства. Некоторые металлы обладают спонтанным магнетизмом, который обусловлен ориентацией спинов свободных электронов.
Вопрос-ответ

Какие связи между атомами существуют в металлах?
В металлах существуют металлические связи. Это особого рода прочные и подвижные связи, которые образуются между положительно заряженными ядрами металлических атомов и свободными электронами.
Каковы свойства металлических связей?
Металлические связи обладают рядом особенных свойств: электрическая и теплопроводность, пластичность, распространение света, отсутствие направленности и темная электронная рефлексия. Эти свойства обусловлены специфической структурой металлов и механизмами переноса заряда через металл.
