Металлы - это особая группа элементов, которые обладают рядом уникальных свойств, в том числе при образовании химической связи. В химии металлы часто выступают в качестве доноров электронов, способных образовывать ионы с положительным зарядом или простые молекулы с низкими окислительными состояниями.
Одним из наиболее характерных свойств металлов при образовании химической связи является их способность давать электроны, образуя ионы положительной зарядности. Это происходит благодаря слабой силе притяжения электронов между атомами, что обусловлено их низкой энергией и большими размерами.
Важным аспектом свойств металлов при образовании химической связи является их способность образовывать металлические связи. Это особый тип связей, которые формируются между положительно заряженными ионами металлов и электронами, образующими "облако" вокруг них. Металлические связи обладают высокой прочностью и пластичностью, что делает металлы идеальными для использования в различных технологических процессах и строительстве.
Еще одним важным свойством металлов при образовании химической связи является их способность образовывать сплавы. Сплавы представляют собой материалы, состоящие из двух или более металлов, которые соединены между собой химической связью. Это позволяет получить новые материалы с сочетанием свойств и характеристик, которые недоступны для чистых металлов. Сплавы широко используются в различных отраслях промышленности, включая авиацию, автомобильное производство и строительство.
Таким образом, свойства металлов при образовании химической связи играют ключевую роль в их физических и химических свойствах, а также в широком спектре практического применения в различных индустриальных процессах.
Основные свойства металлов
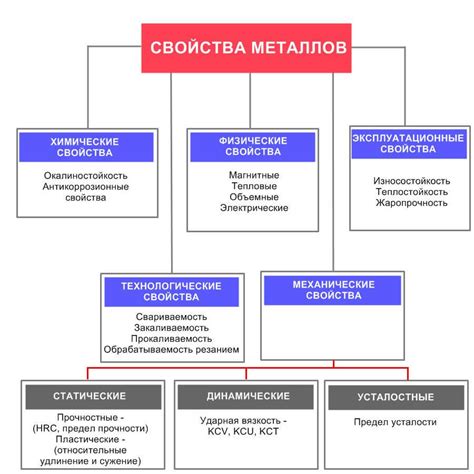
Металлы – это классические элементы, имеющие ряд характерных свойств, отличающих их от других веществ. Вот основные свойства металлов:
- Проводимость электричества и тепла. Металлы обладают высокой электропроводностью и теплопроводностью, что делает их полезными материалами для создания проводников и теплообменных устройств.
- Пластичность и формовываемость. Металлы могут быть легко деформированы без разрушения, что позволяет создавать сложные формы и конструкции.
- Механическая прочность. Большинство металлов обладает высокой прочностью и устойчивостью к механическим нагрузкам, что делает их незаменимыми материалами для строительства и машиностроения.
- Постоянная структура кристаллической решетки. Металлическая решетка имеет регулярную структуру, что обуславливает многие свойства металлов, такие как пластичность и проводимость.
- Химическая реактивность. Металлы обладают способностью образовывать химические соединения с другими элементами, что позволяет им участвовать в различных химических реакциях.
- Глянец и блеск. Металлы обычно имеют характерный блеск и глянец, связанные с их способностью отражать свет.
Все эти свойства делают металлы важными и широко используемыми материалами в различных областях промышленности, науки и повседневной жизни.
Проводимость электричества и тепла

Металлы обладают высокой проводимостью как электричества, так и тепла. Это связано с особенностями их химической связи и структуры.
Электрическая проводимость металлов обусловлена наличием свободных электронов в их структуре. В металлах электроны валентной оболочки отделились от атомов и образовали электронное облако, которое свободно перемещается по кристаллической решетке. Это позволяет электрическому току передаваться без значительных потерь.
Теплопроводность металлов также связана с наличием свободных электронов. При нагревании электроны усиленно движутся и переносят тепловую энергию. Таким образом, металлы хорошо проводят тепло и могут быстро равномерно нагреваться и охлаждаться.
Интересно, что проводимость металлов электричества и тепла связаны между собой. Высокая электрическая проводимость обеспечивает также и высокую теплопроводность. Поэтому металлы широко используются в производстве проводов, контактов и теплообменных элементов.
Пластичность и отличная обработка

Металлы обладают уникальной способностью подвергаться пластической деформации без разрушения связей между атомами. Это свойство называется пластичностью. Благодаря пластичности, металлы можно легко формировать, ковать, выплавлять и вытягивать в различные формы и изделия.
Металлы большинство своих полезных свойств приобретают благодаря предельной пластичности своей кристаллической решетки. При нагревании металлы становятся еще более пластичными и способны принимать различные формы и конфигурации.
Пластичность металлов позволяет легко производить обработку металлических изделий. Их можно сваривать, резать, скручивать, склеивать и применять в различных технологических процессах, таких как литье, штамповка, гибка и вытягивание. Инженеры и дизайнеры широко используют эти свойства, чтобы создавать разнообразные металлические конструкции и детали.
Химическая активность и реактивность
Химическая активность и реактивность - это основные характеристики металлов при образовании химической связи. Они определяют способность металлов вступать в химические реакции и взаимодействовать с другими веществами.
Металлы обладают высокой химической активностью, что обуславливается особенностями электронной структуры атомов. Внешние электроны металлов слабо удерживаются ядром, что делает их легко отделимыми. Это позволяет металлам вступать в реакции окисления и образования ионов положительного заряда.
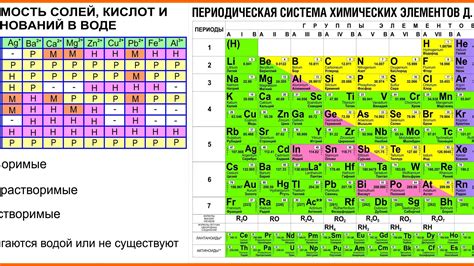
Реактивность металлов также зависит от их положения в периодической системе. Металлы, находящиеся в левой части периодической системы, обычно более активны и реактивны, чем те, что расположены справа. Например, щелочные металлы, такие как натрий и калий, реагируют очень быстро с водой, образуя гидроксиды и выделяя водородный газ.
Однако, не все металлы обладают высокой реактивностью. Некоторые металлы, такие как золото и платина, характеризуются низкой реактивностью и стойкостью к окислению и коррозии. Это связано с их высокой химической инертностью и стабильностью.
В целом, химическая активность и реактивность металлов играют важную роль в их использовании в различных отраслях промышленности, а также в естественных и экологических процессах.
Оптические свойства и блеск

Оптические свойства металлов имеют большое значение в их применении в различных отраслях промышленности и науки. Металлы обладают высокой отражательной способностью, что позволяет им отражать свет и создавать блеск на поверхности. Блеск металлов обусловлен их способностью пропускать и отражать световые волны.
Металлы также имеют интересные оптические свойства, связанные с их электронной структурой. Например, некоторые металлы могут поглощать световые волны определенной частоты и излучать их с другой частотой, создавая яркие цвета. Такие свойства металлов активно используются в производстве красок, покрытий и пигментов.
Благодаря оптическим свойствам металлов, они также находят широкое применение в эстетическом дизайне и ювелирном искусстве. Из металлов создаются украшения и предметы с высоким блеском, которые привлекают внимание своей красотой и роскошью. Блеск металлов придает предметам престижный и нарядный вид.
Механическая прочность и устойчивость

Металлы обладают высокой механической прочностью и устойчивостью к внешним воздействиям благодаря особенностям своей кристаллической структуры. Их атомы располагаются в решетке, образуя кристаллическую решетку. Это позволяет металлам выдерживать большие механические нагрузки и противостоять различным воздействиям.
Кристаллическая решетка металлов хорошо сопротивляется деформациям, обеспечивая им механическую прочность. Благодаря этому, металлы широко используются в строительстве, производстве машин и инструментов. Они способны выдерживать значительные силовые и тепловые нагрузки без разрушения и деформаций.
Металлы также обладают хорошей устойчивостью к коррозии. Их поверхность может быть покрыта оксидным слоем, который предотвращает дальнейшую коррозию и обеспечивает долговечность металлических конструкций. Благодаря этому, металлы могут использоваться в условиях повышенной влажности и агрессивной среды.
Коррозионная стойкость и устойчивость к окружающей среде

Коррозионная стойкость и устойчивость к окружающей среде являются важными свойствами металлов при образовании химической связи. Коррозия – это процесс, при котором металл взаимодействует с окружающей средой и подвергается разрушению в результате химических реакций. Из-за коррозии металлы могут терять свои механические и физические свойства, что приводит к снижению их прочности и долговечности.
Выбор металла с хорошей коррозионной стойкостью играет важную роль при создании различных конструкций, трубопроводов, судов и других объектов. Некоторые металлы, такие как нержавеющие стали и алюминий, обладают высокой устойчивостью к коррозии благодаря своей химической структуре. Они образуют пассивную пленку на своей поверхности, которая защищает металл от воздействия агрессивных сред и электрохимических процессов.
Однако не все металлы обладают хорошей коррозионной стойкостью. Железо и его сплавы, например, подвержены ржавчине при взаимодействии с кислородом и водой, что приводит к разрушению металла. Для защиты от коррозии такие металлы покрывают специальными защитными покрытиями или проводят катодную защиту.
Устойчивость металла к окружающей среде также зависит от конкретных условий, в которых он находится. Например, атмосферная коррозия может быть вызвана дождем, воздушными газами, соленой водой и другими факторами. Морская вода является особенно агрессивной средой для большинства металлов из-за высокого содержания солей и хлорида натрия.
При выборе металла для конкретного применения необходимо учитывать его коррозионную стойкость и устойчивость к окружающей среде. Это поможет обеспечить долговечность и надежность конструкции, а также экономическую эффективность ее эксплуатации.
Вопрос-ответ

Какие свойства металлов влияют на образование химической связи?
Образование химической связи в металлах зависит от таких свойств, как валентность, электроотрицательность, радиус атома, металлическая структура и внешние условия, такие как температура и давление.
Как валентность металлов влияет на образование химической связи?
Валентность металлов определяет число электронов, которые металл может отдать при образовании связи. Чем выше валентность металла, тем больше электронов он может отдать, что облегчает образование связи с другими элементами.
Как радиус атомов металлов влияет на образование химической связи?
Радиус атомов металлов влияет на пространственное расположение атомов в металлической структуре и, следовательно, на возможность образования химической связи. Большие радиусы атомов металлов позволяют свободнее двигаться электронам и создавать более сильные связи с другими элементами.
