Реакция кислорода с металлом является одной из наиболее известных и широко изученных химических реакций. Кислород, благодаря своей электроотрицательности, обладает способностью взаимодействовать с металлами, что приводит к образованию оксидов металлов.
Свойства реакции кислорода с металлом зависят от свойств самих металлов, таких как их активность и степень реактивности. Некоторые металлы, такие как литий и калий, реагируют с кислородом незамедлительно и горят с ярким пламенем. В то время как другие металлы, например, железо или алюминий, медленно окисляются в присутствии кислорода, образуя оксидные слои на своей поверхности.
Реакция кислорода с металлом имеет широкое применение в различных областях науки и промышленности. Эта реакция играет ключевую роль в создании оксидных материалов, которые широко используются в производстве металлических сплавов, керамики, стекла и других материалов. Окислительное действие кислорода также используется в процессах сварки и резки металла, где кислород подается под давлением для организации горения металла и удаления его окалины.
Химическое взаимодействие кислорода с металлами
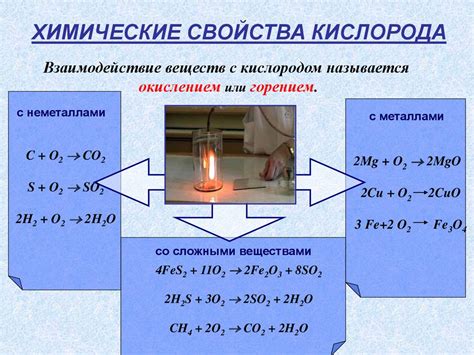
Химическое взаимодействие кислорода с металлами является одним из основных физико-химических процессов, которые происходят в природе. В результате этого взаимодействия образуется металлический оксид. Реакция кислорода с металлами позволяет получать множество важных продуктов, которые используются в различных отраслях промышленности и научных исследованиях.
Оксиды, образующиеся в результате реакции кислорода с металлами, обладают различными свойствами и применяются в различных областях. Например, оксид железа (III), известный как гематит, используется в производстве стали, красок и косметических средств. Оксид магния применяется в производстве огнеупорных материалов, а оксид алюминия - в производстве керамических изделий и алюминиевых сплавов.
Реакция кислорода с металлами также играет важную роль в обеспечении энергетических нужд общества. Например, процесс электролиза воды основан на реакции кислорода с металлами, такими как медь, платина или никель. Электролиз воды позволяет получать водород, который может быть использован в качестве источника энергии или сырья для других химических процессов.
Важно отметить, что взаимодействие кислорода с металлами может приводить к различным реакциям в зависимости от условий. Например, при низких температурах может возникать окисление металла, а при высоких температурах - его горение. Эти реакции являются основой многих технологических процессов, таких как сварка металлов и получение термита.
Химическое взаимодействие кислорода с металлами - важный и широко изучаемый феномен, который имеет множество применений в разных областях науки и промышленности. Благодаря этому взаимодействию мы получаем множество полезных продуктов и развиваем новые технологии, которые помогают нам удовлетворять потребности современного общества.
Свойства реакций

1. Частота реакций: Реакции кислорода с металлами происходят наличии углекислого газа. По этой причине реакции часто протекают в атмосфере, где содержится достаточное количество углекислого газа.
2. Скорость реакций: Реакции кислорода с металлами обычно протекают с высокой скоростью. Многие металлы способны реагировать с кислородом воздуха сразу после контакта. Важным фактором, влияющим на скорость реакции, является площадь поверхности металла, с которой происходит взаимодействие.
3. Изменение свойств металла: Реакция кислорода с металлом приводит к изменению его свойств. Например, железо взаимодействует с кислородом, образуя окислы, что приводит к появлению ржавчины. Как правило, реакции кислорода с металлами приводят к образованию оксидов и гидроксидов.
4. Окислительные свойства: Кислород - сильный окислитель. В реакциях с металлами он обычно выступает в качестве окислителя, передавая электроны металлам и превращая их в положительно заряженные ионы. Кислород способен окислять металлы, образуя ионы металла с более высокой степенью окисления.
5. Применение реакций: Реакции кислорода с металлами имеют различные практические применения. Например, реакция алюминия с кислородом приводит к образованию оксида алюминия, который используется в производстве алюминиевых сплавов и керамических материалов. Реакция железа с кислородом приводит к образованию оксида железа, который используется в производстве стали и магнитов.
Термическое окисление металлов

Термическое окисление металлов – это процесс, при котором металлы вступают в реакцию с кислородом при высоких температурах. В результате этой реакции образуются соединения, называемые оксидами металлов. Термическое окисление происходит с различной интенсивностью в зависимости от химической природы металла.
При термическом окислении металлов образующиеся оксиды часто обладают высокой температурной стабильностью, что делает их полезными во многих технологических процессах. Большинство оксидов металлов имеет высокую термическую проводимость, что обуславливает их применение в производстве теплообменных устройств, например, радиаторов и горелок.
Некоторые оксиды металлов обладают семикратной коэффициентом линейного расширения по сравнению с металлами, из которых они образованы. Это свойство находит применение в производстве термозащитных покрытий для поверхностей, подверженных высоким температурам. Такие покрытия используются, например, в авиационной и аэрокосмической промышленности.
Термическое окисление металлов является неотъемлемой частью процесса гальванического покрытия. Металлические изделия подвергаются окислению в специальных электрохимических реакторах, что позволяет улучшить адгезию между металлом и покрытием, а также защитить поверхность от коррозии.
Использование реакции кислорода с металлом

Реакция кислорода с металлом имеет широкое применение в различных областях. В промышленности она используется для получения металлических оксидов, которые являются важными сырьевыми материалами для производства различных продуктов. Например, оксид алюминия (Al2O3) получают путем сжигания алюминия в кислороде.
Реакция кислорода с металлом также применяется в процессе сварки. При сварке металлов под действием кислорода происходит окисление поверхности металла, что создает эффективную сварочную точку. Также при сварке можно использовать различные сплавы на основе металлов и кислорода для создания качественных сварных соединений.
Другим важным применением реакции кислорода с металлом является использование кислородных установок в медицинской истории. Кислородные установки активно применяются для поддержания дыхания пациентов в случае дыхательной недостаточности. Кислородные баллоны и маски на основе реакции кислорода с металлом позволяют эффективно доставлять кислород в организм человека.
Кроме того, реакция кислорода с металлом используется и в повседневной жизни. Например, при использовании магниевого спичечного кремня, при натирании его о грубую поверхность, происходит реакция такого рода, и зажигается спичка. Алюминиевые противопожарные коврики и одеяла также основаны на реакции кислорода с металлом, в данном случае с алюминием. Это позволяет материалам быстро затухать в случае возгорания и предотвращать распространение огня.
Примеры металлических окислительных реакций
Кислород является одним из самых активных химических элементов и может претерпевать окислительные реакции с различными металлами. Эти реакции могут иметь различные последствия и применения.
Окисление алюминия — одна из наиболее известных окислительных реакций с металлами. При взаимодействии кислорода с алюминием образуется оксид алюминия (Al2O3), который является твердым и химически инертным веществом. Это свойство оксида алюминия позволяет использовать его в производстве керамики, стекла, алюминиевого литья и других промышленных процессах.
Другим примером металлической окислительной реакции является окисление железа. Железо подвергается окислению воздухом и образует оксид железа (Fe2O3), который называется ржавчиной. Ржавчина имеет характерный коричневый цвет и часто используется для создания декоративных эффектов на поверхности металлических предметов.
Еще одним примером металлической окислительной реакции является окисление меди. При взаимодействии кислорода с медью образуется оксид меди (CuO), который имеет черный цвет. Этот оксид можно использовать в качестве катализатора в различных химических процессах.
Таким образом, металлические окислительные реакции с кислородом проявляются в образовании оксидов металлов, которые имеют различные свойства и могут быть использованы в различных отраслях промышленности.
Защита металлов от окисления

Металлы, подвергаясь воздействию кислорода, могут окисляться и терять свои полезные свойства. Окисление металлов может приводить к коррозии и разрушению конструкций. Для защиты металлов от окисления применяются различные методы и материалы.
Один из способов защиты металлов от окисления - нанесение защитных покрытий. Примером такого покрытия может служить оксид, который заполняет поры поверхности металла и создает барьерную защиту от кислорода. Кроме того, могут использоваться специальные краски, лаки или покрытия на основе полимеров.
Другим методом защиты металлов от окисления является использование антикоррозионных покрытий. Эти покрытия содержат в своем составе вещества, способные противостоять воздействию окислителей, например, кислорода. Антикоррозионные покрытия могут быть нанесены на поверхность металла методом покраски, гальваническим покрытием или погружением в специальные растворы.
Кроме того, эффективным методом защиты металлов от окисления является использование антиокислительных веществ. Эти вещества препятствуют реакции окисления металла с кислородом. Они могут добавляться в сплавы при их использовании в производстве, а также быть нанесены на поверхность металла в виде специального покрытия.
Таким образом, существует несколько способов защиты металлов от окисления, включая нанесение защитных покрытий, использование антикоррозионных покрытий и антиокислительных веществ. Эти методы помогают сохранить металлы в хорошем состоянии и продлить их срок службы.
Вопрос-ответ

Что происходит при реакции кислорода с металлом?
При реакции кислорода с металлом образуется металлический оксид. Кислород также может образовывать двуокиси металлов или пероксиды в некоторых случаях.
Какие свойства имеют оксиды металлов, образующиеся в результате реакции с кислородом?
Оксиды металлов обладают рядом свойств, таких как металлический блеск, проводимость электричества и тепла, а также способность образовывать щелочные растворы.
Какие металлы реагируют с кислородом?
Почти все металлы реагируют с кислородом, однако активность этой реакции может различаться. Например, щелочные металлы (литий, натрий, калий) реагируют с кислородом с большей интенсивностью, в то время как платина или золото практически не реагируют с ним.
В каких сферах применяют реакцию кислорода с металлом?
Реакция кислорода с металлом имеет широкий спектр применения. Например, в металлургии она используется для получения металлических оксидов, которые затем могут быть использованы в производстве стекла, керамики и других материалов. Кроме того, в медицине кислород используется для лечения ряда заболеваний и помогает восстановить дыхательные функции пациента.
