Щелочные металлы, включая литий, натрий, калий, рубидий и цезий, являются важными элементами в химической промышленности и научных исследованиях. Одним из основных классов соединений щелочных металлов являются их соли. Они обладают уникальными свойствами, которые делают их неотъемлемыми в различных областях применения.
Соли щелочных металлов обычно обладают высокими температурами плавления и кипения, что делает их идеальными для использования в высокотемпературных процессах, таких как плавление металлов и стекла. Они также обладают хорошей растворимостью в воде, что позволяет использовать их в производстве различных растворов и электролитов.
Одной из главных характеристик солей щелочных металлов является их способность образовывать стабильные кристаллические структуры. Это делает их полезными в производстве кристаллов для электроники, оптики и светодиодов. Кроме того, они также могут быть использованы в производстве катализаторов, используемых в различных химических процессах.
Соли щелочных металлов также обладают высокой электропроводностью, что делает их идеальными для использования в батареях и аккумуляторах. Они могут быть использованы в различных электронных устройствах, включая телефоны, ноутбуки и электромобили. Более того, соли щелочных металлов также имеют медицинское применение, например, в качестве компонентов для производства лекарств и средств для ухода за кожей.
В общем, свойства солей щелочных металлов делают их востребованными в различных областях применения, от промышленных процессов до электроники и медицины. Их уникальные характеристики делают их необходимыми для достижения определенных результатов и развития новых технологий и материалов.
Устойчивость и высокая температура плавления
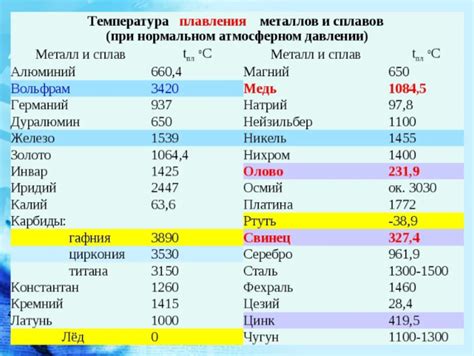
Соли щелочных металлов обладают устойчивостью и высокой температурой плавления, что делает их непревзойденными материалами во многих областях применения. Их химическая структура и кристаллическая решетка обеспечивают устойчивость и прочность при высоких температурах.
Благодаря своей устойчивости, соли щелочных металлов пригодны для использования в процессах, требующих высоких температур, например, в производстве стекла, керамики и специальных покрытий. Они могут выдерживать экстремальные условия и сохранять свои свойства при длительном нагревании.
Температура плавления солей щелочных металлов зависит от их химического состава. Например, хлорид натрия имеет температуру плавления около 800 градусов Цельсия, а карбонат лития - около 618 градусов Цельсия. Это позволяет использовать соли щелочных металлов в различных технологических процессах, где необходимы высокие температуры, такие как плавка металлов или производство электродов.
Электрохимическая активность и проводимость

Соли щелочных металлов обладают высокой электрохимической активностью и проводимостью. Это связано с особенностями их структуры и химическими свойствами, которые обеспечивают быстрое перемещение ионов в растворе или в твердом состоянии.
Электрохимическая активность солей щелочных металлов проявляется в их способности участвовать в реакциях окисления-восстановления. Они могут служить как окислителями, так и восстановителями, образуя соответствующие ионы. В результате этих реакций соли щелочных металлов могут изменять свою состав и химические свойства.
Проводимость солей щелочных металлов определяется их способностью проводить электрический ток в растворе или в твердом состоянии. Это связано с наличием ионов щелочных металлов, которые могут свободно перемещаться под воздействием электрического поля.
Высокая проводимость солей щелочных металлов делает их незаменимыми в различных областях применения. Они широко используются в производстве батареек, электролитов для аккумуляторов, электродных материалов, а также в электрохимических процессах, где требуется быстрый и эффективный перенос зарядов.
Кроме того, соли щелочных металлов играют важную роль в области катализа. Они могут служить активными катализаторами при многих химических реакциях, ускоряя их протекание и повышая эффективность процесса.
Растворимость в различных средах

Соли щелочных металлов обладают уникальной растворимостью в различных средах. Одной из особенностей растворения солей щелочных металлов является их высокая растворимость в воде. За счет ионизации водным раствором, соли щелочных металлов разлагаются на положительно заряженные ионы металла и отрицательно заряженные ионы аниона.
Однако, растворение солей щелочных металлов не ограничивается только водой. Их также можно растворить в других поларных растворителях, таких как спирты и кетоны. В таких растворителях соли образуют однородные растворы, где ионы металла и анионы равномерно распределены.
Кроме того, соли щелочных металлов имеют низкую растворимость в неполярных растворителях, таких как бензин и этиловый эфир. В таких средах формируются неоднородные смеси, где часть соли остается в нерастворимом состоянии.
Каталитические свойства и применение в химической промышленности

Соли щелочных металлов обладают уникальными каталитическими свойствами, что позволяет им находить широкое применение в химической промышленности. Каталитические процессы, выполненные при использовании солей щелочных металлов, отличаются высокой эффективностью и экономичностью.
Одно из наиболее распространенных применений солей щелочных металлов в химической промышленности - каталитическое превращение неорганических и органических соединений. Например, катализаторы на основе солей щелочных металлов могут использоваться в процессах полимеризации, где они значительно повышают скорость реакции и улучшают качество получаемого продукта.
Еще одна область применения солей щелочных металлов - каталитическое окисление и гидрогенирование органических соединений. Благодаря своим каталитическим свойствам, катализаторы на основе солей щелочных металлов позволяют проводить эти процессы при более низких температурах и давлениях, что снижает энергозатраты и повышает эффективность производства.
Кроме того, соли щелочных металлов могут использоваться в качестве катализаторов в процессах синтеза аммиака, синтеза метанола и других важных химических реакций. Их применение в этих процессах позволяет улучшить выборку продукта и повысить качество конечного продукта.
Таким образом, каталитические свойства солей щелочных металлов и их применение в химической промышленности играют важную роль в современных технологиях, повышая эффективность промышленных процессов, снижая их стоимость и улучшая качество окончательных продуктов.
Использование в стекольной и керамической промышленности

Соли щелочных металлов, такие как натрий и калий, находят широкое применение в стекольной и керамической промышленности. Присутствие этих солей в процессе производства помогает достичь определенных свойств материалов и улучшить их качество.
Одним из главных применений солей щелочных металлов в стекольной промышленности является использование их в процессе выплавки стекла. Натрий содержится в основных стеклосоставах и отвечает за устойчивость и прозрачность. Калий также используется в производстве стекла, особенно в стеклоизделиях для лабораторий и химической промышленности.
Соли щелочных металлов играют важную роль и в керамической промышленности. Например, натрий добавляется в глазуровку керамических изделий для придания им прочности и блеска. Калий также применяется в керамике, в частности, для улучшения пластичности глины и поддержания формы изделий в процессе обжига.
Соли щелочных металлов также можно использовать для создания различных цветов и эффектов в стекле и керамике. Например, добавление соединений кобальта или марганца может придать стеклу или керамике синий или фиолетовый оттенок. Также можно использовать соли щелочных металлов для создания эффекта кристаллизации или рассеяния света в материалах.
Применение в медицине и фармацевтической промышленности

Соли щелочных металлов, такие как натрий, калий и литий, широко применяются в медицине и фармацевтической промышленности благодаря своим уникальным свойствам.
Натрий является важным компонентом физиологических растворов, которые применяются для инфузий и капельниц в медицинской практике. Эти растворы содержат натриевые соли, такие как хлорид натрия (NaCl) и лактат натрия (NaC3H5O3), которые помогают поддерживать электролитный баланс организма. Натриевые соли также используются в производстве препаратов, предназначенных для лечения высокого кровяного давления и отечности.
Калий является необходимым микроэлементом для нормального функционирования организма. Калиевые соли применяются в производстве препаратов для лечения недостаточности калия в организме и сердечно-сосудистых заболеваний. Кроме того, калиевые соли используются в процессе производства различных лекарственных форм, таких как таблетки, порошки и растворы, чтобы обеспечить стабильность и улучшить абсорбцию активных компонентов.
Литий является важным препаратом для лечения психических расстройств, таких как биполярное расстройство и депрессия. Литиевые соли, такие как карбонат лития (Li2CO3) и цитрат лития (Li3C6H5O7), снижают активность головного мозга и помогают контролировать настроение пациента. В фармацевтической промышленности литиевые соли используются для создания специальных формул косметических и парфюмерных продуктов благодаря своим уникальным свойствам стабилизации и консервации.
Вопрос-ответ

Какие свойства солей щелочных металлов делают их уникальными?
Соли щелочных металлов обладают рядом уникальных свойств. Одно из них - высокая растворимость в воде. Это делает их прекрасными электролитами, способными проводить электрический ток. Кроме того, соли щелочных металлов обладают низкой температурой плавления, что делает их хорошими компонентами в процессе пайки и сварки. Они также обладают высокой теплопроводностью и хорошей стабильностью в высоких температурах.
Какие области применения имеют соли щелочных металлов?
Соли щелочных металлов имеют широкий спектр применения. Одна из основных областей - это производство стекла и керамики, где они используются в качестве стабилизаторов. Они также используются в процессе очистки воды, в производстве мыла и моющих средств. Соли щелочных металлов применяются в медицине, в производстве лекарственных препаратов, а также как катализаторы в химической промышленности. Кроме того, они используются в светоизлучающих диодах (LED) и аккумуляторах.
Чем соли щелочных металлов отличаются от солей других элементов?
Соли щелочных металлов отличаются от солей других элементов несколькими характеристиками. Во-первых, они обладают низкой температурой плавления, что делает их более подходящими для использования в различных процессах, включая пайку и сварку. Во-вторых, они обладают высокой растворимостью в воде, что делает их прекрасными электролитами. Кроме того, соли щелочных металлов имеют хорошую стабильность при высоких температурах, что делает их полезными в различных процессах нагрева.
Какие особенности имеют соли щелочных металлов в химических реакциях?
Соли щелочных металлов имеют ряд особенностей в химических реакциях. Они легко образуют ионы, которые являются стабильными и активными участниками реакций. Благодаря этому, соли щелочных металлов применяются в качестве катализаторов. Они также могут образовывать комплексные соединения с другими химическими веществами, что расширяет область их применения.
