Металлы являются основными элементами, обладающими хорошей электропроводностью, теплопроводностью и пластичностью. Это связано с особенностями их кристаллической структуры, в которой атомы расположены в виде решетки с деформируемыми промежутками.
При взаимодействии с неметаллами, свойства металлов могут изменяться и проявляться в различных формах.
Окисление – один из наиболее распространенных процессов взаимодействия металлов с неметаллами. Окисление происходит при участии кислорода, который вызывает коррозию металла, приводя к образованию оксидов. Некоторые металлы, такие как алюминий и титан, образуют защитные оксидные пленки, способные предотвратить дальнейшую коррозию.
Гидролиз – еще один способ взаимодействия металлов с неметаллами. Гидролиз заключается в реакции металла с водой, в результате которой образуются соответствующие оксиды или ионы. Например, при взаимодействии натрия с водой образуется гидроксид натрия и выделяется водород.
Взаимодействие металлов с неметаллами может также проявляться в форме образования химических соединений, таких как соли, кислоты и основания, что определяет их важное значение в химической и промышленной сферах.
Влияние металлов на свойства неметаллов

Металлы оказывают существенное влияние на свойства неметаллов, изменяя их химические, физические и механические свойства.
Химическое влияние:
- Металлы могут образовывать с неметаллами соединения, которые могут быть более реактивными или менее реактивными по сравнению со свободными неметаллами. Например, образование оксидов металлов может изменить их окислительные свойства.
- Наличие металлизующих свойств у металлов позволяет им улучшать электропроводность, теплопроводность и магнитные свойства соединений с неметаллами.
Физическое влияние:
- Металлическая структура металлов может влиять на плотность, твердость и температуру плавления неметаллов. Например, добавление металлических примесей в стекло может изменить его светопропускание и оптические свойства.
- Взаимодействие металлов с неметаллами может приводить к изменению ионизации неметалла, что также влияет на его физические свойства, такие как плотность, кристаллическая структура и электронная проводимость.
Механическое влияние:
- Добавление металлов к неметаллам может улучшить их механические свойства, такие как прочность, упругость и твёрдость.
- Некоторые сплавы металлов и неметаллов обладают специфическими свойствами, такими как память формы или сопротивление коррозии, что делает их полезными в различных инженерных и промышленных областях.
Реакционная способность металлов

Реакционная способность металлов – это способность металлов вступать в химические реакции с другими веществами, особенно с неметаллами. Она определяется электронными свойствами металлов, такими как электроотрицательность и электронная структура. Металлы отдают электроны, образуя положительные ионы, что позволяет им взаимодействовать с неметаллами, принимающими электроны.
Некоторые металлы обладают высокой реакционной способностью и могут вступать в химические реакции с различными неметаллами. Например, щелочные металлы (натрий, калий) легко реагируют с кислородом, образуя оксиды металлов. Реакционное взаимодействие металлов с неметаллами может протекать при нормальных условиях или при повышенной температуре и давлении.
Металлы, имеющие высокую реакционную способность, часто используются в промышленности для получения различных химических соединений. Например, натрий и калий используются для получения гидроксида натрия и гидроксида калия, алюминий – для получения оксида алюминия. Реакционная способность металлов также определяет их использование в различных электрохимических процессах, таких как производство аккумуляторов и гальванических элементов.
Последовательность металлов по их реакционной способности с неметаллами составляет химический ряд. В химическом ряду каждый следующий металл имеет большую реакционную способность по сравнению с предыдущим. Например, в ряду литий – натрий – калий – рубидий – цезий – франций, реакционная способность увеличивается от лития к францию.
Электрохимические свойства металлов
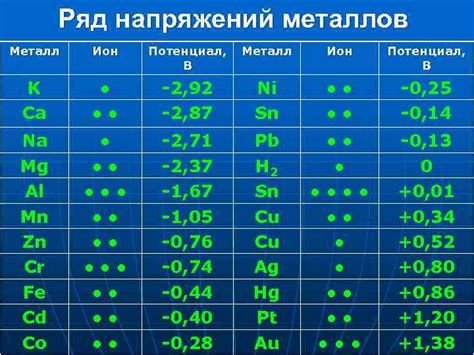
Электрохимические свойства металлов определяются их способностью взаимодействовать с неметаллами и проводить электрический ток. Эти свойства играют важную роль в различных процессах, таких как электролиз, гальваническая коррозия и электрохимические реакции.
Одним из ключевых параметров электрохимических свойств металлов является их электродный потенциал, который определяет их способность отдавать или принимать электроны. Металлы с более низким электродным потенциалом обладают большей склонностью уступать электроны, выступая в роли анодов, в то время как металлы с более высоким потенциалом склонны принимать электроны и выступать в роли катодов.
Электрохимические свойства металлов могут также проявляться в форме окислительно-восстановительной активности. Металлы, обладающие большей активностью, способны легко окисляться и восстанавливаться, образуя разные ионы. Например, некоторые металлы, такие как натрий и калий, реагируют активно с водой, выделяя газы и образуя гидроксиды.
Электрохимические свойства металлов также могут проявляться в виде коррозии. Коррозия – это процесс разрушения металла вследствие его взаимодействия с окружающей средой, в основном влагой и кислородом. Однако, не все металлы коррозируют одинаково. Некоторые металлы, такие как золото и платина, являются коррозионно-стойкими, в то время как другие, такие как железо и алюминий, подвергаются быстрой коррозии.
Важно отметить, что электрохимические свойства металлов могут быть изменены путем добавления различных сплавов или проведения специальной обработки. Например, добавление хрома в сталь позволяет создавать нержавеющую сталь, которая не подвержена коррозии. Также проведение электрохимической обработки может улучшить защитные свойства металла, например, путем нанесения покрытий или проведения анодной окиси.
Термическое взаимодействие металлов с неметаллами

Термическое взаимодействие металлов с неметаллами представляет собой процесс взаимодействия этих двух типов веществ при нагревании. В результате такого взаимодействия происходят различные химические реакции, приводящие к образованию новых веществ с другими свойствами.
Нагревание металла перед реакцией с неметаллом обусловлено тем, что металлы обычно обладают меньшей химической активностью по сравнению с неметаллами. Высокая температура способствует активации химических процессов и повышению скорости реакций.
В результате термического взаимодействия металлов с неметаллами могут образовываться различные соединения, такие как соли, оксиды, карбиды и др. Например, при нагревании железа с серой образуется железная сера (FeS), при нагревании меди с хлором образуется хлорид меди (CuCl2). Такие соединения могут иметь различные свойства и применяться в различных отраслях промышленности и науки.
Термическое взаимодействие металлов с неметаллами является одной из основных методик получения новых веществ и разработки новых материалов. Исследование этого взаимодействия позволяет расширить спектр возможных соединений и применений металлов и неметаллов, а также повысить эффективность процессов воздействия одного типа вещества на другое.
Магнитные свойства металлов

Магнитные свойства металлов рассматриваются в контексте их способности образовывать постоянные или временные магнитные поля и взаимодействия с внешними магнитными полями.
Ферромагнетизм - это основное магнитное свойство некоторых металлов, которое проявляется в том, что они могут взаимодействовать с постоянными магнитными полями и даже сохранять некоторую намагниченность после удаления внешнего магнитного поля.
Одним из самых известных ферромагнитных металлов является железо. Он может быть сильно намагнитен и обладает высокой кривой намагничивания. Железо и его сплавы широко используются в электротехнике, магнитострикционных и магнитных материалах, а также в производстве постоянных и электромагнитных магнитов.
Еще одним металлом с ферромагнитными свойствами является никель. Он обладает высокой намагниченностью и широко используется в производстве магнитов и магнитооптических устройств.
Некоторые металлические сплавы, такие как сплавы железа с никелем (пермаллой), могут быть особенно магнитными и иметь магнитные свойства, превосходящие свойства исходных металлов.
Парамагнетизм - это второе магнитное свойство металлов, которое проявляется в их слабой намагниченности при взаимодействии с внешними магнитными полями. В отсутствие магнитного поля парамагнитные металлы не обладают намагниченностью.
Одним из примеров парамагнитных металлов является алюминий. При наличии магнитного поля он становится слабо намагниченным. Парамагнитные металлы используются в магнитных лабораторных устройствах и медицинской технике.
Диамагнетизм - это третье магнитное свойство металлов, при котором они обладают отрицательной магнитной восприимчивостью, то есть отталкиваются от внешнего магнитного поля.
Одним из примеров диамагнитных металлов является медь. Она слабо взаимодействует с магнитными полями и не проявляет намагниченности.
Таким образом, металлы обладают различными магнитными свойствами, которые могут быть полезными в различных областях, таких как электротехника, медицина и научные исследования.
Фотохимическое взаимодействие металлов с неметаллами

Фотохимическое взаимодействие металлов с неметаллами представляет собой процесс, при котором металлы и неметаллы воздействуют на друг друга под воздействием света. Это взаимодействие возникает в результате фотохимических реакций, когда энергия света используется для активации химических процессов.
В результате фотохимического взаимодействия металлов с неметаллами происходит образование новых веществ. Например, при воздействии света на хлорид меди (CuCl2) происходит фотохимическое окисление хлорида меди до оксида меди (Cu2O). Или, при воздействии света на сульфид железа (FeS2) происходит фотохимическое окисление сульфида железа до оксида железа (Fe2O3).
Одним из примеров фотохимического взаимодействия металлов с неметаллами является фотокаталитическое воздействие титании (TiO2) на органические вещества в присутствии света. В результате этого процесса, органические вещества окисляются до более низких степеней окисления, что позволяет использовать титанию как активный фотокаталитический материал для очистки воды и воздуха.
Фотохимическое взаимодействие металлов с неметаллами имеет широкий спектр применения. Оно используется не только в химической промышленности для получения новых веществ, но и в фотохимической обработке поверхностей, в фотографии, в солнечных батареях и в многих других отраслях науки и техники.
Механические свойства металлов при взаимодействии с неметаллами

Металлы обладают различными механическими свойствами, которые могут изменяться в зависимости от их взаимодействия с неметаллами. Одним из основных свойств металлов является их прочность. Металлы обладают высокой прочностью, что позволяет им выдерживать большие механические нагрузки без деформации или разрушения.
Однако при взаимодействии с неметаллами свойства металлов могут изменяться. Например, при контакте с кислородом металлы могут окисляться, что приводит к образованию оксидов и изменению их механических свойств. Оксиды металлов обладают меньшей прочностью и могут быть хрупкими и легко разрушаться при малейшей нагрузке.
Еще одним важным механическим свойством металлов при взаимодействии с неметаллами является их устойчивость к коррозии. Коррозия - это процесс, при котором металлы подвергаются деструктивному воздействию окружающей среды, что может привести к их разрушению. Некоторые неметаллы, например, кислород или хлориды, способны вызывать коррозию металлов.
Также взаимодействие металлов с неметаллами может приводить к изменению их эластичности. Эластичность - это способность материала возвращаться в исходное состояние после прекращения воздействия механической нагрузки. При взаимодействии с некоторыми неметаллами, металлы могут терять свою эластичность и становиться хрупкими.
Вопрос-ответ

Какие свойства металлов обеспечивают их взаимодействие с неметаллами?
Свойства металлов, обеспечивающие их взаимодействие с неметаллами, включают: высокую электропроводность, высокую теплопроводность, химическую активность, низкую энергию ионизации и возможность образования ионных связей.
Как металлы взаимодействуют с неметаллами при образовании соединений?
Металлы могут взаимодействовать с неметаллами при образовании соединений путем передачи электронов, образуя ионные связи. Металлы отдают электроны, становясь положительно заряженными ионами, в то время как неметаллы получают электроны, становясь отрицательно заряженными ионами.
Какова роль электропроводности металлов в их взаимодействии с неметаллами?
Высокая электропроводность металлов позволяет им передавать электроны неметаллам при образовании соединений. Электроны могут свободно перемещаться между атомами металла, образуя электронный облако, благодаря чему металлы могут отдавать электроны и образовывать ионные связи с неметаллами.
Почему именно металлы обладают химической активностью во взаимодействии с неметаллами?
Металлы обладают высокой химической активностью из-за их низкой энергии ионизации. Низкая энергия ионизации означает, что энергия, необходимая для отделения электрона от атома металла, является относительно низкой. Поэтому металлы легко отдают электроны и вступают в химические реакции с неметаллами.
