Металлы являются одним из основных классов элементов, обладающих уникальными свойствами. Их особенности связаны с их кристаллической структурой и взаимным расположением атомов. Одним из важных характеристик металлов является расстояние между атомами, которое играет важную роль в определении их физических и химических свойств.
Расстояние между атомами в металлах зависит от их кристаллической структуры. Металлическая структура характеризуется наличием регулярного трехмерного распределения атомов внутри кристаллической решетки. Расположение атомов внутри металла определяет его механические и физические свойства, такие как прочность, упругость и проводимость тепла и электричества.
В металлах расстояние между атомами может быть определено с помощью различных методов, таких как рентгеноструктурный анализ и электронная микроскопия. Эти методы позволяют увидеть внутреннюю структуру металла и определить расстояние между атомами с высокой точностью. Исследования показывают, что расстояние между атомами в металлах может колебаться в зависимости от условий синтеза и обработки материала.
Изучение расстояния между атомами в металлах имеет важное практическое значение. Например, зная расстояние между атомами в металле, можно предсказать его химическую реактивность и возможность образования сплавов. Кроме того, правильное расположение атомов внутри металла влияет на его механические и электрические свойства, что необходимо учитывать при разработке новых материалов для различных применений.
В заключение, свойства металлов тесно связаны с их кристаллической структурой и расстоянием между атомами. Знание и понимание этих особенностей помогает разрабатывать новые материалы с определенными свойствами и улучшать уже существующие. Изучение расстояния между атомами в металлах является важной задачей современной материаловедении и помогает расширить наше понимание о свойствах металлов и их использовании в различных отраслях промышленности и науки.
Значение расстояния между атомами для свойств металлов
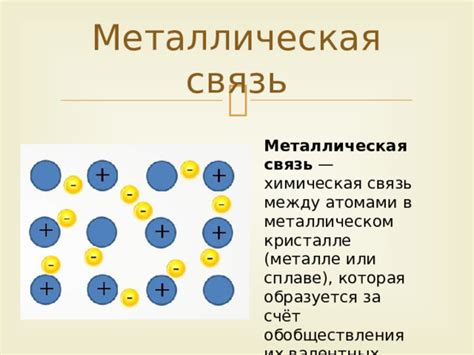
Расстояние между атомами играет важную роль в определении свойств металлов. Оно является одним из ключевых факторов, влияющих на их физические и химические свойства. Расстояние между атомами определяется их атомным радиусом и упорядочением в кристаллической решетке.
Металлы характеризуются высокой проводимостью электричества и тепла, а также металлическим блеском и пластичностью. Одной из причин этих свойств является малое расстояние между атомами в кристаллической решетке металла. Близкое расположение атомов позволяет электронам свободно двигаться по кристаллической решетке, что способствует проводимости электричества и тепла.
Расстояние между атомами также влияет на механические свойства металлов, такие как прочность и текучесть. У металлов с малым расстоянием между атомами силы взаимодействия между атомами значительно выше, что обеспечивает более крепкую и прочную кристаллическую решетку. Это делает металлы устойчивыми к деформациям и позволяет им быть пластичными и легко обрабатываемыми.
В таблице Менделеева указаны атомные радиусы различных элементов. Сравнение этих значений позволяет сделать выводы о расстоянии между атомами в металлах и их соответствующих свойствах. Однако следует отметить, что конкретные значения расстояния между атомами и их влияние на свойства металлов могут варьироваться в зависимости от других факторов, таких как кристаллическая структура и примеси.
Влияние правильного расположения атомов на свойства металлов
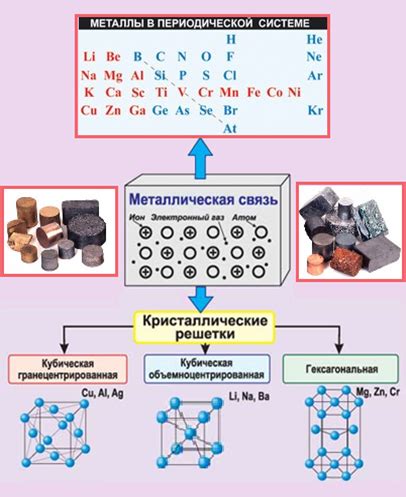
Расстояние между атомами в металлах играет важную роль в их свойствах. Оно определяет плотность и кристаллическую структуру металла. Вещества с более компактной структурой, где атомы расположены ближе друг к другу, обычно обладают высокой плотностью и твердостью. Отличительной особенностью металлов является их способность образовывать кристаллическую решетку, в которой атомы расположены в особым образом.
Правильное расположение атомов в металлах обеспечивает им устойчивость и прочность. Кристаллическая решетка металла формируется таким образом, чтобы каждый атом имел наибольшее число соседей и достиг максимально возможной симметрии. Это позволяет металлам образовывать крепкие связи между атомами и обладать высокой устойчивостью к деформациям и разрушению.
Правильное расположение атомов также влияет на проводимость электричества и тепла. В металлах электрические и тепловые проводимости связаны с наличием свободных электронов, которые могут свободно перемещаться по решетке. Если атомы в решетке не находятся в правильном положении, то свободные электроны могут сталкиваться с препятствиями и проводимость будет снижаться. Правильное расположение атомов позволяет электронам свободно двигаться и обеспечивает высокую электрическую и тепловую проводимость.
Влияние правильного расположения атомов на свойства металлов также проявляется в их пластичности и формоизменяемости. Вещества с компактной кристаллической структурой могут быть легко деформированы под воздействием внешних сил, не разрушаясь при этом. Правильное расположение атомов позволяет металлам обладать высокой пластичностью и способностью к формоизменению, что делает их идеальными материалами для различных промышленных процессов.
В целом, правильное расположение атомов в металлах является ключевым фактором, определяющим их механические и физические свойства. Изучение этого аспекта позволяет лучше понять структуру металлов и разработать новые материалы с улучшенными свойствами.
Факторы, влияющие на расстояние между атомами в металлах

Расстояние между атомами в металлах играет важную роль в их свойствах и характеристиках. Это расстояние зависит от нескольких факторов, которые определяют структуру металлической решетки.
1. Тип металла: Расстояние между атомами в металлах различается в зависимости от их типа. Разные металлы имеют разный радиус атомов, что влияет на расстояние между ними. Например, щелочные металлы имеют большие атомы, поэтому расстояние между ними будет больше, чем у переходных металлов с меньшими атомами.
2. Кристаллическая решетка: Расстояние между атомами также зависит от типа кристаллической решетки металла. В плотных кристаллических решетках, таких как кубические или гексагональные, атомы находятся ближе друг к другу, что приводит к меньшему расстоянию между ними. В то время как в других решетках, например в кубической гранецентрированной или гексагональной ближней упаковке, расстояние между атомами будет больше.
3. Окружающая среда: Расстояние между атомами в металлах также может зависеть от окружающей среды. Например, при изменении давления или температуры, атомы могут продолжать свое движение и перестраиваться, что может привести к изменению расстояния между ними.
4. Деформация и напряжение: Силы деформации и напряжения также могут влиять на расстояние между атомами в металлах. При деформации металла, например при загибе или сжатии, атомы могут приближаться или отдаляться друг от друга, что может изменить расстояние между ними.
Все вышеперечисленные факторы влияют на расстояние между атомами в металлах и могут изменять его значение в зависимости от условий и свойств металла.
Техники контроля правильного расположения атомов в металлах
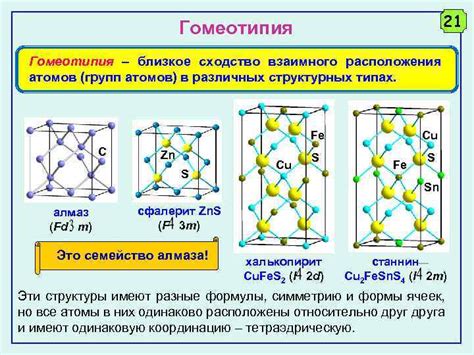
Для обеспечения оптимальных свойств металлов и их использования в различных областях, важно обеспечить правильное расположение атомов в их кристаллической решетке. Существуют различные техники контроля и анализа этого расположения, которые позволяют выявить возможные дефекты и расстройства.
Одной из основных методик является рентгеноструктурный анализ, при котором используется рентгеновское излучение для определения расстояний между атомами в кристаллической решетке. Этот метод позволяет получить детальное представление о структуре металла и выявить нарушения или деформации в атомном расположении.
Второй метод, широко используемый при контроле кристаллической структуры металлов, - это метод электронной микроскопии. Он позволяет непосредственно наблюдать атомные решетки металлов с помощью электронного пучка и создавать изображения с высоким разрешением. Этот метод особенно полезен для анализа наноматериалов и поверхностных дефектов.
Дополнительно используются методы спектроскопии, такие как рентгеновская флуоресценция, которая позволяет определить состав металла и идентифицировать примеси или иные дефекты в структуре. Также применяются методы дифракции, которые позволяют анализировать характеристики дифракционных лучей при прохождении через кристаллическую решетку металла и определять его структуру и кристаллическую симметрию.
Таким образом, техники контроля правильного расположения атомов в металлах играют ключевую роль при исследовании и использовании металлов в различных областях, таких как материаловедение, электроника, катализ и многие другие. Они позволяют выявлять дефекты в атомном расположении, оптимизировать структуру и свойства металлов, а также создавать новые материалы с улучшенными характеристиками.
Применение свойств металлов с учетом расстояния между атомами и правильного расположения

Свойства металлов обусловлены особенностями их структуры и атомного состава. Одно из важных свойств металлов - их твердость, которая определяется правильным расположением атомов и межатомным расстоянием.
Расстояние между атомами в металлах влияет на их механические свойства, такие как прочность и упругость. Правильное расположение атомов обеспечивает оптимальную упаковку, что обуславливает стабильность и прочность металла.
В промышленности свойства металлов, связанные с их структурой, широко используются. Например, благодаря правильному расположению атомов и межатомному расстоянию, металлы обладают высокой прочностью и могут использоваться для создания конструкций, несущих большие нагрузки.
Также, свойства металлов позволяют им проводить электрический ток и тепло. Из-за определенного расстояния между атомами, электроны в металлах свободно движутся, создавая электрическую проводимость. Такое свойство находит широкое применение в электротехнике и электронике.
Кроме того, правильное расположение атомов металлов обуславливает их способность к формированию кристаллической решетки. Благодаря этому, металлы могут быть подвергнуты различным обработкам, таким как прокатка, литье и экструзия, чтобы получить конкретную форму или структуру.
Итак, применение свойств металлов с учетом расстояния между атомами и правильного расположения находит широкий спектр применений в промышленности и науке. Уникальные свойства металлов, обусловленные их структурой, позволяют эффективно использовать их в различных отраслях, будь то машиностроение, электроника или строительство.
Вопрос-ответ

Какое значение имеет расстояние между атомами металла?
Расстояние между атомами в металлах имеет большое значение для их свойств. Это расстояние определяет межатомные взаимодействия и влияет на электронную структуру металла, его физические и химические свойства.
Как правильно располагаются атомы в металлах?
Атомы в металлах располагаются в регулярной кристаллической структуре, называемой решеткой. Эта структура обладает периодичностью и состоит из одинаковых блоков, называемых ячейками решетки. В каждой ячейке решетки находится один или несколько атомов металла.
Какие свойства металлов зависят от правильного расположения атомов?
Правильное расположение атомов металла в решетке имеет важное значение для его свойств. Например, это влияет на механическую прочность металла, его плотность, термическую и электрическую проводимость. Также решетка атомов может влиять на поведение металла при деформации, образовании дефектов и его способностью к образованию соединений.
