Гидриды металлов - это химические соединения между металлами и водородом. Они обладают широким спектром интересных свойств и химических реакций, что делает их особенно важными для изучения и применения в различных областях науки и технологий.
Основным принципом реакций гидридов металлов является их способность к обмену водорода с другими веществами. Как полюсные соединения, гидриды металлов часто выступают в качестве сильных восстановителей в реакциях с оксидами, нитридами и галогенами. Это может приводить к образованию новых соединений и изменению свойств их исходных компонентов.
Возможные реакции гидридов металлов включают спонтанное выделение водорода при контакте с кислотами или водой, а также реакцию с азотом или кислородом при повышенных температурах. Гидриды металлов также могут использоваться в качестве катализаторов при различных химических процессах, таких как производство аммиака или водорода, а также в процессах электролиза.
Гидриды металлов: что это такое?

Гидриды металлов - это химические соединения, состоящие из атомов металла и атомов водорода. Они обладают специфическими свойствами и находят широкое применение как катализаторы, хранители водорода и вещества для проведения различных химических реакций.
Гидриды металлов могут быть разделены на две основные группы: ионные и ковалентные. Ионные гидриды образуются при реакции металла с водородом и могут быть представлены в виде соединений металла с отрицательно заряженным ионом водорода. Ковалентные гидриды образуются при соединении металла с молекулой водорода и имеют более сложную структуру.
Гидриды металлов демонстрируют разнообразные реакции, такие как реакции с водой, кислородом и другими веществами. Некоторые гидриды металлов могут выделять водород при воздействии на них кислород или воду, что делает их ценными для использования в процессах сжигания водорода или водородной энергетике.
Важным свойством гидридов металлов является их способность катализировать различные химические реакции. Например, некоторые гидриды металлов способны катализировать восстановительные реакции, включая реакции синтеза органических соединений или восстановление металлов из их солей. Это делает гидриды металлов важными соединениями для химической промышленности и исследований в области катализа.
Химический состав и структура гидридов металлов
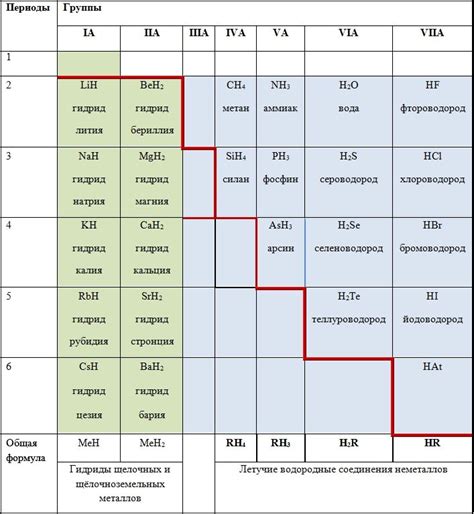
Гидриды металлов – это химические соединения, включающие атомы металла и водорода. Они обладают значительной практической значимостью и широко применяются в различных отраслях промышленности.
Особенностью гидридов металлов является их способность образовывать комплексные структуры. Гидриды металлов могут существовать в различных фазах – от мономолекулярных комплексов до полимерных сетей.
Структура гидридов металлов определяется химическими свойствами и электронной структурой металла. Это включает в себя расположение атомов водорода относительно атомов металла и их взаимодействие. Существует несколько типов структур гидридов металлов, таких как кубическая (fcc), гексагональная (hcp) и гексагональная плотная упаковка (hcp).
Гидриды металлов также могут быть разделены на два основных типа – ионные и координатные. Ионные гидриды характеризуются тем, что атомы водорода передают свои электроны металлу, образуя положительно заряженные ионы металла и отрицательно заряженные ионы гидрида. Координатные гидриды образуются при образовании связи металл-водород, в которой электроны водорода переносятся на атом металла, образуя координационную связь.
Химический состав гидридов металлов может быть различным и зависит от конкретного металла. Некоторые гидриды металлов имеют простой состав (например, MH), в то время как другие могут содержать более одного атома металла (например, MnHm). Более сложные гидриды металлов могут также включать различные типы атомов металла или дополнительные атомы, такие как атомы кислорода или азота.
Изучение химического состава и структуры гидридов металлов является важным для понимания их свойств и возможных реакций. Это позволяет улучшить их применение в различных областях науки и техники, а также способствует развитию новых материалов с улучшенными характеристиками.
Физические свойства гидридов металлов
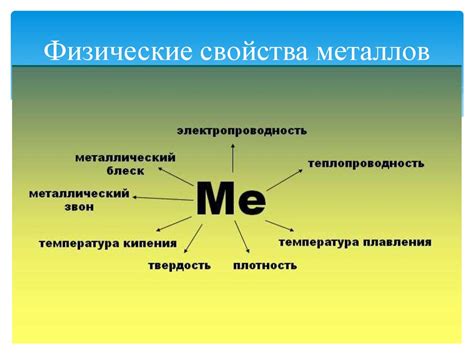
Гидриды металлов являются соединениями металлов с водородом, и их физические свойства зависят от типа и структуры гидрида. Одним из основных физических свойств гидридов металлов является их плотность. Плотность гидридов металлов может быть различной и зависит от состава и структуры соединения.
Также важным физическим свойством гидридов металлов является их температурная стабильность. Некоторые гидриды металлов могут выдерживать высокие температуры без разложения, в то время как другие могут разлагаться при низких температурах или воздействии внешних факторов.
Гидриды металлов могут обладать специфическими физическими свойствами, такими как аморфность или кристалличность. Аморфные гидриды металлов обладают более сложной структурой и обычно имеют более низкую плотность по сравнению с кристаллическими гидридами металлов.
Некоторые гидриды металлов могут обладать магнитными свойствами. Например, некоторые никелевые гидриды обладают ферромагнитными свойствами, что делает их полезными в магнитной технологии и применениях.
Таким образом, физические свойства гидридов металлов определяются их плотностью, температурной стабильностью, структурой и магнитными свойствами. Изучение этих свойств позволяет понять их химическую реактивность и применение в различных областях науки и техники.
Основные принципы реакций гидридов металлов

Гидриды металлов являются химическими соединениями, которые содержат водород и какой-либо металл. Важной особенностью гидридов металлов является их способность к реакциям с различными веществами.
Один из основных принципов реакций гидридов металлов заключается в обмене водорода между гидридом и другими соединениями. Водород может быть передан от гидрида металла к другому соединению, а также наоборот.
Еще одним принципом реакций гидридов металлов является их способность к образованию комплексов с различными органическими и неорганическими молекулами. Это связано с возможностью взаимодействия атомов водорода гидрида с другими атомами.
Важно отметить, что реакции гидридов металлов могут происходить как с образованием новых соединений, так и без образования новых продуктов. При этом могут происходить различные типы реакций, такие как реакции с окислителями, кислотами, основаниями и другими веществами.
В целом, основными принципами реакций гидридов металлов являются обмен водорода с другими соединениями, образование комплексов и возможность происхождения различных типов реакций. Изучение данных принципов позволяет лучше понять и контролировать химические свойства гидридов металлов.
Взаимодействие гидридов металлов с кислородом

Взаимодействие гидридов металлов с кислородом – это процесс, при котором гидридные соединения металлов реагируют с молекулами кислорода, образуя различные продукты.
Реакция гидридов металлов с кислородом может протекать по разным механизмам в зависимости от условий. В одних случаях может происходить окисление металла, при этом гидридная группа приобретает одновременно два атома кислорода, образуя супероксид или пероксидный радикал.
В других случаях взаимодействие гидрида металла с кислородом может приводить к образованию гидроксида металла. Это происходит при реакции гидридно-ме-, кислоты металлов с водой, что приводит к выделению молекулярного водорода и образованию соответствующего гидроксида металла.
Также возможно взаимодействие гидридов металлов с оксидами металлов, что приводит к образованию соответствующего гидрида металла. Этот процесс может протекать при повышенных температурах и давлении и является реверсивным.
Реакции гидридов металлов с водой

Гидриды металлов – химические соединения, в которых водород образует ион H-. Взаимодействие гидридов металлов с водой может протекать различными способами и приводить к образованию различных продуктов.
Одним из типичных примеров реакции гидрида металла с водой является образование гидроксида металла и выделение водорода. Например, реакция гидрида натрия (NaH) с водой приводит к образованию гидроксида натрия (NaOH) и выделению молекул водорода:
2NaH + 2H2O → 2NaOH + H2↑
Также гидриды металлов могут реагировать с водой, образуя кислоты и выделяя водород. Например, реакция гидрида натрия (NaH) с водой может протекать следующим образом:
NaH + H2O → H2 + NaOH
Помимо этого, некоторые гидриды металлов могут реагировать с водой, образуя соединения металла и выделяя водород. Например, реакция гидрида кальция (CaH2) с водой приводит к образованию гидроксида кальция (Ca(OH)2) и выделению водорода:
CaH2 + 2H2O → Ca(OH)2 + 2H2↑
Такие реакции гидридов металлов с водой имеют практическое применение в различных отраслях химии и промышленности, и их изучение позволяет лучше понять химические свойства гидридов металлов и возможные пути их превращения.
Взаимодействие гидридов металлов с кислотами

Взаимодействие гидридов металлов с кислотами является одной из важных реакций, которые могут происходить с данными соединениями. Гидриды металлов, такие как алюминиевый гидрид (AlH3), магниевый гидрид (MgH2) и литиевый гидрид (LiH), обладают высокой степенью восстановительных свойств и способны реагировать с кислотами.
Основной принцип взаимодействия гидридов металлов с кислотами заключается в образовании соответствующих солей металлов и выделении водорода. Гидрид металла действует как восстановитель, отдавая свой водородный атом кислоте и образуя соль металла. Кислота в данном случае активируется за счет наличия свободного водорода, либо других электроотрицательных элементов.
Примеры реакций гидридов металлов с кислотами могут быть следующими:
- Алюминиевый гидрид (AlH3) реагирует с соляной кислотой (HCl), при этом происходит образование хлорида алюминия (AlCl3) и выделение водорода
- Магниевый гидрид (MgH2) реагирует с серной кислотой (H2SO4), образуя сульфат магния (MgSO4) и выделяя водород
- Литиевый гидрид (LiH) реагирует с азотной кислотой (HNO3), образуя нитрат лития (LiNO3) и выделяя водород
Взаимодействие гидридов металлов с кислотами может протекать при обычных условиях температуры и давления, однако для некоторых гидридов требуется добавление катализаторов или повышение температуры для инициирования и ускорения реакции. Эта реакция может быть полезной при производстве водорода для различных промышленных и технических нужд, таких как производство аммиака и полиэтилена.
Реакции гидридов металлов с щелочными металлами

Гидриды металлов являются соединениями, образованными металлами и водородом. Они обладают различными физическими и химическими свойствами, и одной из интересных их особенностей является возможность реагировать с щелочными металлами.
При взаимодействии гидрида металла и щелочного металла происходит замещение водорода на металл щелочного элемента. Такие реакции могут быть проведены как в присутствии растворителя, так и в газообразной фазе.
Примером реакции гидрида металла с щелочным металлом является реакция гидрида натрия (NaH) с литием (Li). При этом образуется гидрид лития (LiH) и металлический натрий (Na). Эта реакция может протекать при нагревании или при воздействии на гидриды электрическим разрядом.
Реакция гидридов металлов с щелочными металлами может использоваться для получения новых соединений. Например, такая реакция может привести к образованию нитридов или карбидов, которые обладают особыми химическими и физическими свойствами и широко используются в различных отраслях науки и промышленности.
Примеры применения гидридов металлов в промышленности
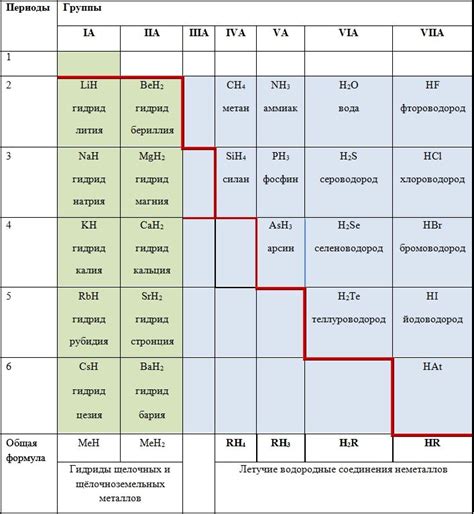
Гидриды металлов являются важными компонентами ряда процессов в промышленности благодаря своим уникальным химическим свойствам. Ниже приведены примеры их применения в различных отраслях:
1. Хранение и перенос водорода: Гидриды металлов широко используются для хранения и переноса водорода в разных отраслях. Они обладают способностью поглощать и выделять водород, что делает их отличным вариантом для использования в топливных элементах, водородных батареях и системах водородного хранения.
2. Синтез органических соединений: Гидриды металлов играют важную роль в процессе синтеза органических соединений. Они применяются в качестве катализаторов при превращении одних органических соединений в другие, а также при гидрировании двойных и тройных связей в органических молекулах.
3. Производство полупроводниковых материалов: Гидриды металлов являются важными компонентами в производстве полупроводниковых материалов. Они используются для получения определенных тонкопленочных материалов, которые необходимы для производства полупроводниковых приборов, таких как транзисторы и солнечные батареи.
4. Металлургия и обработка металлов: Гидриды металлов применяются в металлургии и обработке металлов для осуществления различных химических процессов. Они используются в качестве веществ для дегазации металлов, улучшения их механических свойств, а также для создания покрытий на металлических поверхностях.
5. Производство катализаторов: Гидриды металлов широко используются в производстве катализаторов различного назначения. Они обеспечивают высокую активность и стабильность катализаторов, что позволяет эффективно проводить различные химические реакции, такие как окисление, гидрирование и дезгидрирование.
Это лишь некоторые примеры применения гидридов металлов в промышленности. Благодаря своим особым химическим свойствам, они находят применение во многих других отраслях, таких как электроэнергетика, автомобильная промышленность, пищевая промышленность и многие другие.
Вопрос-ответ

Какие металлы могут образовывать гидриды?
Гидриды могут образовываться у многих металлов, таких как натрий, литий, кальций, магний, алюминий, железо и другие. Все зависит от их электрохимических свойств и способности образовывать связи с водородом.
Какие реакции могут происходить с гидридами металлов?
С гидридами металлов могут происходить различные реакции. Одна из основных реакций - это реакция с водой, при которой образуется водород. Также гидриды металлов могут реагировать с кислородом, азотом, серой и другими элементами в зависимости от своего состава и свойств металла.
Какие свойства имеют гидриды металлов?
Гидриды металлов обладают рядом особых свойств. Они обычно являются твердыми веществами с высокой температурой плавления и кипения. Многие гидриды металлов обладают металлическим блеском и проводят электричество. Кроме того, они могут образовывать структуры с различными типами связей между атомами металла и водорода.
Какие принципы лежат в основе реакций гидридов металлов?
Основными принципами реакций гидридов металлов являются способность металла образовывать связи с водородом и его электрохимические свойства. В реакциях гидридов металлов также играют роль концентрация водорода, температура, давление и растворители.
