Свинец является одним из самых распространенных химических элементов на Земле. Он имеет атомный номер 82 и обозначается символом Pb (от латинского слова plumbum). Свинец находится в группе 14 периодической таблицы элементов и относится к блоку p. Этот металл характеризуется низкой температурой плавления (327,5 градуса Цельсия), что делает его одним из самых плавких металлов.
Одной из особенностей свинца является его химическая инертность. В невозбужденном состоянии свинец практически не взаимодействует с водой, кислотами или щелочами. Однако, он способен образовывать различные соединения с другими элементами. Например, свинец образует соединения с серой, азотом, кислородом и другими неметаллами.
Благодаря своим химическим свойствам, свинец имеет широкое применение в индустрии. Он используется в производстве аккумуляторов, плакировочных материалов, пластиков, кабельной оболочки, косметических средств и других множестве изделий. Свинец также активно применяется в строительстве, в частности, при производстве кровельных материалов и противопожарных дверей.
Химические свойства свинца:

Свинец — химический элемент с атомным номером 82 и символом Pb (от латинского Plumbum). Этот мягкий металл имеет особенные химические свойства, которые находят широкое применение в различных отраслях промышленности.
Реакция со воздухом: Свинец активно взаимодействует с воздухом, образуя покрытие оксида на поверхности металла. Это защищает свинец от окисления и коррозии.
Химическая активность: Свинец обладает низкой химической активностью, что делает его устойчивым к воздействию многих химических веществ. Однако свинец реагирует с некоторыми кислотами и щелочами, образуя соли.
Инертность к воде: Свинец практически не взаимодействует с водой, что делает его хорошим материалом для создания водостойких изделий.
Сплавляемость: Одно из основных свойств свинца — низкая температура его плавления. При 327,5 градусах Цельсия свинец становится жидким. Это делает его идеальным материалом для припоя и других сплавов.
Применение: Мягкость, низкая сплавляемость и высокая стабильность делают свинец ценным материалом для производства аккумуляторов, припоев, кабельных оболочек, пулевого граната и других изделий.
Особенности химических свойств

Свинец - это мягкий и тугоплавкий металл, который обладает рядом уникальных химических свойств.
Во-первых, свинец химически довольно стабилен и практически не реагирует с водой и воздухом при обычных условиях. Эта особенность делает его устойчивым к коррозии и окислению, что делает его идеальным для использования в различных областях, таких как в строительстве, производстве аккумуляторов и снаряжении для забора и хранения питьевой воды.
Во-вторых, свинец обладает способностью образовывать различные соединения с другими элементами. Одним из наиболее известных соединений свинца является оксид свинца (PbO), который широко используется в стеклянной промышленности для придания стеклу различных свойств, таких как прозрачность и цветность.
Кроме того, свинец также может образовывать соединения с другими металлами, в результате чего получаются сплавы. Например, сплав свинца с оловом называется припоем и используется в паяльных работах и производстве электроники.
И наконец, свинец также обладает токсичными свойствами и может накапливаться в организме, что может вызвать серьезные проблемы со здоровьем. По этой причине свинец и многие его соединения сейчас ограничены в использовании и заменены менее опасными альтернативными материалами.
Взаимодействие свинца с кислотами

Свинец, являясь тяжелым металлом, проявляет реактивность при взаимодействии с кислотами. Это обусловлено его способностью образовывать соли с различными кислотами.
Свинец реагирует с минеральными кислотами, такими как серная, соляная и азотная, образуя соответствующие соли. Например, при взаимодействии соляной кислоты со свинцом образуется хлорид свинца (II), который широко используется в химической промышленности для получения оксидов и ацетата свинца.
Кроме того, свинец реагирует с органическими кислотами. Одной из наиболее распространенных реакций является взаимодействие свинца с уксусной кислотой, при которой образуется ацетат свинца. Этот соединение широко используется в производстве керосина, пластмасс и пропиленоксида.
В целом, взаимодействие свинца с кислотами играет важную роль в промышленности и науке, позволяя получать различные соединения свинца с желаемыми свойствами и применением.
Способность свинца образовывать сплавы

Свинец - мягкий и пластичный металл, который обладает уникальной способностью образовывать сплавы с другими металлами. Эта особенность делает свинец незаменимым материалом во многих отраслях промышленности.
Сплавы свинца широко используются в производстве паяльных сплавов, которые применяются при пайке электронных компонентов. Благодаря своей низкой температуре плавления, такие сплавы позволяют соединять электронные элементы без их повреждения.
Также свинцовые сплавы используются при создании аккумуляторов. Сплавы, содержащие свинец, обладают высокой плотностью, что позволяет хранить большое количество энергии. Благодаря этому, аккумуляторы с свинцовыми сплавами применяются в автономных источниках электропитания, бесперебойных источниках питания и других энергосистемах.
Кроме того, свинец широко применяется в производстве охлаждающих жидкостей для радиаторов автомобилей. Сплавы свинца в сочетании с другими материалами обеспечивают высокую эффективность отвода тепла, что позволяет поддерживать оптимальную температуру двигателя.
В искусстве также используют сплавы свинца. Они применяются для изготовления оловянных скульптур и медалей. Благодаря своей пластичности, свинец позволяет создавать сложные формы и детали с высокой детализацией.
Реакция свинца с водой и паром

Свинец – реактивный металл, который проявляет химическую активность во взаимодействии с водой и паром. При контакте с водой, свинец медленно растворяется, образуя сложные ионы и гидроксид свинца. Этот процесс протекает медленно и нестабильно, поэтому растворение свинца в воде происходит с отчетливым пузырьковым выделением газа в виде мельчайших частиц.
Между тем, взаимодействие свинца с паром происходит при повышенных температурах. При нагревании свинца до кипения, он реагирует с паром воздуха, образуя оксид свинца (II). Эта реакция сопровождается образованием характерного белого дыма, состоящего из мельчайших частиц оксида свинца.
Реакция свинца с водой и паром применяется в различных областях. В металлургической промышленности, свинец часто используется при производстве сплавов, таких как оловянные сплавы. Реакция свинца с водой и паром играет важную роль при получении качественной продукции.
Кроме того, реакция свинца с водой может использоваться в химическом анализе для определения наличия данного металла в веществах. Однако, взаимодействие свинца с водой и паром требует контроля и специальных условий, так как реакция может быть негативно нацелена, особенно в виде выделения токсичных газов.
Свойства свинца в присутствии других элементов
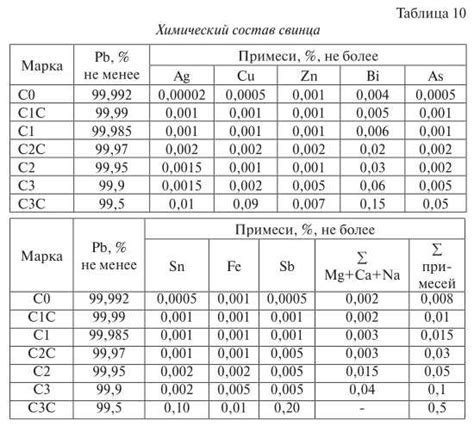
Свинец находит широкое применение в различных отраслях промышленности благодаря своим уникальным химическим свойствам. Когда свинец взаимодействует с другими элементами, образуются различные соединения, которые могут иметь особые свойства и применения.
Смеси свинца с различными металлами, такими как алюминий, медь и серебро, образуют сплавы с пониженной температурой плавления и повышенной прочностью. Например, сплав свинца с алюминием и медью известен под названием паяльная припой, который широко используется в электронной промышленности для соединения компонентов и плат.
В присутствии кислорода свинец образует оксиды, которые могут использоваться в производстве стекла и керамики. Особенно популярен оксид свинца (IV), также известный как сурьма, который используется в производстве стекла с высоким показателем преломления, линз и оптических приборов.
Свинец также может вступать в реакции с серой, образуя сульфиды, которые обладают хорошей тепло- и электропроводностью. Это делает их полезными в производстве аккумуляторов и других электронных устройств.
Нельзя не упомянуть о свойствах свинца в газообразном состоянии. В присутствии хлора свинец может образовывать токсичные соединения, такие как хлорид свинца(II), которые используются в качестве пестицида и убийцы вредителей в сельском хозяйстве и промышленности.
Таким образом, свинец при взаимодействии с другими элементами проявляет широкий спектр химических свойств, что делает его полезным и разнообразным материалом для множества промышленных и научных приложений.
Применение свинца в промышленности

Свинец является одним из наиболее распространенных металлов в промышленности благодаря своим уникальным химическим свойствам. Он обладает высокой плотностью, низкой температурой плавления и легкой обрабатываемостью.
Одним из основных применений свинца является производство аккумуляторных батарей. Свинец используется в производстве пластин для электродов, а также в качестве компонента паяльных сплавов. Батарейки на основе свинцовых аккумуляторов используются в автомобильной и промышленной отраслях, а также в бытовой электронике.
Свинец также широко применяется в производстве свинцовых труб и соединительных деталей, которые используются в системах водоснабжения и отопления. Это связано с его высокой устойчивостью к коррозии и возможностью легкого формирования.
Еще одним важным применением свинца является его использование в производстве покрытий для электрических кабелей и проводов. Эти покрытия обеспечивают хорошую электропроводность и защищают от воздействия окружающей среды.
Кроме того, свинец используется в производстве пневматических шаров, заливки пробок для винных бутылок, шариков для письменных ручек и ряде других промышленных изделий.
Таким образом, свинец является незаменимым материалом во многих отраслях промышленности благодаря своим уникальным свойствам и возможностям для множества применений.
Защита от токсичности свинца

Свинец — высокотоксичный металл, поэтому необходимо принимать меры для защиты организма от его негативного воздействия. Важно помнить, что свинец может накапливаться в организме со временем, поэтому профилактические меры имеют особое значение.
Одной из главных рекомендаций для защиты от токсичности свинца является избежание контакта с этим металлом. Необходимо воздерживаться от употребления продуктов, которые могут содержать свинец (например, рыбу из загрязненных водоемов). Также следует избегать длительного пребывания в помещениях, где находятся старые окрашенные поверхности или изделия, содержащие свинец.
Особое внимание необходимо уделить детям и беременным женщинам, так как они являются наиболее уязвимыми к токсичности свинца. Врачи рекомендуют ограничить или полностью исключить контакт с этим металлом во время беременности и во время грудного вскармливания.
Помимо этого, важно придерживаться здорового образа жизни и укреплять иммунитет. Правильное питание, включающее продукты, богатые кальцием, железом и витамином С, поможет организму более эффективно бороться с токсичностью свинца. Также рекомендуется регулярно проводить детоксикацию организма и употреблять в пищу пищевые добавки, которые способствуют выводу тяжелых металлов из организма.
Вопрос-ответ

Какие основные химические свойства имеет свинец?
Свинец - мягкий металл с атмосферной коррозией, обладает низкой теплопроводностью и плохо проводит электричество. Также свинец является химически инертным металлом, устойчив к окислению и не реагирует с кислородом воздуха.
Какие сферы применения имеет свинец?
Свинец находит широкое применение в различных отраслях промышленности, таких как: производство аккумуляторов, пайка и припой, производство свинцовых сплавов, использование в качестве радиоопакного вещества в медицине, производство стекла и керамики.
Какие реакции свинца с другими веществами известны?
Свинец способен реагировать с различными кислотами, образуя соли свинца. Также свинец реагирует с галогенами, образуя свинцовые галогениды. В реакции с кислородом, свинец образует оксид свинца(II) и оксид свинца(IV).
