Металлы являются одной из основных групп химических элементов, имеющих особые свойства и широкое применение в различных областях нашей жизни. Эти материалы обладают высокой электропроводностью, прочностью, пластичностью и способностью отражать свет, что делает их идеальными для использования в машиностроении, электротехнике, строительстве и других отраслях промышленности.
Одной из ключевых особенностей металлов является наличие кристаллической решетки ионов или атомов. Кристаллическая решетка представляет собой упорядоченную структуру, в которой ионы или атомы металла расположены в определенном порядке. Эта структура обеспечивает металлам их уникальные свойства и дает им возможность выдерживать большие нагрузки и сохранять форму при воздействии силы.
В кристаллической решетке металлов ионы или атомы образуют группы, которые связаны между собой ковалентными или металлическими связями. Эти связи обеспечивают металлам их прочность и пластичность, позволяя им деформироваться без разрушения и восстанавливаться после деформации. Такая способность металлов к деформации позволяет им быть идеальными материалами для изготовления различных конструкций и деталей.
Исследование свойств кристаллической решетки ионов и атомов металлов позволяет нам лучше понять их уникальные свойства и использовать их в различных областях нашей жизни. Такие исследования также способствуют разработке новых материалов с улучшенными свойствами и расширению границ применения металлов в различных сферах. Благодаря этому, металлы продолжают быть одними из самых важных материалов в современной промышленности и науке.
Структура металлов: кристаллическая решетка
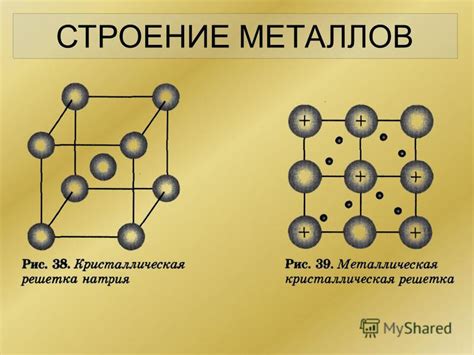
Металлы обладают особым строением, называемым кристаллической решеткой. Кристаллическая решетка представляет собой регулярное упорядоченное распределение атомов или ионов в кристалле. Она является основной причиной многих свойств металлов.
Металлы имеют кубическую кристаллическую решетку, где каждый атом окружен своими соседними атомами. Характерным свойством металлической решетки является наличие электронов свободных от атомов, называемых свободными электронами.
Свободные электроны могут легко передвигаться по кристаллической решетке металла, образуя электрический ток. Благодаря этому металлы обладают высокой электропроводностью. Кроме того, свободные электроны отражают световые волны, что обуславливает блестящую поверхность металлов.
Кристаллическая решетка металлов также определяет их механические свойства. Атомы или ионы в металлической решетке образуют прочные связи, что позволяет металлам выдерживать большие механические нагрузки без разрушения. Благодаря этой особенности, металлы обладают высокой прочностью и жесткостью.
Особенности кристаллической решетки металлов
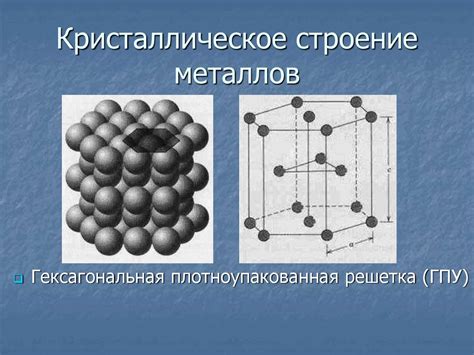
Металлы обладают особым типом кристаллической решетки, которая обусловлена особенностями расположения ионов или атомов внутри металлической структуры. Одним из главных свойств кристаллической решетки металлов является их большая толерантность к деформации.
Кристаллическая решетка металлов включает в себя слои ионов или атомов, которые упорядочены и расположены в пространстве. В металлах состояние решетки обусловлено наличием свободных электронов. Эти электроны образуют электронное облако, которое "плавает" между ионами или атомами металла.
Особенностью кристаллической решетки металлов является высокая плотность и компактность. Ионы или атомы металла располагаются близко друг к другу, что обеспечивает высокую плотность вещества. Кристаллическая решетка обладает также высокой упругостью и прочностью, что делает металлы одними из самых прочных материалов.
Кристаллическая решетка металлов также обладает высокой электропроводностью. Это связано с тем, что свободные электроны, находящиеся в решетке металла, могут свободно перемещаться под действием электрического поля. Именно благодаря свободным электронам металлы являются хорошими проводниками электричества.
Свойства металлической решетки
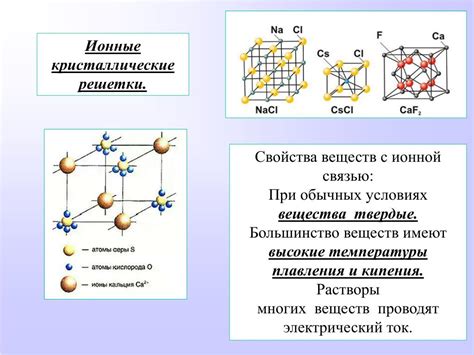
Металлы обладают особым типом кристаллической решетки, называемой металлической решеткой. Она отличается от решетки ионов и атомов в других типах кристаллов.
В металлической решетке атомы или ионы располагаются в виде регулярных решеток. Кристаллическая решетка металлов характеризуется наличием свободных электронов, которые между собой образуют электронное облако. Это облако положительно заряжено и создает особое состояние, называемое электронным газом.
В результате наличия электронного газа, металлы обладают рядом уникальных свойств. Одно из них - высокая электропроводность. Электроны в металлической решетке могут легко передвигаться от одного атома к другому, что позволяет металлам являться хорошими проводниками электричества.
Кроме того, металлы обладают высокой теплопроводностью. Электроны в металлической решетке также могут легко передвигаться, что позволяет металлам передавать тепло эффективно.
В металлической решетке также происходит явление металлической связи, которое обуславливает такие свойства металлов, как пластичность и прочность. Благодаря наличию свободных электронов, атомы металлов могут сдвигаться относительно друг друга без нарушения решетки, что придает металлам способность к деформации и формированию различных структур.
Резюмируя, свойства металлической решетки обусловлены наличием свободных электронов, которые образуют электронное облако. Это облако создает положительное заряженное окружение и обуславливает высокую электропроводность, теплопроводность, металлическую связь и другие характеристики, типичные для металлов.
Физические свойства металлов
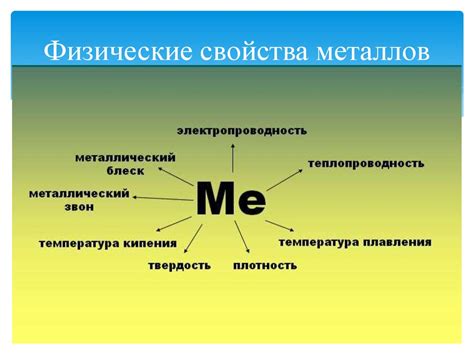
Металлы обладают рядом уникальных физических свойств, которые делают их незаменимыми в различных сферах промышленности и науки.
Первое важное свойство металлов - высокая тепло- и электропроводность. Это объясняется наличием свободных электронов, которые легко перемещаются по кристаллической решетке металла.
Еще одно характерное свойство металлов - их способность принимать любую форму и сохранять ее при кристаллизации. Эта пластичность достигается благодаря отсутствию строгой связи между ионами или атомами в кристаллической решетке.
Металлы обладают также высокой механической прочностью, что позволяет им выдерживать большие нагрузки без разрушения. Это свойство обусловлено хорошим сцеплением ионов или атомов внутри металлической решетки, а также высокой плотностью упаковки атомов в кристалле.
Среди других характерных свойств металлов можно выделить их высокую плотность, яркий блеск и отсутствие прозрачности для видимого света. Кроме того, металлы обладают высокой температурой плавления и кипения, что позволяет использовать их в процессах, связанных с высокими температурами.
Механические свойства металлов
Металлы являются материалами, обладающими уникальными механическими свойствами, которые делают их широко используемыми в различных отраслях промышленности. Одной из основных характеристик, определяющих механические свойства металлов, является их прочность.
Прочность - это способность материала сопротивляться разрушению при воздействии механических сил. Металлы обладают высокой прочностью, благодаря своей кристаллической решетке, которая позволяет атомам или ионам упаковываться плотно и образовывать сильные связи.
Еще одним важным механическим свойством металлов является пластичность. Она означает способность материала подвергаться деформации без разрушения. Металлы обладают высокой пластичностью благодаря движению ионов или атомов в кристаллической решетке, что позволяет им принимать новые формы при механической обработке.
Кроме того, у металлов высокая твердость, которая определяется способностью материала сопротивляться постоянной деформации под воздействием внешних сил. Это свойство связано с силой сцепления атомов или ионов в кристаллической решетке.
Еще одним важным механическим свойством металлов является их упругость. Упругий материал способен восстанавливать свою форму после снятия деформации. Металлы обладают высокой упругостью благодаря своей кристаллической решетке, которая обеспечивает быстрое восстановление структуры после механического воздействия.
Таким образом, металлы обладают высокой прочностью, пластичностью, твердостью и упругостью благодаря особенностям их кристаллической решетки, что делает их одними из наиболее востребованных материалов в различных отраслях промышленности.
Химические свойства металлов

Металлы обладают рядом характерных химических свойств, которые определяют их широкое применение в различных сферах нашей жизни.
Во-первых, металлы обладают способностью образовывать катионы - положительно заряженные ионы. При этом они обычно теряют электроны из внешней энергетической оболочки и становятся менее электронегативными по сравнению с неметаллами.
Во-вторых, металлы активно реагируют с кислородом. В результате окисления металла, например железа при взаимодействии с воздухом, образуется ржавчина. Окисление металлов является процессом, сопровождающим многочисленные реакции, которые основываются на передаче электронов.
Металлы могут реагировать с кислотами с образованием солей и выделением водорода. Такие реакции можно наблюдать, например, при взаимодействии цинка с соляной кислотой или алюминия с солями других металлов.
Кроме того, металлы способны к образованию сплавов. Это смеси металлов, получаемые путем плавления и смешивания при наличии определенного соотношения компонентов. Сплавы обладают новыми свойствами, которые часто улучшают технические характеристики материала.
Таким образом, химические свойства металлов определяют их активность в реакциях с другими веществами, что делает их важными материалами для многих отраслей промышленности и науки.
Влияние ионов и атомов на свойства металлов

Свойства металлов определяются как структурой, так и химическим составом кристаллической решетки. Эта решетка состоит из ионов и атомов, которые влияют на физические и химические свойства металлов.
Ионы в кристаллической решетке металла имеют различные заряды, что позволяет им формировать ионные связи. Эти связи обладают высокой прочностью и способствуют высоким температурным плавлениям, твердости и прочности металлов. Кристаллическая решетка, состоящая из ионов, также обеспечивает электрическую проводимость металлов.
Атомы, входящие в состав кристаллической решетки, определяют химические свойства металлов. Различные атомы могут образовывать сплавы, что позволяет изменять свойства металла. Например, добавление цинка к железу приводит к образованию сплава, называемого оцинкованным железом, который обладает повышенной коррозионной стойкостью.
Ионы и атомы также влияют на электронные свойства металлов. Наличие свободных электронов, которые могут двигаться по всей решетке, обеспечивает электропроводность металлов. Заряженные ионы и атомы влияют на подвижность этих электронов, определяя проводимость металла.
Таким образом, ионы и атомы, составляющие кристаллическую решетку металлов, играют ключевую роль в формировании их физических, химических и электронных свойств. Понимание влияния этих компонентов является основой для разработки новых сплавов и улучшения свойств металлических материалов.
Вопрос-ответ

Что такое кристаллическая решетка?
Кристаллическая решетка - это регулярное упорядоченное расположение атомов или ионов в кристаллическом веществе. Она определяет свойства и структуру кристалла, и может быть описана с помощью трех измерений - длины, ширины и высоты.
Какие свойства металлов определяются их кристаллической решеткой?
Кристаллическая решетка металлов определяет их механические, тепловые, электрические и другие свойства. Например, размер и форма решетки влияют на прочность и пластичность металла, а плотность решетки - на его плотность и теплопроводность. Разделение металла на отдельные кристаллы также определяет его поликристаллическую структуру и магнитные свойства.
Чем отличается кристаллическая решетка ионов от кристаллической решетки атомов?
Кристаллическая решетка ионов и атомов отличается тем, какие частицы располагаются в решетке и как они связаны между собой. В решетке ионов, атомы замещены ионами, которые имеют заряды и могут притягивать или отталкивать соседние частицы. В решетке атомов, атомы не имеют зарядов и связаны только взаимодействием электронных облаков.
Какие особенности кристаллической решетки металлов?
Основные особенности кристаллической решетки металлов - это наличие свободных электронов и межатомных связей. В металлическом кристалле, атомы металла образуют ковалентные связи и образуют сеть плотно упакованных атомов. Электроны в металлической решетке совместно принадлежат всем атомам и могут свободно передвигаться по кристаллической решетке, что делает металл хорошим проводником тепла и электричества.
Почему металлы обладают высокой теплопроводностью?
Металлы обладают высокой теплопроводностью благодаря свободным электронам в их кристаллической решетке. Свободные электроны металла могут свободно двигаться по решетке и передавать тепло от одного атома к другому. Это позволяет металлам эффективно распространять тепловую энергию и иметь высокую теплопроводность.
