Пероксиды щелочных металлов – это класс химических соединений, состоящих из атомов щелочных металлов (например, натрия, калия, лития) и атомов кислорода, связанных между собой химической связью одного из мощных соединений - пероксидной связью. Такая структура обуславливает названия пероксидов, которые в химической номенклатуре обозначаются названием металла с соответствующим индексом окисления и словом "пероксид" после него.
Строение пероксидов щелочных металлов характеризуется наличием их особой структуры – кристаллической решетки, которая образуется благодаря упорядоченному расположению атомов металла и кислорода в основной элементной ячейке соединения. Это предопределяет некоторые свойства и особенности взаимодействия пероксидов с другими веществами.
Кристаллическая решетка пероксидов щелочных металлов образует простейший кубический тип, в котором каждый атом щелочного металла окружен шестью атомами кислорода, образующими октакоординационную сферу. В свою очередь, атом кислорода окружен шестью атомами металла, что придает пероксидам высокую структурную устойчивость и прочность.
Пероксиды щелочных металлов: строение и свойства
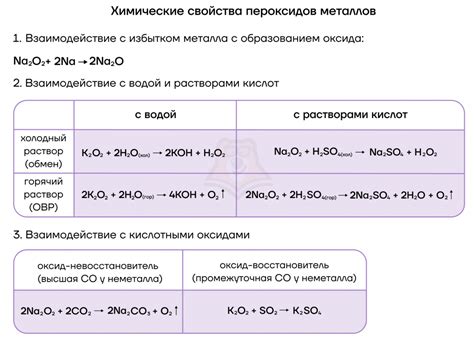
Пероксиды щелочных металлов являются соединениями, содержащими в своей структуре анион пероксида, состоящий из двух атомов кислорода, связанных между собой. Данные соединения представляют собой мощные окислители и обладают рядом интересных свойств и применений.
Строение пероксидов щелочных металлов характеризуется простой ионной решеткой, в которой положительно заряженные катионы металла окружены отрицательно заряженными анионами пероксида. Двухатомная структура пероксидного аниона позволяет ему легко проникать внутрь решетки катионов металла.
Одним из основных свойств пероксидов щелочных металлов является их способность к автоокислительно-восстановительным реакциям. При взаимодействии с другими соединениями пероксиды щелочных металлов окисляют их, переходя при этом в более низкоокисленное состояние и выделая при этом кислород. Это свойство пероксидов широко используется в химической промышленности и в качестве катализаторов в органическом синтезе.
Еще одной важной характеристикой пероксидов щелочных металлов является их способность к быстрой дезинфекции и окислению органических веществ. Благодаря этим свойствам пероксиды находят применение в медицине, в процессе обеззараживания поверхностей и портирования пищевых продуктов.
Основные свойства пероксидов щелочных металлов

Пероксиды щелочных металлов - это соединения, состоящие из атомов металла и пероксидных групп, содержащих два атома кислорода, связанных между собой. Они обладают рядом особых свойств, которые определяют их химическую природу и применение в различных областях.
Одно из основных свойств пероксидов щелочных металлов - их окислительная активность. Эти соединения легко окисляют другие вещества, особенно органические соединения. Пероксиды щелочных металлов широко используются в качестве окислителей в различных промышленных процессах, таких как белизна и отбеливание текстиля, производство красителей и препаратов для волос.
Еще одно важное свойство пероксидов щелочных металлов - их антиокислительная активность. Они обладают способностью снижать содержание свободных радикалов в организме, которые могут нанести вред клеткам и вызвать возникновение различных заболеваний. Поэтому пероксиды щелочных металлов широко применяются в фармацевтической промышленности для производства препаратов, предназначенных для улучшения обмена веществ и поддержания здоровья организма.
Также пероксиды щелочных металлов проявляют алкалинные свойства. Они растворяются в воде с образованием щелочных растворов, к которым относятся гидроксиды и пероксиды соответствующих металлов. Это свойство пероксидов используется для регулирования pH-уровня в различных промышленных процессах и в качестве щелочей в различных химических реакциях.
Важно отметить, что пероксиды щелочных металлов обладают высокой реакционной способностью. Они реагируют с различными веществами, такими как кислород, кислоты, спирты, образуя новые соединения. Это делает их важными компонентами в химической промышленности, где они находят применение в производстве различных продуктов и материалов.
Применение пероксидов щелочных металлов в различных отраслях

Пероксиды щелочных металлов – это соединения, содержащие атомы кислорода в двухвалентном состоянии. Они широко применяются в различных отраслях благодаря своим уникальным химическим свойствам.
Применение в медицине
Пероксиды щелочных металлов используются в медицине как антисептики и дезинфицирующие средства. Они обладают сильными окислительными свойствами, что позволяет эффективно бороться с микроорганизмами и предотвращать инфекции. Кроме того, пероксиды щелочных металлов используются в процессе заживления ран и язв, так как стимулируют образование новых тканей.
Применение в экологии
Пероксиды щелочных металлов играют важную роль в экологической сфере. Они используются для очистки воды и воздуха от загрязнений. Пероксиды образуют активные кислородные радикалы, которые способны окислять и разлагать токсические вещества, в результате чего происходит их нейтрализация. Это позволяет улучшить качество окружающей среды и снизить воздействие вредных веществ на здоровье человека и животных.
Применение в производстве
Пероксиды щелочных металлов используются в производстве различных продуктов, включая бумагу, текстиль, пищевые добавки и косметические средства. Они являются важными компонентами в процессе отбеливания и обработки материалов, а также в качестве катализаторов химических реакций. Благодаря своей высокой активности, пероксиды щелочных металлов обеспечивают эффективные и экологически безопасные процессы производства.
Применение в энергетике
Пероксиды щелочных металлов находят применение в энергетической отрасли. Они используются в процессе хранения и переноса кислорода, который является одним из основных компонентов в батареях и аккумуляторах. Пероксиды обеспечивают надежное сохранение кислорода и его безопасную транспортировку, что является важным фактором для энергетического оборудования и систем хранения энергии.
Применение в научных исследованиях
Пероксиды щелочных металлов широко используются в научных исследованиях. Они служат исходными материалами для получения различных соединений и веществ, используемых в химии и биологии. Благодаря своей химической активности и стабильности, пероксиды щелочных металлов являются важными инструментами для проведения различных экспериментов и исследований.
Безопасность и хранение пероксидов щелочных металлов

Пероксиды щелочных металлов, такие как пероксид натрия и пероксид калия, являются химическими соединениями с повышенной реактивностью и потенциальной опасностью для здоровья и окружающей среды. Поэтому очень важно соблюдать правила безопасности при работе с ними и правильно хранить данные соединения.
Пероксиды щелочных металлов являются сильными окислителями и могут вызывать образование взрывоопасных смесей при взаимодействии с органическими веществами, а также с противопоказанными собственными веществами. Поэтому необходимо соблюдать предельную осторожность при работе с ними, использовать перчатки, защитные очки и хорошо проветривать рабочее место.
Для хранения пероксидов щелочных металлов необходимо учитывать их особенности. Соединения этого типа должны храниться отдельно от других химических веществ, особенно от веществ, которые могут реагировать с пероксидами. Необходимо выбирать специальные контейнеры, предназначенные для хранения таких соединений, такие как стеклянные банки или пластиковые емкости с крышками из нержавеющей стали, чтобы избежать непредсказуемых химических реакций. Также следует хранить пероксиды в хорошо проветриваемом и сухом помещении, защищенном от огня и высоких температур.
При хранении и обращении с пероксидами щелочных металлов необходимо соблюдать некоторые специальные меры предосторожности. Например, при открывании или пробивании контейнера с пероксидом необходимо делать это под контролируемыми условиями, чтобы избежать возгорания или взрыва. Также не рекомендуется перемешивать пероксиды с другими химическими веществами, если это не требуется для определенного эксперимента или процесса. В случае непредвиденных реакций или аварийной ситуации необходимо незамедлительно принять меры по локализации и устранению утечек и связаться с профессионалами в области безопасности.
Вопрос-ответ

Какие металлы формируют пероксиды?
Пероксиды образуются щелочными металлами, такими как натрий, калий и цезий.
Каково строение пероксидов щелочных металлов?
Строение пероксидов щелочных металлов заключается в том, что каждый металл связан с двумя атомами кислорода через атомы пероксида.
Какие свойства имеют пероксиды щелочных металлов?
Пероксиды щелочных металлов обладают окислительными свойствами и являются сильными окислителями. Они также могут реагировать с водой, выделяя кислород.
Чем пероксиды щелочных металлов полезны?
Пероксиды щелочных металлов используются как кислородные источники в различных процессах и реакциях, таких как окисление органических соединений.
В чем состоит структура пероксида металла?
Структура пероксида щелочных металлов включает в себя ионы металла, которые окружены атомами кислорода, связанными между собой двумя атомами пероксида.
