Металлы – это одна из наиболее распространенных и важных групп химических элементов, существующих в природе. Они представлены в таблице Менделеева и обладают рядом особенностей, определяющих их строение и свойства. Основные черты, которые характеризуют металлы, делают их уникальными материалами с широким спектром применения.
Во-первых, металлы обладают высокой тепло- и электропроводностью. Это связано с особенностью электронного строения атомов металлов, в котором одна или несколько внешних оболочек содержат свободные электроны. Благодаря этому, металлы способны передавать электроны с одной части материала на другую, что обуславливает их проводящие свойства. Также высокая теплопроводность металлов объясняется этой особенностью строения, так как свободные электроны способны переносить тепловую энергию.
Во-вторых, металлы обладают характерным металлическим блеском. Это свойство связано с взаимодействием свободных электронов с падающим светом. При попадании световых волн на поверхность металла, электроны начинают колебаться и испускают световые фоны, в результате чего металл приобретает свой характерный блеск.
Кроме того, металлы обладают высокой пластичностью и прочностью. Пластичность – это способность материала изменять свою форму без разрушения. Она связана с особенностями строения металлов, так как свободные электроны позволяют атомам подвижно перемещаться друг относительно друга. Прочность металлов обусловлена их кристаллической структурой, где атомы располагаются строго по определенным плоскостям.
История открытия и классификация металлов
История открытия и классификации металлов тесно связана с развитием человеческой цивилизации. С первобытных времен люди использовали металлы для создания оружия, инструментов и украшений. С течением времени открытие новых металлов и развитие технологий их обработки стали одной из ключевых задач не только в науке, но и в промышленности.
Процесс открытия новых металлов начался с древности, когда люди обнаружили медь и олово. В древности металлы классифицировались по своим физическим свойствам и использованию. Однако систематическая классификация металлов возникла лишь в результате развития химии и открытия периодической системы элементов Д.И. Менделеевым в конце XIX века.
В таблице Менделеева металлы группируются в левой части таблицы, начиная с щелочных металлов и заканчивая металлами платиновой группы. Металлы характеризуются отличительными чертами: высокой теплопроводностью и электропроводностью, способностью придавать изделиям прочность и долговечность.
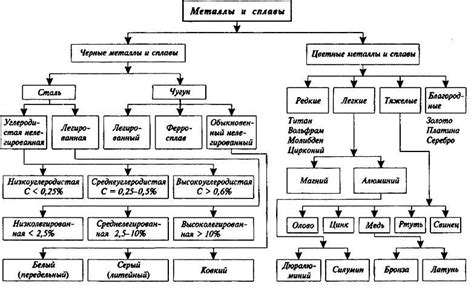
Современная классификация металлов основана на совокупности признаков – химическом составе, физических свойствах и области применения. Металлы делятся на легкоплавкие и тугоплавкие, цветные и черные, драгоценные и недрагоценные. Каждая группа металлов обладает своими уникальными свойствами и используется в разных отраслях промышленности.
- Легкоплавкие металлы – алюминий, магний, свинец – имеют низкую температуру плавления и широко используются в авиационной и автомобильной промышленности, а также как конструкционные материалы.
- Цветные металлы – медь, золото, серебро – обладают высокой электропроводностью и активно используются в электротехнике, электронике и ювелирной промышленности.
- Черные металлы – железо и его сплавы – широко применяются в строительстве, машиностроении и автомобильной промышленности.
- Драгоценные металлы – платина, золото, серебро – используются в ювелирном и финансовом секторе, а также в производстве катализаторов и электроники.
Важно отметить, что металлы имеют большое значение не только для промышленности, но и для нашей повседневной жизни. Они используются как строительные материалы, для производства техники, оружия, украшений и многого другого. Благодаря своим уникальным свойствам, металлы стали неотъемлемой частью современного мира и драйвером прогресса во многих отраслях науки и технологий.
Структура атома и особенности металлической связи

Структура атома является основополагающей для понимания особенностей металлической связи. Атом состоит из ядра, которое содержит протоны и нейтроны, и облака электронов, движущихся вокруг ядра.
Металлическая связь является особым типом химической связи, характерным для металлов. Она осуществляется между положительно заряженными ионами металлов и свободными электронами, образуя так называемую "электронную оболочку". Эта связь обладает некоторыми особенностями, которые обусловливают уникальные свойства металлов.
Одной из особенностей металлической связи является подвижность электронов внутри металлической решетки. Электроны в металлах не привязаны к конкретным атомам, а перемещаются свободно по всей структуре. Это обеспечивает высокую электропроводность и теплопроводность металлов.
Еще одной особенностью металлической связи является возможность образования кристаллической структуры. Металлы обычно имеют регулярную и упорядоченную решетку атомов, благодаря чему они обладают высокой плотностью и механической прочностью.
Кроме того, металлическая связь обусловливает специфические химические свойства металлов, например, их способность образовывать сплавы и легко принимать ионную форму, участвовать в реакциях окисления и восстановления, а также проявлять ферромагнетизм и др.
Основные свойства металлов и их значение в промышленности

Металлы – одни из основных материалов, используемых в промышленности. Их основные свойства делают их незаменимыми во многих отраслях, таких как машиностроение, энергетика, строительство и другие.
Первое основное свойство металлов – проводимость электричества и тепла. Благодаря этому свойству металлы широко используются в производстве электрооборудования и проводов, а также в теплотехнике и реакторных установках. Металлические проводники электричества обладают высокой эффективностью и низкими потерями энергии.
Второе важное свойство – пластичность. Металлы можно легко обрабатывать: ковать, прокатывать, волочить. Это позволяет изготавливать различные изделия разнообразной формы, а также проводить вторичную обработку для получения точности и желаемых характеристик. Пластичность металлов важна в производстве автомобилей, трубопроводов, металлоконструкций и других продуктов.
Третье важное свойство – прочность. Металлы обладают высокой механической прочностью, что делает их незаменимыми материалами в строительстве и машиностроении. Благодаря своей прочности, металлы выдерживают большие нагрузки и испытания, обеспечивая надежность и долговечность конструкций и машин.
Четвертое важное свойство металлов – коррозионная стойкость. Многие металлы обладают способностью к самозащите от коррозии, что позволяет им использоваться в условиях высокой влажности, агрессивной среды и коррозийных процессов. Это важно в производстве химической промышленности, водоснабжения, судостроения и других отраслях.
Таким образом, основные свойства металлов – проводимость, пластичность, прочность и коррозионная стойкость – делают их ценными и незаменимыми материалами в промышленности. Они являются основой многих технологических процессов и обеспечивают надежность и эффективность в производстве различных продуктов и конструкций.
Таблица Менделеева и строение металлов: основные черты
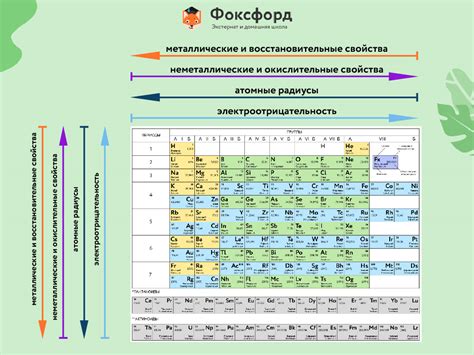
Таблица Менделеева является основой для изучения и классификации элементов, в том числе и металлов. Металлы занимают большую часть таблицы Менделеева и обладают рядом общих черт в своем строении.
Одной из основных черт металлов является наличие электронов в валентной оболочке. Все металлы находятся слева от линии разделения в таблице Менделеева и обладают от одного до трех электронов в валентной оболочке. Такое строение позволяет металлам образовывать идеальную кристаллическую решетку, что делает их прочными и устойчивыми в процессе деформации.
Еще одной особенностью металлов является способность проводить тепло и электричество. Объясняется это наличием свободных электронов, которые могут свободно перемещаться внутри металлической решетки и переносить энергию. Именно благодаря этой способности металлы широко используются в электротехнике и теплотехнике.
Кроме того, металлы обладают высокой плотностью и тяжестью. Большинство металлов имеют высокие температуры плавления и кипения, что обуславливается их атомной структурой и энергетическими особенностями.
Таким образом, таблица Менделеева позволяет систематизировать и классифицировать металлы, а их строение обусловливает их основные черты, такие как прочность, электропроводность и теплопроводность. Эти особенности делают металлы незаменимыми материалами во многих отраслях промышленности и науки.
Вопрос-ответ

Что такое таблица Менделеева?
Таблица Менделеева - это упорядоченная система, которая представляет все известные на данный момент химические элементы в виде таблицы, где они расположены по возрастанию атомного номера и атомной массы. Она была разработана русским химиком Дмитрием Менделеевым в 1869 году.
Какие основные черты строения металлов можно выделить?
Основные черты строения металлов включают: решетчатую структуру, образованную регулярно расположенными положительными ионами металла и свободно движущимися электронами; устойчивость металлов благодаря сильным межатомным связям; наличие валентных и скрытых валентных электронов, что позволяет металлам образовывать разнообразные соединения; и наличие свободных электронов, которые могут быть ответственными за химическую реактивность металлов.
Какие свойства металлов связаны со строением металла?
Строение металла определяет такие свойства металлов, как высокая теплопроводность, электропроводность и относительно низкое плотление. Решетчатая структура металла обеспечивает свободное движение электронов, что позволяет проводить ток. Кроме того, строение металла обуславливает его механическую прочность и пластичность, что делает металлы удачными материалами для строительства и производства различных изделий.
В чем разница между решетчатой структурой металла и молекулярной структурой вещества?
Решетчатая структура металла отличается от молекулярной структуры вещества тем, что регулярно расположенные положительные ионы металла образуют решетку, а между ними находятся свободно движущиеся электроны. В молекулярной структуре вещества, например, воды, атомы связаны ковалентной связью и образуют молекулы, которые могут свободно двигаться вещества в зависимости от условий.
