Атомы - это основные строительные блоки всего материального мира. Стоит отметить, что они могут быть различными, и одно из ключевых различий состоит в том, являются ли они металлами или неметаллами.
Металлы - это группа элементов, которые обладают рядом уникальных свойств. Они обычно хорошие проводники электричества и тепла, обладают блестящей поверхностью и гибкостью. Основным строительным блоком металлов является кристаллическая решетка, в которой положительно заряженные ионы располагаются в регулярном порядке. Эта упорядоченность обуславливает уникальные физические и химические свойства металлов.
Неметаллы, в свою очередь, имеют отличия от металлов как по строению, так и по свойствам. В отличие от металлов, они плохие проводники тепла и электричества. Неметаллы обычно образуют молекулы, состоящие из атомов, и располагаются внутри сетки, схожей с кристаллической решеткой, но нестоль упорядоченной и регулярной. Это дает неметаллам возможность образовывать более сложные структуры.
В результате различного строения и особенностей металлов и неметаллов, они обладают разными физическими и химическими свойствами, что определяет их разную роль в процессах их применения в различных отраслях промышленности и науки.
Строение атомов: металлы и неметаллы
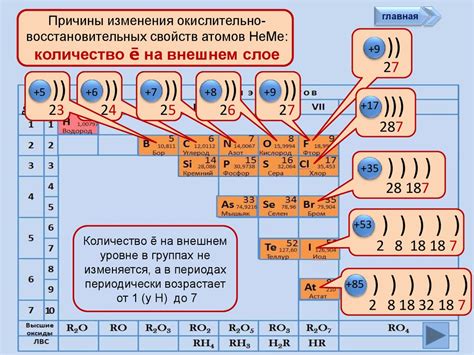
Строение атомов металлов и неметаллов определяет их особенности и свойства. Атомы металлов обладают отличительной структурой, которая позволяет им выступать в качестве отличных проводников электричества и тепла. Они характеризуются наличием свободных электронов, которые легко движутся по кристаллической решетке металла.
В то же время атомы неметаллов имеют более сложное строение и электронную орбиталь, что делает их плохими проводниками электричества. Однако, неметаллы обладают большей силой взаимодействия с другими элементами, что позволяет им образовывать разнообразные химические соединения и химические реакции.
В таблице Менделеева металлы располагаются слева, а неметаллы - справа. Обычно металлы относят к группам 1-12, а неметаллы - к группам 13-18. Однако, существуют и полуметаллы, которые располагаются на границе между металлами и неметаллами. Полуметаллы обладают свойствами как металлов, так и неметаллов.
Строение атомов металлов и неметаллов имеет прямое отношение к их физическим и химическим свойствам. Понимание этой особенности позволяет более глубоко изучать их взаимодействие с другими веществами и применять в различных областях, таких как промышленность, электроника и медицина.
Особенности металлов:

Металлы являются основным классом элементов в периодической системе и характеризуются рядом особенностей, которые делают их уникальными в мире атомов.
1. Проводимость электричества и тепла: Металлы обладают высокой проводимостью электричества и тепла. Эта особенность связана с особой структурой их атомов, в которых свободные электроны могут двигаться свободно. Именно благодаря этому свойству металлы широко используются в электронике, электротехнике и других отраслях промышленности.
2. Гибкость и пластичность: Металлы могут быть легко подвергнуты деформации и принимать различные формы. Это обусловлено наличием свободных электронов и их способностью перемещаться внутри металлической сетки. Благодаря этой особенности металлы применяются в производстве различных изделий, от автомобилей до мелких электронных компонентов.
3. Металлический блеск: Металлы обладают характерным металлическим блеском, который связан с возможностью свободных электронов поглощать и переизлучать свет. Эта особенность делает металлы эстетически привлекательными и применимыми в ювелирном искусстве.
4. Высокая плотность: Металлы обладают высокой плотностью, что обусловлено компактностью их атомов в кристаллической решетке. Именно благодаря этой особенности металлы обладают высокой механической прочностью и используются в строительстве и машиностроении.
5. Склонность образовывать ионы положительного заряда: Металлы имеют способность отдавать электроны и образовывать ионы положительного заряда. Это связано с их низкой электроотрицательностью и строением атомов. Благодаря этой способности металлы могут образовывать ионы, которые в свою очередь могут быть использованы для соединения с другими элементами и образования различных химических соединений.
Особенности неметаллов:
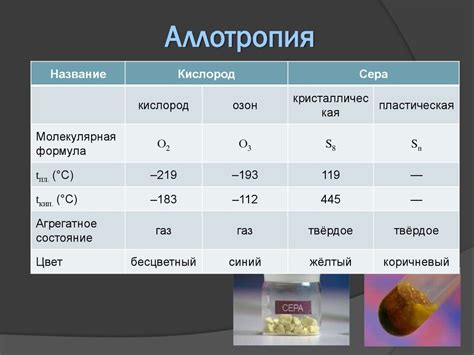
Неметаллы — элементы, которые отличаются от металлов как физическими, так и химическими свойствами. Они находятся на правой стороне периодической системы элементов и включают такие вещества, как кислород, углерод, азот и многие другие.
Одной из особенностей неметаллов является их негативный заряд ядра атома, что делает их способными привлекать электроны и образовывать ковалентные связи. В отличие от металлов, неметаллы обычно не обладают выраженной металлической блеской и небольшой проводимостью электричества и тепла.
Неметаллы обладают высокой электроотрицательностью, что позволяет им образовывать ионные связи с металлами или ковалентные связи с другими неметаллами. Их атомы имеют обычно небольшие размеры и большую силу притяжения электронных оболочек, в результате чего неметаллы образуют молекулы, состоящие из двух или более атомов.
Однако неметаллы могут образовывать различные структуры, такие как слоистые кристаллы (графит), полимеры (полиэтилен) и аморфные вещества (стекло). Это связано с их способностью образовывать различные химические связи, такие как водородные связи, дипольно-дипольные взаимодействия и взаимодействия Ван-дер-Ваальса.
Неметаллы играют важную роль во многих областях науки и техники. Например, кислород является необходимым для дыхания живых организмов, а углерод является основным компонентом органических веществ. Кроме того, неметаллы используются в производстве полупроводников, катализаторов, полимеров и других материалов, которые находят применение в различных отраслях промышленности.
Вопрос-ответ

Чем особенно отличаются атомы металлов от атомов неметаллов?
Атомы металлов обычно имеют меньшую электроотрицательность и большую способность отдавать электроны. Они имеют малое количество электронов во внешней оболочке и склонны образовывать положительно заряженные ионы. Атомы неметаллов, напротив, имеют высокую электроотрицательность и большую способность принимать электроны. Они обычно имеют большое количество электронов во внешней оболочке и склонны образовывать отрицательно заряженные ионы или молекулы, связанные ковалентными связями.
Почему металлы обладают хорошей электропроводностью?
Металлы обладают хорошей электропроводностью из-за особенностей строения и поведения их атомов. Атомы металлов обычно имеют свободные или подвижные электроны во внешней оболочке, которые легко могут передвигаться между атомами. Это позволяет электронам не привязываться к определенным атомам и свободно двигаться по металлической структуре, создавая электрический ток при подключении источника энергии.
Какие особенности строения атомов металлов делают их хорошими проводниками тепла?
Металлы являются хорошими проводниками тепла благодаря особенностям строения и поведения атомов. Под действием тепловой энергии свободные электроны в металлах приобретают кинетическую энергию и начинают двигаться по металлической решетке, передавая энергию от атома к атому. Это позволяет металлам быстро и эффективно распространять тепло по всему объему материала.
