Металл натрий является одним из наиболее распространенных элементов в природе и занимает одно из ведущих мест в периодической системе химических элементов. Строение его атома является интересным и важным объектом изучения в химии.
Схема строения атома натрия может быть представлена следующим образом: атомных ядер в нем находится 11 протонов и 12 нейтронов, что делает его заряд положительным и равным +11e. Вокруг ядра вращаются 11 электронов, создавая область отрицательного заряда и делая атом нейтральным.
Каждый электрон в атоме натрия занимает свою энергетическую оболочку, которая представлена электронными орбиталями. Первая энергетическая оболочка содержит одну s-орбиталь, на которой располагается два электрона. Вторая энергетическая оболочка содержит одну s-орбиталь и три p-орбитали, на которых располагается восемь электронов.
Строение атома натрия имеет определенные свойства и особенности, которые определяют его поведение в химических реакциях и взаимодействии с другими веществами. Изучение схемы строения атома металла натрия является важным для понимания его химических свойств и применения в различных областях науки и техники.
Строение атома натрия
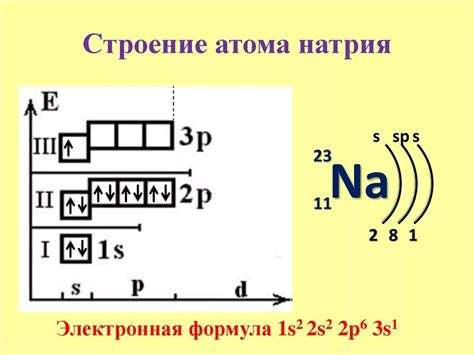
Атом натрия представляет собой элементарную частицу, обладающую положительным зарядом ядра и отрицательно заряженными электронами, движущимися вокруг ядра в электронных оболочках.
Атом натрия состоит из 11 протонов, 11 нейтронов и 11 электронов. Протоны и нейтроны находятся в ядре атома, образуя его центральную часть. Электроны располагаются на электронных оболочках вокруг ядра.
Первая электронная оболочка атома натрия может вместить не более 2 электронов. Вторая электронная оболочка может вместить до 8 электронов. Таким образом, внешняя оболочка атома натрия содержит один электрон. Этот электрон называется валентным электроном и определяет химические свойства атома.
Строение атома натрия можно представить в виде электронной конфигурации: 1s² 2s² 2p⁶ 3s¹.
Атом натрия обычно находится в ионизированном состоянии, что означает, что он имеет отсутствие или избыток электронов. В ионизированном состоянии атом натрия образует ион Na⁺, потеряв один валентный электрон.
Строение атома натрия является основой для его химических свойств и реакций. Взаимодействуя с другими атомами, натрий может образовывать соединения и участвовать в различных реакциях. Способность атома натрия образовывать ионы и участвовать в химических реакциях объясняет его активность и широкое применение в различных отраслях промышленности и науки.
Основные компоненты

Атом металла натрия состоит из нескольких основных компонентов, каждый из которых играет свою роль в структуре и свойствах вещества. Одним из основных компонентов является ядро атома, которое содержит протоны и нейтроны. Протоны - частицы положительного заряда, определяющие химические свойства элемента. Нейтроны не имеют заряда и помогают поддерживать стабильность ядра.
Вокруг ядра находятся электроны - частицы отрицательного заряда. Электроны находятся на разных уровнях энергии, которые называются электронными оболочками. Наиболее близким к ядру является первая оболочка, которая может вмещать всего два электрона. Следующая оболочка может вместить уже восемь электронов, и так далее.
Количество электронов в последней заполненной оболочке атома натрия определяет его химические свойства. У натрия в последней оболочке находится один электрон, что делает его весьма реакционноспособным элементом.
Кроме того, в структуре атома натрия присутствует электронная оболочка со слабым связью, называемая внешней оболочкой. Эта оболочка состоит из трёх электронов, которые слабо связаны с ядром и могут участвовать в химических реакциях с другими атомами.
Внешняя оболочка атома натрия дает ему возможность образовывать ионный связь с другими атомами. Таким образом, основными компонентами атома металла натрия являются ядро с протонами и нейтронами, электроны на электронных оболочках и внешняя оболочка с электронами, способными образовывать связи.
Внешнее строение
Атом натрия состоит из ядра и электронной оболочки. Ядро натрия содержит протоны и нейтроны, которые находятся плотно друг к другу и образуют ядро. Протоны имеют положительный заряд, а нейтроны не имеют заряда. Таким образом, ядро находится в центре атома и содержит большую часть его массы.
Электронная оболочка атома натрия состоит из электронов, которые обращаются вокруг ядра. Электроны имеют отрицательный заряд и создают электронную оболочку, которая окружает ядро. Электроны располагаются на разных энергетических уровнях, и наибольшая часть электронов находится на внешнем энергетическом уровне.
У атома натрия на внешнем энергетическом уровне находится один электрон. Внешний электрон представляет собой электрон валентной оболочки, который участвует в химических реакциях. Валентный электрон определяет химические свойства атома натрия и его способность образовывать соединения с другими элементами.
Внешний электрон атома натрия обладает относительно низкой энергией и легко участвует в обмене электронами с другими атомами. Именно благодаря валентному электрону атом натрия образует ионы и образует различные соединения, такие как хлорид натрия или оксид натрия. Внешняя оболочка атома натрия является важным фактором в его химической активности и влияет на его взаимодействие с другими элементами.
Внутреннее строение
Атом натрия имеет следующую схему строения. В центре атома располагается ядро, в котором находятся протоны и нейтроны. Протоны имеют положительный заряд, а нейтроны являются нейтральными. Количество протонов определяет атомный номер в периодической системе элементов, поэтому для натрия атомный номер равен 11.
Вокруг ядра располагаются электроны. Электроны имеют отрицательный заряд и совместно с протонами образуют электронную оболочку атома натрия. Электроны располагаются на разных энергетических уровнях в атоме и заполняют их по принципу минимальной энергии.
Схему расположения электронов в атоме натрия можно представить следующим образом:
- На первом энергетическом уровне располагается 2 электрона.
- На втором энергетическом уровне располагается 8 электронов.
- На третьем энергетическом уровне также может располагаться 8 электронов, но в атоме натрия он заполнен только до 1 электрона.
Все эти электроны образуют электронную оболочку, которая обеспечивает стабильность атома и его взаимодействие с другими атомами.
Эта схема строения атома натрия помогает понять его химические свойства и взаимодействие с другими веществами.
Взаимодействия с другими атомами

Атомы металла натрия активно взаимодействуют с другими атомами, образуя различные соединения и соединительные связи. Основными типами взаимодействий являются ионные связи, ковалентные связи и металлические связи.
Ионные связи: Ионы натрия, имеющие положительный заряд, вступают в реакцию с атомами, обладающими отрицательными зарядами. В результате образуются ионные соединения, такие как хлорид натрия (NaCl) или сульфат натрия (Na2SO4). Ионные связи характеризуются сильной электростатической привлекательной силой между положительными и отрицательными ионами.
Ковалентные связи: Атомы натрия также могут образовывать ковалентные связи, в которых они обменивают электроны с другими атомами. Примером такого взаимодействия может служить образование молекулы хлорида натрия (NaCl) с помощью обмена одного электрона между атомами натрия и хлора. Ковалентные связи обладают средней прочностью и сохраняются в молекуле или соединении.
Металлические связи: Атомы натрия также способны образовывать металлические связи, в которых свободные электроны перемещаются между атомами и создают силы притяжения. Это позволяет атомам металла сформировать кристаллическую решетку и образовывать металлические структуры. Металлические связи обладают высокой твердостью и проводимостью электричества и тепла.
Таким образом, атомы металла натрия проявляют различные типы взаимодействий с другими атомами, образуя ионные, ковалентные и металлические связи. Эти взаимодействия позволяют создавать разнообразные соединения и способствуют формированию металлических структур.
Вопрос-ответ

Какова основная схема строения атома металла натрия?
Атом металла натрия имеет электронную конфигурацию [Ne] 3s1, что означает, что внешний электрон равен электронному конфигурации инертного газа неона (Ne) и находится в третьей энергетической оболочке на подуровне s.
Какие уровни энергии занимают электроны в атоме натрия?
Электроны в атоме натрия занимают три уровня энергии: первый, второй и третий. На первом уровне находится 2 электрона, на втором - 8 электронов, а на третьем - 1 электрон.
Каково количество протонов и нейтронов в атоме металла натрия?
В атоме металла натрия находится 11 протонов и, как правило, 12 нейтронов. Протоны находятся в ядре атома вместе с нейтронами, а электроны окружают ядро.
Что происходит с электронами в атоме натрия при образовании ионов?
При образовании ионов электроны в атоме натрия могут быть переданы или получены. Атом натрия имеет один внешний электрон в третьей энергетической оболочке. При потере этого электрона атом становится положительным ионом с зарядом +1. Приобретение этого электрона другим атомом приведет к образованию отрицательного иона с зарядом -1.
